Clear Sky Science · de
Wnt-3a verschärft die Produktion von TNF-α in mit LPS stimulierten Mikroglia unabhängig vom kanonischen β‑Catenin‑Weg
Warum Gehirnentzündungen wichtig sind
Viele Erkrankungen des Gehirns, einschließlich der Parkinson‑Krankheit, gehen inzwischen mit chronischer Entzündung einher. Bei diesem Vorgang können die im Gehirn ansässigen Immunzellen, die sogenannten Mikroglia, von schützenden Helfern zu überaktiven Angreifern werden, die benachbarte Neurone schädigen. Diese Studie stellt eine aktuelle Frage: Kann ein Signalmolekül namens Wnt‑3a, dem lange Zeit beruhigende, schützende Wirkungen zugeschrieben wurden, unter bestimmten Bedingungen die Entzündung tatsächlich verschlimmern? Die Antwort ist komplexer als erwartet und zeigt, warum dasselbe Molekül in einem Kontext hilfreich und in einem anderen schädlich sein kann.
Ein Botenstoff mit zwei Gesichtern
Wnt‑Proteine sind eine Familie chemischer Botenstoffe, die die Gehirnentwicklung steuern, Zellen im Erwachsenenalter erhalten und beeinflussen, wie Zellen auf Verletzungen reagieren. Eines der am besten untersuchten Mitglieder, Wnt‑3a, wird häufig mit einem „kanonischen“ Signalweg in Verbindung gebracht, der ein Protein namens β‑Catenin in der Zelle stabilisiert. In vielen Systemen scheint die Aktivierung dieses Weges Entzündungen zu dämpfen und das Überleben von Neuronen zu fördern, weshalb einige Forscher gehofft haben, dass eine Verstärkung von Wnt‑3a gefährdete dopaminproduzierende Neurone bei der Parkinson‑Krankheit schützen könnte. Wnt‑Proteine können jedoch auch über alternative, „nicht‑kanonische“ Wege signalisieren, die stattdessen Entzündungen fördern können – welcher Weg dominiert, hängt vom Zelltyp und dessen Zustand ab.
Wenn ruhige Zellen ruhig bleiben
Um diese Möglichkeiten zu untersuchen, analysierten die Forscher primäre Mikroglia, die aus Mäusegehirnen gewonnen wurden. Zunächst betrachteten sie Mikroglia im ruhenden, homöostatischen Zustand und setzten sie nur Wnt‑3a aus. Unter diesen ruhigen Bedingungen erhöhte Wnt‑3a nicht die Freisetzung wichtiger Entzündungsmoleküle wie TNF‑α oder IL‑1β. Obwohl einige zelluläre Signalwege aktiviert wurden, gingen die Mikroglia nicht in einen ausgeprägt entzündlichen Zustand über. Das legt nahe, dass das alleinige Zufügen von Wnt‑3a in einem gesunden, nicht entzündeten Gehirn die entzündliche Aktivität der Mikroglia nur geringfügig beeinflussen könnte.
Wenn entzündete Zellen weiter angekurbelt werden
Das Bild änderte sich dramatisch, sobald die Mikroglia zuerst mit bakterieller Lipopolysaccharid (LPS) in einen entzündlichen Zustand versetzt wurden – ein gängiges Laborwerkzeug zur Nachahmung einer Infektion. Wie erwartet führte LPS allein zu einem starken Anstieg der TNF‑α‑Produktion. Wurde Wnt‑3a jedoch zusammen mit LPS gegeben, setzten die Mikroglia deutlich mehr TNF‑α frei als bei LPS allein, während IL‑1β nicht weiter anstieg. Detaillierte Messungen zeigten, dass dieser Anstieg von TNF‑α nicht auf eine stärkere Aktivierung des üblichen NFκB‑Entzündungswegs oder auf eine zusätzliche Aktivierung des kanonischen β‑Catenin‑Pfads zurückzuführen war. Das Blockieren des β‑Catenin‑Wegs mit einem Protein namens DKK1 ließ den durch Wnt‑3a ausgelösten TNF‑α‑Anstieg unverändert, was darauf hinweist, dass der erwartete „anti‑entzündliche“ Weg nicht verantwortlich war.
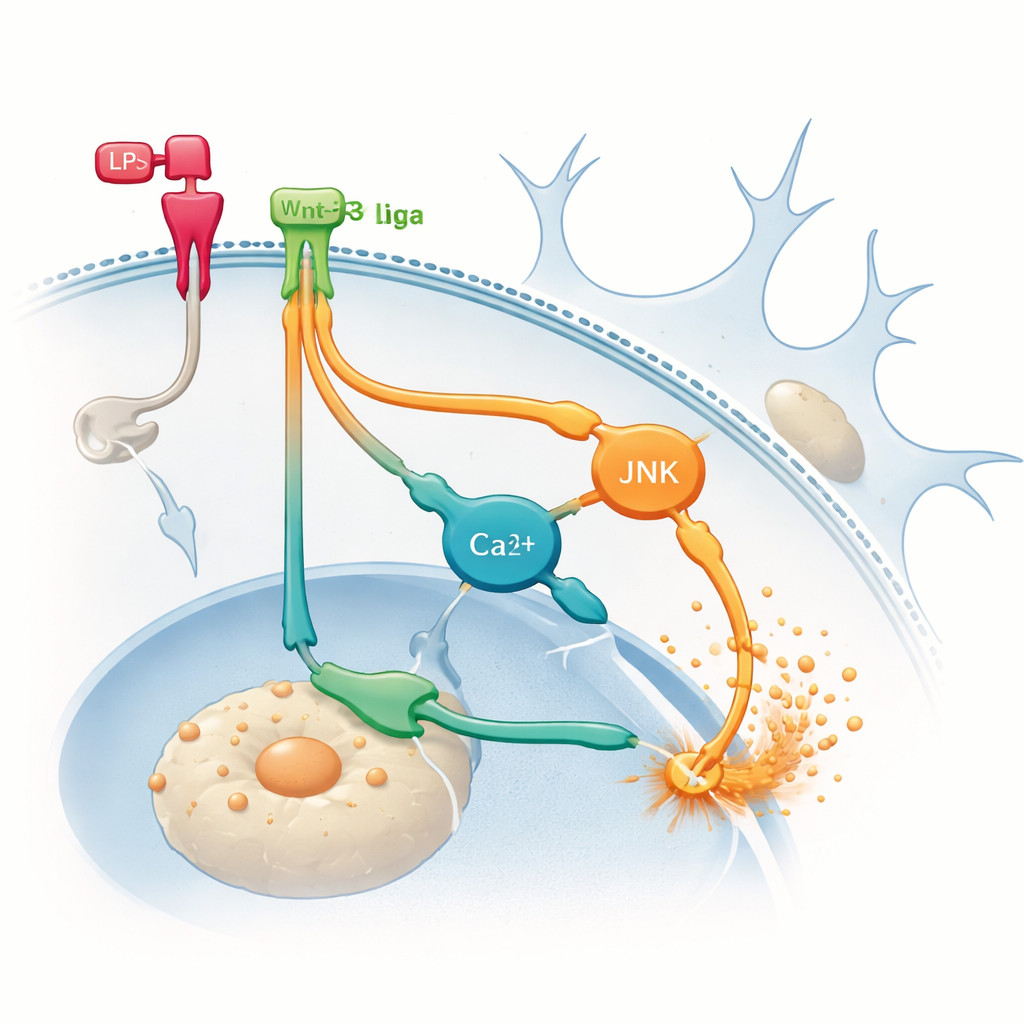
Versteckte Wege, die das Feuer schüren
Um herauszufinden, woher die zusätzliche Entzündung stammte, wandte sich das Team den alternativen, nicht‑kanonischen Wegen zu, die Wnt‑Proteine nutzen können. Sie blockierten pharmakologisch zwei Signaläste innerhalb der Mikroglia: einen, an dem ein Protein namens JNK beteiligt ist, und einen anderen, der mit Änderungen der Calciumkonzentration in der Zelle verknüpft ist. Die Hemmung eines dieser Zweige reduzierte die durch LPS induzierte TNF‑α‑Produktion und verhinderte, dass Wnt‑3a TNF‑α weiter verstärkte. Diese Ergebnisse deuten darauf hin, dass Wnt‑3a, sobald Mikroglia bereits entzündet sind, überwiegend nicht‑kanonische Wege nutzt, die entzündliche Signale verstärken statt zu beruhigen. Anders formuliert: Derselbe Botenstoff kann je nach dem Ausgangszustand der Zelle einen anderen inneren Pfad nehmen, mit sehr unterschiedlichen Folgen.
Test in einem Parkinson‑Modell
Die Forscher fragten dann, ob dieses Verhalten von Wnt‑3a in Mikroglia sich in einem lebenden Gehirn auf Neurone auswirken würde. Sie infundierten Wnt‑3a direkt in die Ventrikel von Mäusen, die mit dem Toxin MPTP behandelt wurden – ein weit verbreitetes Modell für Parkinson‑ähnliche Schädigungen von Dopaminneuronen und Mikrogliaaktivierung. Wie erwartet verringerte MPTP die Zahl der Dopaminneurone und erhöhte die Mikrogliaanzahl in einer für die Bewegung wichtigen Mittelhirnregion. Zusätzliches Wnt‑3a verschlechterte jedoch weder den Neuronenverlust noch veränderte es die Mikrogliazahlen im Vergleich zu mit Vehikel behandelten Tieren signifikant. In diesem komplexen in vivo‑Setting schützte Wnt‑3a über den untersuchten Zeitraum weder eindeutig noch verschlechterte es die schädigenden Effekte des Toxins.
Was das für künftige Therapien bedeutet
Insgesamt zeigt die Studie, dass Wnt‑3a kein einfacher Ein‑/Aus‑Schalter für Gehirnentzündungen ist. In ruhigen Mikroglia zeigt es wenig Wirkung, doch in bereits entzündeten Zellen kann es selektiv die Freisetzung von TNF‑α über nicht‑kanonische Signalwege steigern, unabhängig vom klassischen β‑Catenin‑Weg. Zugleich schützte oder schädigte die Gabe von Wnt‑3a in einem Parkinson‑ähnlichen Mausmodell die Dopaminneurone kurzfristig nicht eindeutig. Für die Entwicklung zukünftiger Therapien ist die Kernbotschaft, dass die Zielrichtung der Wnt‑Signalgebung den zellulären Kontext genau berücksichtigen muss. Auf Wnt‑3a oder verwandte Moleküle gestützte Therapien könnten in manchen Situationen nützlich sein, in anderen jedoch nach hinten losgehen, wenn sie unbeabsichtigt schädliche Entzündungsreaktionen verstärken.
Zitation: Federici, G., Stayte, S., Rentsch, P. et al. Wnt-3a exacerbates production of TNF-α in LPS stimulated microglia independent of the β-catenin canonical pathway. Sci Rep 16, 8222 (2026). https://doi.org/10.1038/s41598-026-37653-1
Schlüsselwörter: Gehirnentzündung, Mikroglia, Wnt-Signalgebung, Parkinson-Krankheit, TNF-alpha