Clear Sky Science · de
APOL1-Plasmamembran-Pools widerstehen schneller Proteinabbaurate
Warum das „Verschwinden“ eines Nierenproteins wichtig ist
Ein großer Anteil schwerer Nierenerkrankungen bei Menschen mit jüngerer afrikanischer Abstammung lässt sich auf zwei Varianten eines einzelnen Gens, APOL1, zurückführen. Dennoch tun sich Wissenschaftler schwer, genau zu erklären, wie dieses Gen Nierenzellen schädigt, ohne die meisten Träger zu beeinträchtigen. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Sobald das APOL1-Protein in Zellen hergestellt ist, wie lange bleibt es bestehen und wo ist es am stabilsten? Die Antworten zeigen eine überraschende gespaltene Persönlichkeit — APOL1 wird innerhalb der Zelle schnell abgebaut, bleibt jedoch hartnäckig stabil, wenn es in der äußeren Zelloberfläche eingebettet ist. Das ist ein Hinweis, der künftige Therapien leiten könnte.
Risikogen mit zweischneidiger Wirkung
Das APOL1-Gen schützt Menschen vor bestimmten Parasiten, ein evolutionärer Vorteil, der wahrscheinlich erklärt, warum seine Risikoformen, genannt G1 und G2, in afrikanischen Populationen verbreitet sind. Unglücklicherweise haben Menschen, die zwei Kopien dieser Varianten erben, ein deutlich erhöhtes Risiko für als APOL1-vermittelte Nierenerkrankungen zusammengefasste Leiden. Frühere Arbeiten zeigten, dass erhöhte APOL1-Spiegel — häufig als Reaktion auf Entzündungen — das Protein toxisch machen können, besonders in empfindlichen Filterzellen der Niere, den Podozyten. Die meisten Studien haben sich jedoch darauf konzentriert, was APOL1 anschaltet. Viel weniger war darüber bekannt, wie Zellen es wieder abschalten, zum Beispiel durch den Abbau des Proteins.
Ein zerbrechliches Protein in der Zelle verfolgen
Um die Stabilität von APOL1 zu untersuchen, erzeugten die Forschenden humane Zelllinien, die fluoreszenzmarkierte Versionen von APOL1 und seinem nächsten Verwandten APOL2 produzierten. Damit konnten sie beobachten, wie viel von jedem Protein unter verschiedenen Bedingungen akkumulierte oder verschwand, mithilfe von Western Blot, Mikroskopie und Durchflusszytometrie. Sie blockierten die Hauptproteinzerstörungsmaschine der Zelle, das Proteasom, und in einer separaten Behandlung die Neusynthese von Proteinen. Wenn das Proteasom gehemmt war, stiegen die APOL1-Spiegel schnell an, was zeigt, dass es normalerweise rasch abgebaut wird. Wenn die Neusynthese gestoppt wurde, fielen die APOL1-Spiegel schnell. Im starken Kontrast dazu veränderte sich APOL2 unter keiner der Behandlungen nennenswert, was es als deutlich stabileres Protein erscheinen lässt. Wichtig ist, dass der hohe Umsatz von APOL1 sowohl für die normale Version (G0) als auch für die Nierenrisikovarianten (G1 und G2) gleich war und sich über mehrere natürlich vorkommende APOL1-Formen hinweg zeigte, die sich darin unterscheiden, wie sie in Membranen liegen.
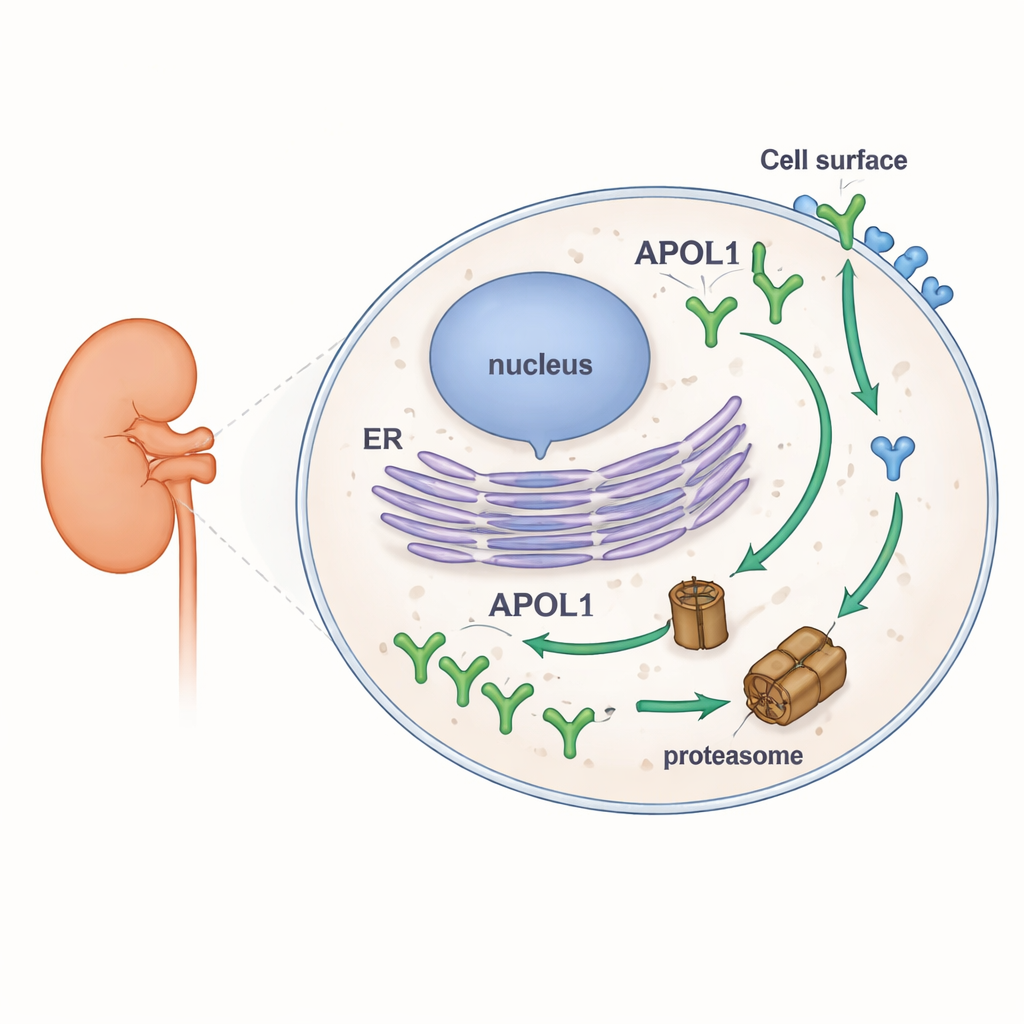
Sequenzhinweise und die Geschichte zweier Nachbarschaften
Bei der Analyse der Proteinstruktur nutzte das Team Computertools, um APOL1 und APOL2 nach flexiblen, ungeordneten Segmenten zu durchsuchen, die als intrinsisch ungeordnete Regionen bekannt sind. Solche Regionen fungieren oft als „friss mich“-Signale für das Proteasom. Sie identifizierten zwei starke Kandidatenregionen in APOL1, die in APOL2 weitgehend fehlten. Um zu testen, ob das einzigartige vordere Ende von APOL1 zu seiner Zerbrechlichkeit beiträgt, erzeugten sie Chimären: ein verkürztes APOL1, dem die ersten 59 Aminosäuren fehlten, und eine APOL2-Chimäre, die dieses APOL1-Segment trug. Das Hinzufügen des N-terminalen Stücks von APOL1 zu APOL2 ließ APOL2 schneller abgebaut werden, während das verkürzte APOL1 instabil blieb, was darauf hindeutet, dass mehr als ein Teil von APOL1 den schnellen Abbau fördert. Zusammengenommen verbinden diese Ergebnisse APOL1s ungewöhnliche flexible Segmente mit seinem schnellen Umsatz, ohne dieses Verhalten spezifisch an die krankheitsverursachenden Varianten zu binden.
Hartnäckiges Protein an der Zelloberfläche
Die auffälligste Beobachtung ergab sich, als die Autorinnen und Autoren zwischen APOL1 im Zellinneren und APOL1 an der Zelloberfläche unterschieden. Mithilfe von Antikörpern, die nur den nach außen gerichteten Teil von APOL1 erkennen, maßen sie die Oberflächenlevel getrennt von den Gesamtleveln. Im Zellinneren verhielt sich APOL1 erwartungsgemäß: Es häufte sich an, wenn das Proteasom blockiert war, und verschwand schnell, wenn die Neusynthese gestoppt wurde. Oberflächen-APOL1 hingegen veränderte sich unter keiner der Bedingungen nennenswert. Sobald APOL1-Moleküle die Plasmamembran erreichten, erwiesen sie sich als hochgradig resistent gegen schnellen Abbau. Darüber hinaus produzierten die Risikovarianten zwar weniger Gesamt-APOL1 als die normale Version, ihre Oberflächenlevel waren jedoch ähnlich. Das legt nahe, dass Risiko- und normale APOL1-Innenpools in vergleichbarer Weise abgebaut werden, die membran-gebundenen Pools — von denen angenommen wird, dass sie Ionenkanäle bilden und Toxizität antreiben — jedoch bei allen Varianten erhalten bleiben.
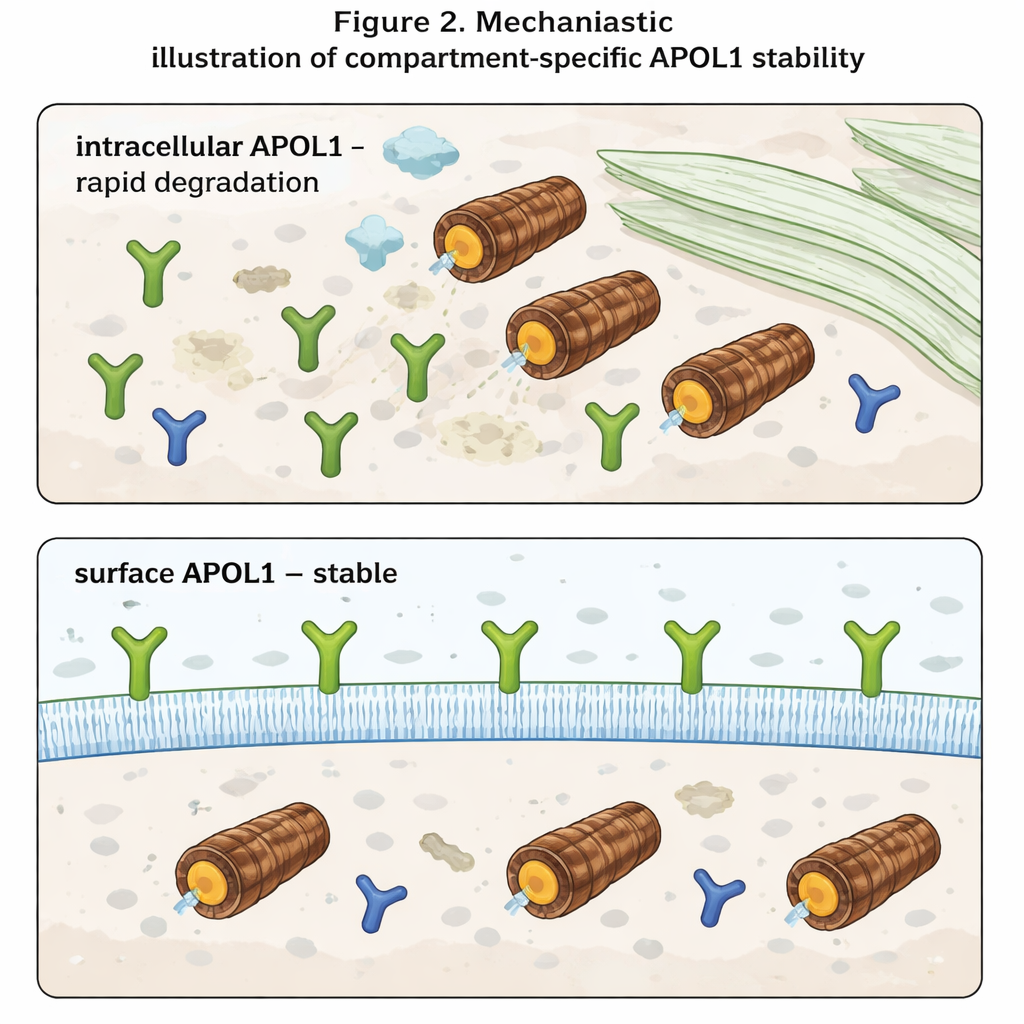
Was das für zukünftige Behandlungen bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft: APOL1 verhält sich sehr unterschiedlich, je nachdem, wo es sich befindet. Im Zellinneren ist es ein kurzlebiges Protein, das schnell erkannt und zerstört wird. An der Zelloberfläche hingegen ist es langlebig und relativ geschützt, selbst wenn die Abbaumaschinerie der Zelle verändert ist. Da die Krankheit offenbar entsteht, wenn APOL1-Kanäle an der Oberfläche das Gleichgewicht von Ionen wie Natrium und Kalium stören, sollten Therapien weniger auf die Gesamtkonzentration von APOL1 abzielen als darauf, wie viel davon die Plasmamembran erreicht und dort bestehen bleibt. Strategien, die den Transport von APOL1 zur Oberfläche verringern oder selektiv den Oberflächenpool destabilisieren, könnten prinzipiell den Nierenschaden abmildern, ohne die nützlichen immunologischen Funktionen des Gens vollständig zu blockieren.
Zitation: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
Schlüsselwörter: APOL1, Nierenerkrankung, Proteinabbau, Plasmamembran, Proteasom