Clear Sky Science · de
Erhöhte Meropenem-Wirksamkeit durch ein aus dem Mikrobiom stammendes Peptid, das die OXA-48-Carbapenemase in carbapenemresistenten Klebsiella-pneumoniae-Isolaten angreift
Warum das für die Alltagsgesundheit wichtig ist
Antibiotikaresistenz macht einst gut behandelbare Infektionen schwieriger und manchmal unmöglich zu heilen, insbesondere in Krankenhäusern. Diese Studie untersucht einen neuen Weg, ein bestehendes Reserveantibiotikum, Meropenem, wieder wirksam zu machen gegen ein gefährliches Bakterium, Klebsiella pneumoniae, das häufig Intensivpatienten befällt. Statt ein völlig neues Medikament zu entwickeln, testen die Forschenden ein kleines Hilfsmolekül — ein Peptid aus dem menschlichen Mikrobiom — das eines der wichtigsten Resistenzwerkzeuge des Bakteriums deaktiviert, sodass Meropenem wieder wirken kann.
Ein hartnäckiger Krankenhauskeim und sein chemischer Schutzschild
Klebsiella pneumoniae ist eine häufige Ursache für Lungenentzündungen, Blutinfektionen und Harnwegsinfektionen bei hospitalisierten Patienten. Einige Stämme sind gegenüber Carbapenemen resistent, einer starken Antibiotikaklasse, die Ärzte normalerweise für schwere, schwer behandelbare Fälle aufbewahren. Viele dieser Bakterien produzieren ein spezielles Enzym namens OXA-48, das wie ein chemischer Schutzschild wirkt und Carbapenem-Arzneimittel abbaut, bevor diese das Mikrobenwachstum stoppen können. Im Nahen Osten, einschließlich Iran, sind OXA-48-produzierende Stämme besonders verbreitet, und die Behandlungsmöglichkeiten schwinden, da sogar gegenüber neueren Wirkstoffkombinationen Resistenzen auftreten. Dadurch ist OXA-48 ein vorrangiges Ziel für neue Therapien geworden.
Ein Hilfspeptid aus dem menschlichen Mikrobiom entwerfen
Die Forschenden hatten zuvor Computermodelle genutzt, um Datenbanken natürlicher menschlicher antimikrobieller Peptide—kurze Proteinfragmente, die von unserem Körper und den ansässigen Mikroben produziert werden—nach Kandidaten zu durchsuchen, die möglicherweise fest an das OXA-48-Enzym binden. Durch virtuelle Docking-Studien und lange molekulardynamische Simulationen verfeinerten sie diese Kandidaten und wählten eines aus, M104 genannt, das voraussichtlich stabil an die aktive Stelle des Enzyms bindet und dessen Funktion blockiert, dabei wasserlöslich und chemisch stabil bleibt. In dieser Studie prüften sie M104 im Labor, kombiniert mit Meropenem gegen 20 patientenabgeleitete Klebsiella-Isolate: 10, die OXA-48 produzierten und gegen Meropenem resistent waren, und 10, die keine Carbapenemasen aufwiesen und medikamentenempfindlich waren.
Ein altes Antibiotikum wieder wirksam machen
Wurde Meropenem allein eingesetzt, waren alle OXA-48-positiven Klebsiella-Isolate deutlich resistent. Die Zugabe des Peptids M104 veränderte dieses Bild. In der höchsten getesteten Konzentration verringerte M104 die benötigte Menge an Meropenem, um das Bakterienwachstum zu stoppen, für jeden getesteten resistenten OXA-48-Produzenten mindestens um die Hälfte — in manchen Fällen sogar bis zu sechsmal. Dadurch wurden viele Stämme von deutlich resistent in einen intermediären oder sogar empfänglichen Bereich verschoben, gemessen an akzeptierten klinischen Grenzwerten. Wichtig ist, dass M104 keine eigene abtötende Wirkung zeigte und Meropenem nicht verstärkte, wenn die Bakterien das OXA-48-Enzym nicht besaßen, was auf eine sehr spezifische Wirkung gegen diesen Resistenzmechanismus und nicht auf eine breite, nichtselektive Toxizität hinweist.
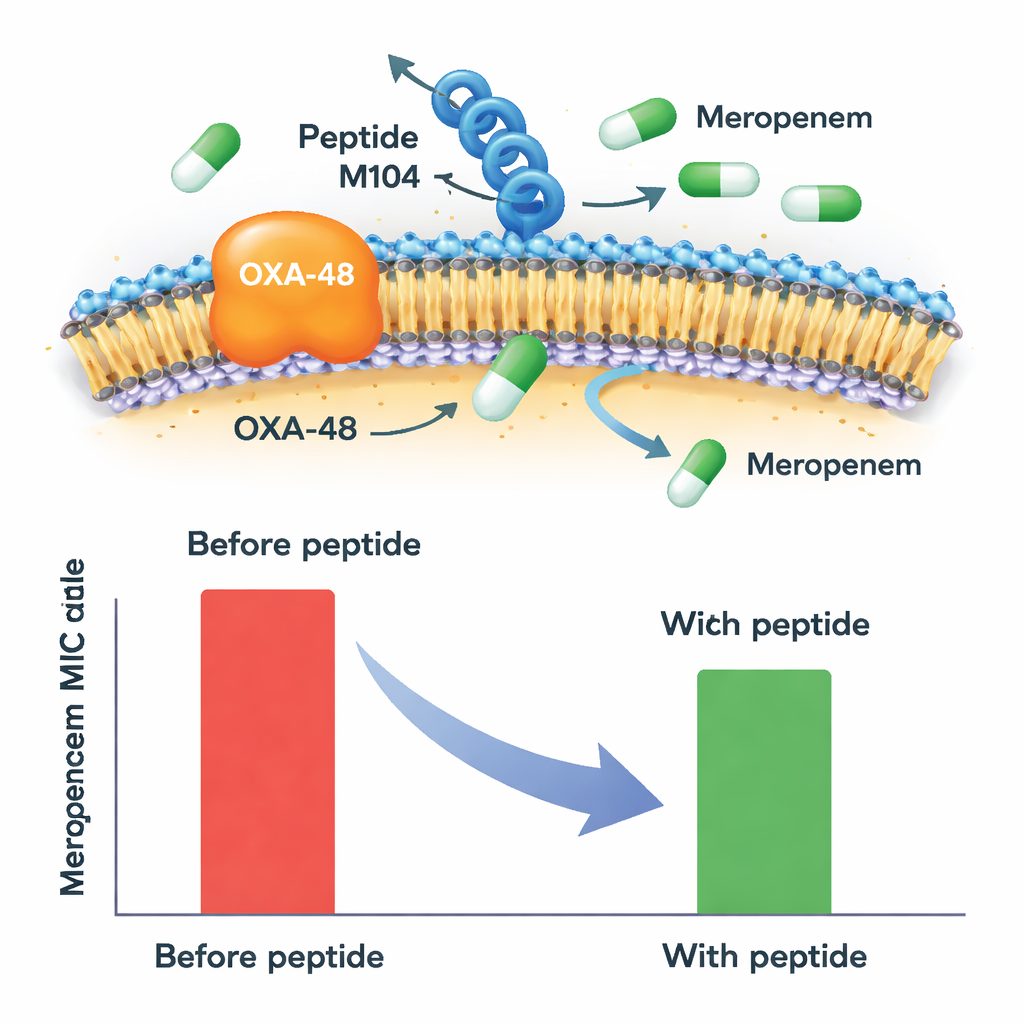
Herausforderungen durch schleimige Biofilme und Sicherheitsprüfungen
Viele Krankenhausinfektionen involvieren Biofilme—schleimige, geschichtete Bakteriengemeinschaften, die an Geräten und Geweben haften und wesentlich schwerer zu beseitigen sind als frei schwebende Zellen. Das Team prüfte daher, ob M104 Meropenem helfen kann, die Bildung von Biofilmen zu verhindern oder bereits bestehende Biofilme bei stark Biofilm-bildenden Klebsiella-Stämmen zu entfernen. Während die Peptid‑Meropenem-Kombination im Allgemeinen die benötigte Arzneimittelmenge zur Hemmung des Biofilmwachstums oder zur Einleitung der Entfernung reifer Biofilme halbierte, waren diese Effekte mäßig und erreichten in dieser kleinen Stichprobe keine klare statistische Signifikanz. Hinsichtlich der Sicherheit zeigte M104 keine nachweisbaren Schäden an menschlichen roten Blutkörperchen und verringerte die Lebensfähigkeit von menschlichen Hautfibroblasten nach 24 Stunden bei einer Konzentration, die über der in den Bakterientests verwendeten lag, nicht; erst nach 48 Stunden sank die Zellüberlebensrate um etwa 10 Prozent. Sequenzvergleiche deuteten außerdem auf ein geringes Risiko hin, dass das Peptid versehentlich andere bakterielle oder menschliche Proteine angreift.
Was das für künftige Behandlungen bedeuten könnte
Insgesamt deuten die Ergebnisse darauf hin, dass das Peptid M104 gezielt das OXA-48-Resistenzenzym entwaffnen und einen großen Teil der Wirksamkeit von Meropenem gegen ansonsten unbehandelbare Klebsiella pneumoniae wiederherstellen kann — zumindest für frei schwimmende Bakterien. Obwohl die Wirkung auf hartnäckige, etablierte Biofilme unter den getesteten Bedingungen begrenzt war, stellt die Studie den ersten berichteten peptidbasierten Blocker von OXA-48 vor und zeigt, dass solche gezielten Hilfsstoffe kurzzeitig sowohl wirksam als auch relativ schonend für menschliche Zellen sein können. Mit weiteren Tests an mehr Bakterienstämmen, anderen Carbapenemen, optimierten Formulierungen und Tiermodellen könnte diese Art präziser Zusatztherapie helfen, die nutzbare Lebensdauer unserer stärksten Antibiotika zu verlängern, anstatt Ärzten gegenüber resistenten Infektionen mit leeren Händen gegenüberzustehen.
Zitation: Sadeghi, S., Faramarzi, M.A. & Siroosi, M. Enhanced meropenem activity by a microbiome derived peptide targeting oxacillinase 48 carbapenemase in carbapenem resistant Klebsiella pneumoniae isolates. Sci Rep 16, 7589 (2026). https://doi.org/10.1038/s41598-026-37644-2
Schlüsselwörter: antibiotikaresistenz, carbapenemresistente Klebsiella, OXA-48-Enzym, Meropenem, Peptidinhibitoren