Clear Sky Science · de
In vitro-Charakterisierung der katalytischen Domäne der humanen Histon-Deacetylase 5
Warum winzige Schalter in unserer DNA-Verpackung wichtig sind
In jeder Zelle ist unsere DNA um Proteine gewickelt, die wie Spulen wirken und helfen, Meter an genetischem Material in mikroskopischen Raum zu packen. Ob ein Gen ein- oder ausgeschaltet ist, hängt oft von kleinen chemischen Markierungen auf diesen Spulenproteinen ab. Diese Studie fokussiert auf einen bestimmten Proteinschalter namens HDAC5, der mit Herzkrankheiten, neurologischen Störungen, Krebs und mehr in Verbindung gebracht wird. Indem die Forscher verstehen, wie HDAC5 auf molekularer Ebene arbeitet, wollen sie den Weg für präzisere Medikamente mit weniger Nebenwirkungen ebnen.
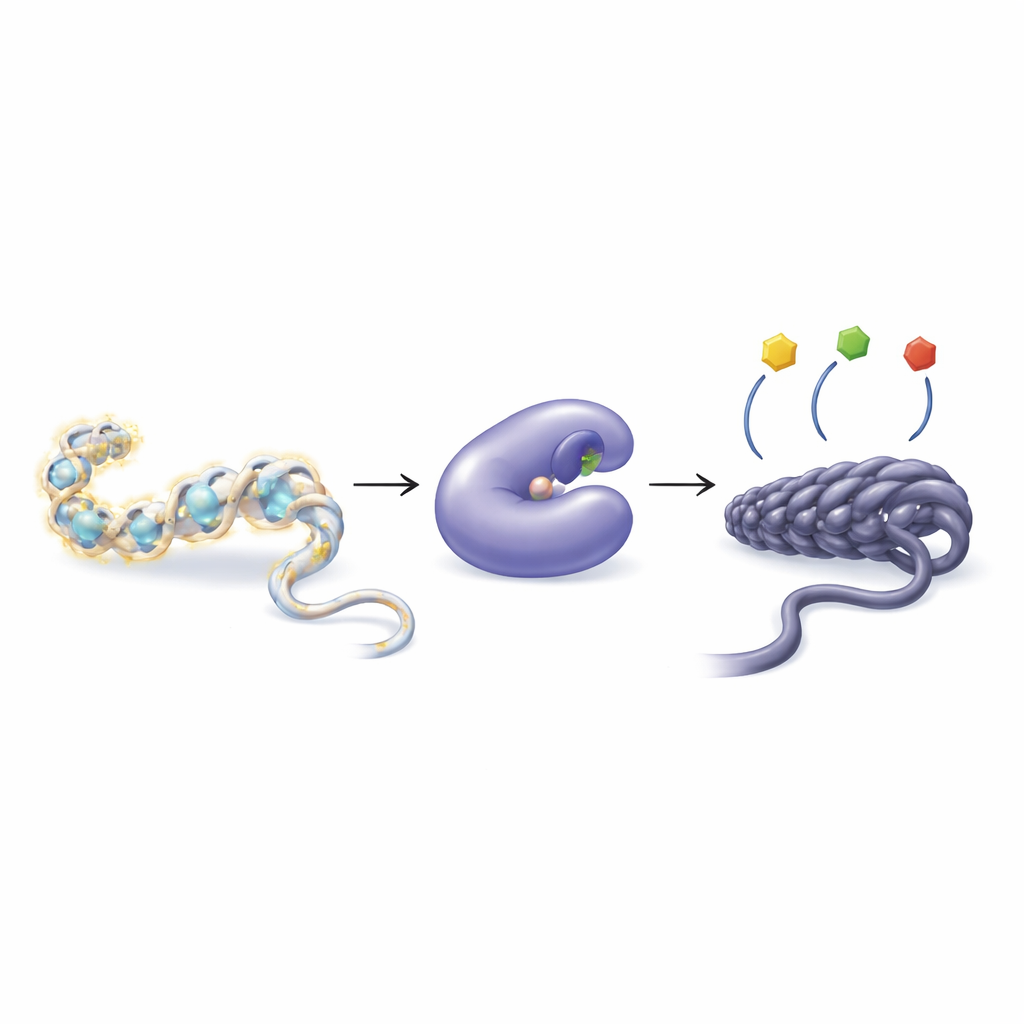
Wie Zellen Gene mit winzigen chemischen Markierungen einstellen
Unsere DNA liegt nicht frei, sondern ist um Proteine namens Histone gewickelt und bildet so die Struktur Chromatin. Zellen können kleine chemische Gruppen, etwa Acetylgruppen, an Histonschwänken anfügen oder entfernen, um das Chromatin lockerer oder dichter zu machen. Lockerere Verpackung macht Gene in der Regel leichter ablesbar; dichtere Verpackung führt häufig zu Stilllegung. Zwei Enzymgruppen steuern dieses Gleichgewicht: Histon-Acetyltransferasen fügen Acetylgruppen hinzu, während Histon-Deacetylasen (HDACs) sie entfernen. Wenn dieses Gleichgewicht gestört ist, kann das zu einer Vielzahl von Krankheiten beitragen, darunter Krebs, Herzleiden, Muskelabbau und Störungen des Immunsystems.
Warum HDAC5 ein vielversprechendes, aber anspruchsvolles Arzneimittelziel ist
HDACs bilden eine große Familie verwandter Enzyme, die in mehrere Klassen unterteilt ist. Viele der derzeit klinisch eingesetzten Medikamente blockieren mehrere HDAC-Typen gleichzeitig, was wichtige normale Funktionen abschalten und starke Nebenwirkungen verursachen kann. Klasse-IIa-HDACs, zu denen HDAC5 gehört, zeichnen sich dadurch aus, dass sie in bestimmten Geweben wie Gehirn, Herz und Skelettmuskulatur angereichert sind und mit anderen Proteinen zusammenarbeiten, um zentrale Gen-Netzwerke zu regulieren. HDAC5 wirkt oft als Brücke, indem es ein sehr aktives Partnerenzym (HDAC3) an bestimmte Gene bringt, sodass Chromatin verdichtet und diese Gene stillgelegt werden können. Wegen dieser fokussierten Rollen gilt HDAC5 als attraktives Ziel für selektivere Wirkstoffe, doch es fehlten bislang detaillierte biochemische Daten und eine hochauflösende Struktur seines aktiven Kerns, was rationale Wirkstoffentwicklung erschwert.
HDAC5 im Reagenzglas nachbauen
Um diese Lücke zu schließen, erzeugten die Forscher nur den katalytischen Kern von humanem HDAC5 – den Teil, der die chemische Reaktion ausführt – in Bakterien, reinigten ihn und bestätigten, dass er als stabile, einzelsträngige Einheit in Lösung vorliegt. Anschließend testeten sie seine Aktivität bei verschiedenen Salzkonzentrationen und pH-Werten. Die Aktivität von HDAC5 blieb über einen weiten Salzbereich robust und erreichte ihr Maximum bei mild basischen Bedingungen, ähnlich denen in vielen Zellen. Mit speziellen fluoreszierenden Testmolekülen fanden sie heraus, dass die natürliche Form von HDAC5 nur einen bestimmten Substrattyp erkennt, der üblicherweise zur Untersuchung von Klasse-IIa-Enzymen verwendet wird. Angelehnt an frühere Arbeiten an verwandten HDACs tauschten sie eine einzelne Aminosäure (Histidin) an einer kritischen Stelle gegen Tyrosin aus. Bemerkenswerterweise erlaubte diese kleine Änderung der mutierten HDAC5-Version, beide Arten von Testsubstraten effizient zu verarbeiten, und zeigte damit, wie eine einzelne Restgruppe im aktiven Zentrum die chemische Präferenz des Enzyms steuert.
Testen und Vergleichen von zwei neuen Wirkstoffkandidaten
Als Nächstes untersuchte das Team zwei experimentelle HDAC5-blockierende Moleküle, bekannt als NT160 und FFK24. Diese Verbindungen verwenden eine neuere Zink-Bindungsgruppe, die einige der Toxizität und schlechten Selektivität älterer, hydroxamatbasierter Wirkstoffe vermeidet. Durch Messung, wie jeder Inhibitor HDAC5 in sorgfältig kontrollierten Reaktionen verlangsamte, bestimmten die Autoren extrem niedrige Hemmkonstanten im Nanomolarbereich, was bedeutet, dass beide Verbindungen fest an das Enzym binden. NT160 band dabei konsequent etwa zehnmal stärker als FFK24. Um die Gründe hierfür zu verstehen, nutzten die Forscher computergestütztes Docking mit einer von AlphaFold vorhergesagten Struktur des HDAC5-Kerns. Beide Inhibitoren teilten eine gemeinsame Kopfregion, die tief in die aktive Tasche hineinreichte und mit dem Metallion in Kontakt trat, doch der Schwanz von NT160 bildete zusätzliche stabilisierende Kontakte mit spezifischen Aminosäuren in der Tasche. Diese zusätzlichen Wechselwirkungen erklären vermutlich seine höhere Wirksamkeit.
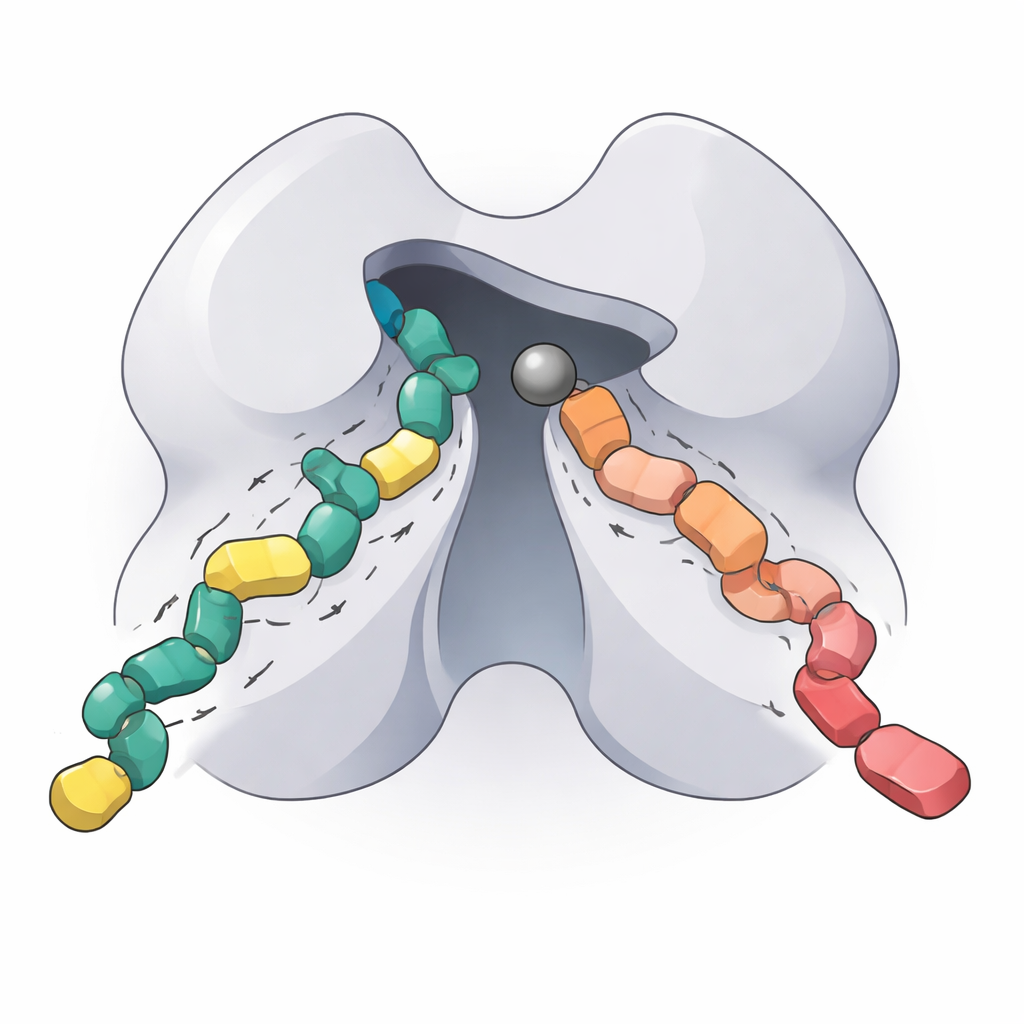
Was das für künftige zielgerichtete Therapien bedeutet
Indem sie den funktionellen Kern von HDAC5 rekonstruierten, seine optimalen Arbeitsbedingungen kartierten, aufschlüsselten, wie eine einzelne Aminosäurenänderung sein Verhalten verändert, und quantifizierten, wie zwei Next‑Generation-Inhibitoren binden, liefert diese Studie einen detaillierten biochemischen „Fingerabdruck“ eines wichtigen, zuvor untercharakterisierten Enzyms. Für Nicht‑Spezialisten ist die Kernbotschaft, dass HDAC5 dabei hilft, zu steuern, ob bestimmte Gene an- oder abgeschaltet sind, und dass das präzise Einstellen dieses Schalters bei der Behandlung von Herzkrankheiten, Neurodegeneration, Krebs und Immunstörungen wertvoll sein könnte. Die hier vorgestellten neuen Erkenntnisse und Werkzeuge sollten Forschern helfen, HDAC5‑ und Klasse‑IIa‑selektive Wirkstoffe zu entwickeln, die dort wirken, wo sie benötigt werden, und unerwünschte Effekte an anderen Stellen im Körper minimieren.
Zitation: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
Schlüsselwörter: Histon-Deacetylase 5, epigenetische Regulation, HDAC-Inhibitoren, zielgerichtete Krebstherapie, Chromatinstruktur