Clear Sky Science · de
H19 fördert das Wachstum und die Invasion von Bauchspeicheldrüsenkrebs, indem es die inhibitorischen Effekte von miR-29c-5p auf ATF2/ECM1 reduziert
Warum diese verborgene Zellbotschaft wichtig ist
Bauchspeicheldrüsenkrebs gehört zu den tödlichsten Krebserkrankungen, teilweise weil er häufig spät entdeckt wird und gegen gängige Therapien resistent ist. Diese Studie blickt über proteinkodierende Gene hinaus und konzentriert sich auf „stille“ genetische Botschaften – lange und kleine RNA-Moleküle –, die das Wachstum, die Ausbreitung und die Therapieflucht von Pankreastumoren unterstützen. Indem die Autoren aufdecken, wie eine lange RNA namens H19 und ein winziger Partner namens miR-29c-5p gemeinsam die Umgebung des Tumors umgestalten, zeichnen sie ein neues molekulares Schaltbild, das zu früherer Diagnose und präziseren Therapien führen könnte.
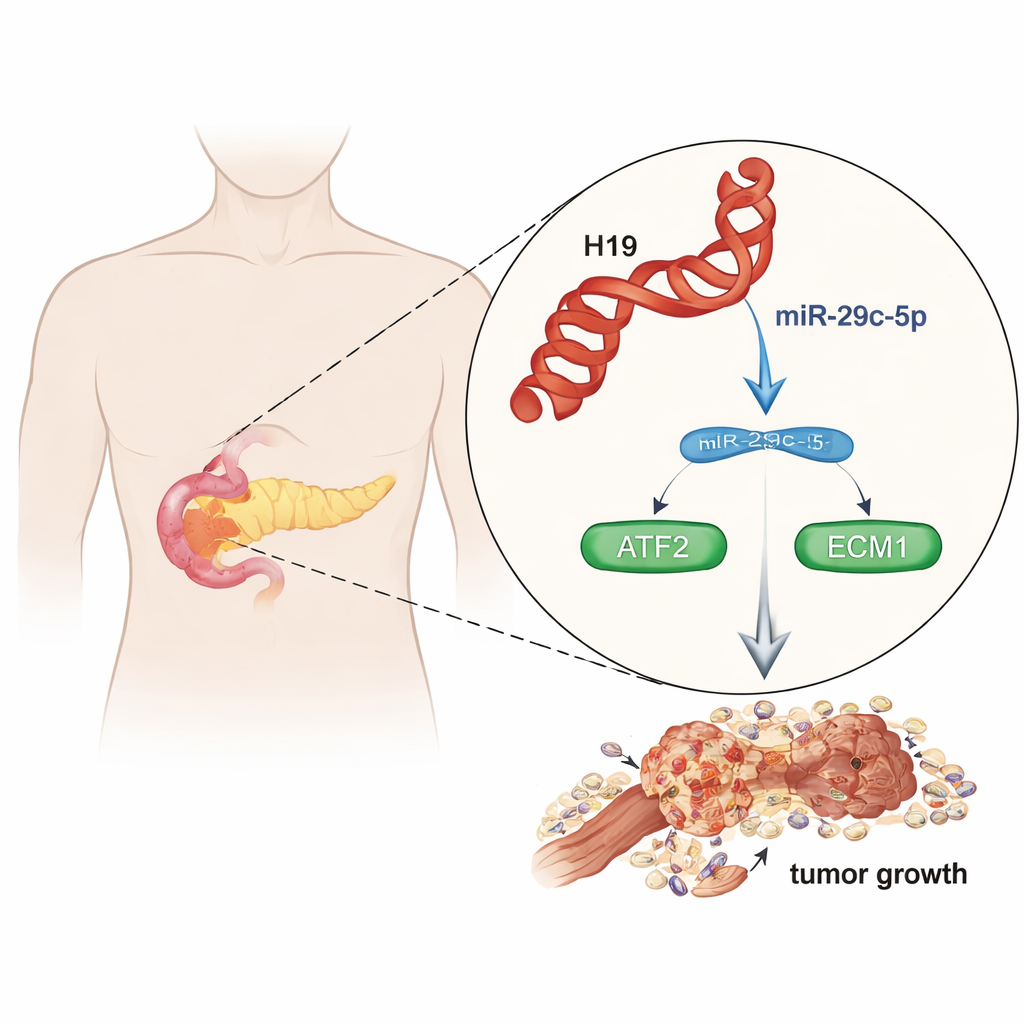
Ein gefährlicher Krebs mit wenigen Optionen
Das duktale Adenokarzinom der Bauchspeicheldrüse (PDAC) hat eine Fünf-Jahres-Überlebensrate unter 10 Prozent, hauptsächlich weil es früh metastasiert und schlecht auf Chemotherapie anspricht. Forschende erkennen zunehmend, dass nicht-kodierende RNAs – genetische Botschaften, die keine Proteine produzieren – mächtige Schalter sind, die das Krebsverhalten steuern. In dieser Arbeit analysierte das Team große öffentliche Datensätze und Patientenproben und fand heraus, dass eine solche lange nicht-kodierende RNA, H19, in Pankreastumoren konstant höher exprimiert ist als im gesunden Pankreasgewebe. Patienten mit Tumoren, die mehr H19 enthielten, starben früher, was darauf hindeutet, dass H19 nicht nur Beiwerk, sondern ein Treiber des aggressiven Verlaufs ist.
Wie H19 das Gleichgewicht in Tumorzellen verschiebt
Innerhalb der Zellen sitzt H19 überwiegend im wässrigen Zytoplasma, wo es eher mit anderen RNAs interagiert, statt direkt die DNA zu verändern. Die Autoren entdeckten, dass H19 wie ein molekularer Schwamm wirkt: Es bindet und hält eine kleine RNA namens miR-29c-5p, die sonst dazu beitragen würde, Tumorwachstum zu bremsen. Sind die H19-Spiegel hoch, steht weniger freies miR-29c-5p zur Verfügung, um seine Wächterfunktion auszuüben. Laborversuche zeigten, dass eine Erhöhung von H19 die Vermehrung von Pankreas-Krebszellen beschleunigte und ihre Wanderung durch künstliche Membranen erleichterte, während das Stilllegen von H19 ihr Wachstum und ihre Invasivität verlangsamte. Umgekehrt hob die Wiederherstellung von miR-29c-5p viele dieser schädlichen Effekte auf, was auf ein Tauziehen zwischen den beiden Molekülen hinweist.
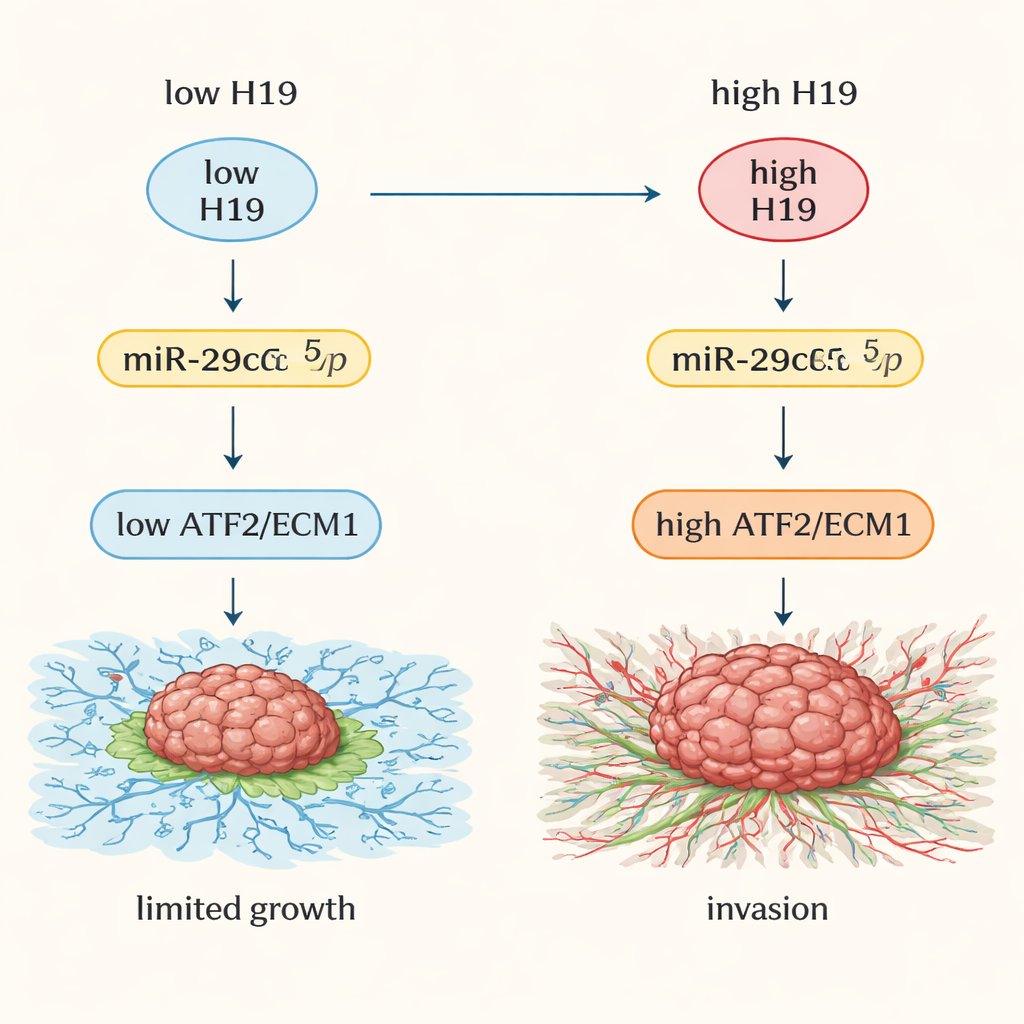
Abwärts gerichtete Ziele: Die Bremsen des Tumorwachstums lösen
Die kleine RNA miR-29c-5p hilft normalerweise, zwei wichtige Proteine zu dämpfen: ATF2, einen Genregulator im Zellkern, und ECM1, ein Protein, das die extrazelluläre Matrix gestaltet. Wenn miR-29c-5p von H19 gebunden wird, steigen ATF2- und ECM1-Spiegel an. In Tumorproben und öffentlichen Krebsdatenbanken waren sowohl ATF2 als auch ECM1 in Pankreaskrebs deutlich höher als im normalen Gewebe. Hohe Spiegel dieser Proteine korrelierten mit fortgeschrittenerem Erkrankungsstadium und schlechterem Überleben. In Zell- und Mausexperimenten führten die Reduktion von H19 oder die Erhöhung von miR-29c-5p zu niedrigeren ATF2- und ECM1-Spiegeln, verkleinerten Tumoren und abgeschwächter Invasivität. Die Daten deuten auf eine Kettenreaktion hin: H19 bindet miR-29c-5p, wodurch ATF2 entlastet wird, das wiederum ECM1 hochreguliert und so eine steife, fibrotische Umgebung fördert, die die Tumorausbreitung begünstigt.
Vom Mechanismus zu potenziellen Markern und Therapien
Über die Kartierung dieser Signalkette hinaus prüften die Forschenden, ob diese Moleküle Ärzten bei Diagnose oder Klassifikation von Bauchspeicheldrüsenkrebs helfen könnten. Anhand von Patientendaten stellten sie fest, dass ECM1- und ATF2-Spiegel Tumorgewebe mit hoher Genauigkeit vom normalen Pankreas unterscheiden konnten und in einigen Analysen den üblichen Blutmarker CA19-9 übertrafen. Patienten mit niedrigeren ECM1-Spiegeln in ihren Tumoren lebten tendenziell länger, was darauf hindeutet, dass ECM1 ein Hinweis auf aggressivere Erkrankung sein könnte. Obwohl die klinische Probenmenge an diesem Krankenhaus klein war, stärkt die Konsistenz über unabhängige Datenbanken und Tierexperimente hinweg die Annahme, dass diese Achse zentral für die PDAC-Biologie ist.
Was das für Patienten und künftige Forschung bedeutet
Einfach ausgedrückt zeigt diese Studie, dass eine lange „stille“ RNA, H19, Pankreastumoren dabei unterstützt, zu wachsen und zu invasieren, indem sie eine schützende kleine RNA, miR-29c-5p, neutralisiert und zwei wachstumsfördernde Proteine, ATF2 und ECM1, freisetzt. Diese vierteilige Kette – H19/miR-29c-5p/ATF2/ECM1 – hilft dem Tumor, seine Nachbarschaft in ein unterstützendes Nest umzubauen und steht in engem Zusammenhang mit schlechteren Ergebnissen. Während größer angelegte klinische Studien nötig sind, legen die Ergebnisse nahe, dass die Messung von Komponenten dieses Weges dabei helfen könnte, Hochrisikopatienten zu identifizieren, und dass Medikamente, die H19 oder ECM1 blockieren oder die Aktivität von miR-29c-5p wiederherstellen, eines Tages neue Behandlungsoptionen gegen diesen schwer zu behandelnden Krebs bieten könnten.
Zitation: Rui, M., Xiuping, L., Yu, C. et al. H19 enhances pancreatic cancer proliferation and invasion by reducing miR-29c-5p’s inhibitory effects on ATF2/ECM1. Sci Rep 16, 7623 (2026). https://doi.org/10.1038/s41598-026-37632-6
Schlüsselwörter: Bauchspeicheldrüsenkrebs, nicht-kodierende RNA, H19, Tumormikroumgebung, Biomarker