Clear Sky Science · de
Modell zur Beschreibung der Wechselwirkungen zwischen Ellagitanninen und Fe(II)-Ionen
Warum Pflanzenstoffe im Tierfutter wichtig sind
Antibiotikaresistente Bakterien sind ein wachsendes Problem für Landwirte und die öffentliche Gesundheit. Viele dieser schwer zu behandelnden Keime entstehen in der Nutztierhaltung, wo Antibiotika in Futtermischungen noch immer weit verbreitet sind. Diese Studie untersucht Tannine — natürliche Pflanzenstoffe — als vielversprechende Alternative. Insbesondere erklärt sie, wie eine spezielle Gruppe von Tanninen aus Kastanienholz Eisen auf eine Weise binden kann, die Bakterien möglicherweise eines ihrer lebenswichtigen Nährstoffe entzieht und so ihr Wachstum hemmt.
Natürliche Verteidiger, verborgen in Bäumen
Tannine sind bittere, von Pflanzen gebildete Moleküle, die Rotwein seine Adstringenz verleihen und seit Jahrhunderten beim Gerben von Leder und bei Tinten verwendet werden. Sie kommen in vielen Futtermitteln und Lebensmitteln reichlich vor und sind allgemein als unbedenklich für Tiere und Menschen eingestuft. Manche Typen, die sogenannten Ellagitannine, sind besonders interessant, weil sie zahlreiche kleine chemische „Hände“ besitzen, die an Metallionen wie Eisen andocken können. Kastanienholzextrakt, das bereits in Tierfutter eingesetzt wird, enthält mehrere Ellagitannine, darunter zwei große Vertreter, roburin A und roburin D. Frühere Arbeiten zeigten, dass einfachere Verwandte dieser Verbindungen Eisen binden können und dadurch Bakterien den Zugang zu diesem essentiellen Element erschweren könnten.
Bakterien ihr Lieblingsmetall entziehen
Bakterien können ohne Eisen nicht gedeihen. Sie nutzen es für die Atmung, den Aufbau von DNA und zahlreiche Enzymreaktionen. Im Tierdarm oder in Nährmedien beschaffen sie sich Eisen normalerweise mit eigenen kleinen eisenbindenden Molekülen. Ellagitannine stören diesen Prozess, indem sie enge Komplexe mit Eisenionen bilden und so das Metall für Bakterien „einsperren“. Die Autorinnen und Autoren konzentrierten sich auf Eisen in der Fe(II)-Form, dem Zustand, den Tannine im Wasser rasch einfangen, bevor es langsam zu Fe(III) oxidiert. Durch die Isolierung von roburin A und D aus Kastanienextrakt und deren Untersuchung in kontrollierten Lösungen konnten die Forschenden verfolgen, wie gut diese großen Tannine Eisen aus der Flüssigphase entfernen.
Untersuchung, wie Tannine Eisen fassen
Um die Details zu verstehen, prüften die Forschenden zunächst, wie roburine Protonen aufnehmen und abgeben (ein Prozess der Säure–Base-Gleichgewichte) bei unterschiedlichen pH-Werten. Mithilfe der ultraviolett–sichtbaren Spektroskopie verfolgten sie, wie sich die Lichtabsorption der roburine über verschiedene pH-Bereiche verschob. Diese Verschiebungen zeigten, dass roburin A und D sich ähnlich verhalten wie ihre kleineren Verwandten vescalagin und castalagin, jedoch mit etwa doppelt so vielen Stellen, die ein Proton verlieren und anschließend an der Eisenbindung teilnehmen können. Anschließend mischten sie Tannine und Eisen in verschiedenen Verhältnissen und nutzten erneut die Lichtabsorption, um sogenannte Job-Plots zu erstellen, die das Mischungsverhältnis zeigen, bei dem die Bildung des Eisen–Tannin-Komplexes maximal ist. Aus diesen Daten schlossen sie, dass jedes roburin-Molekül sechs Fe(II)-Ionen binden kann — die doppelte Kapazität der kleineren Ellagitannine.
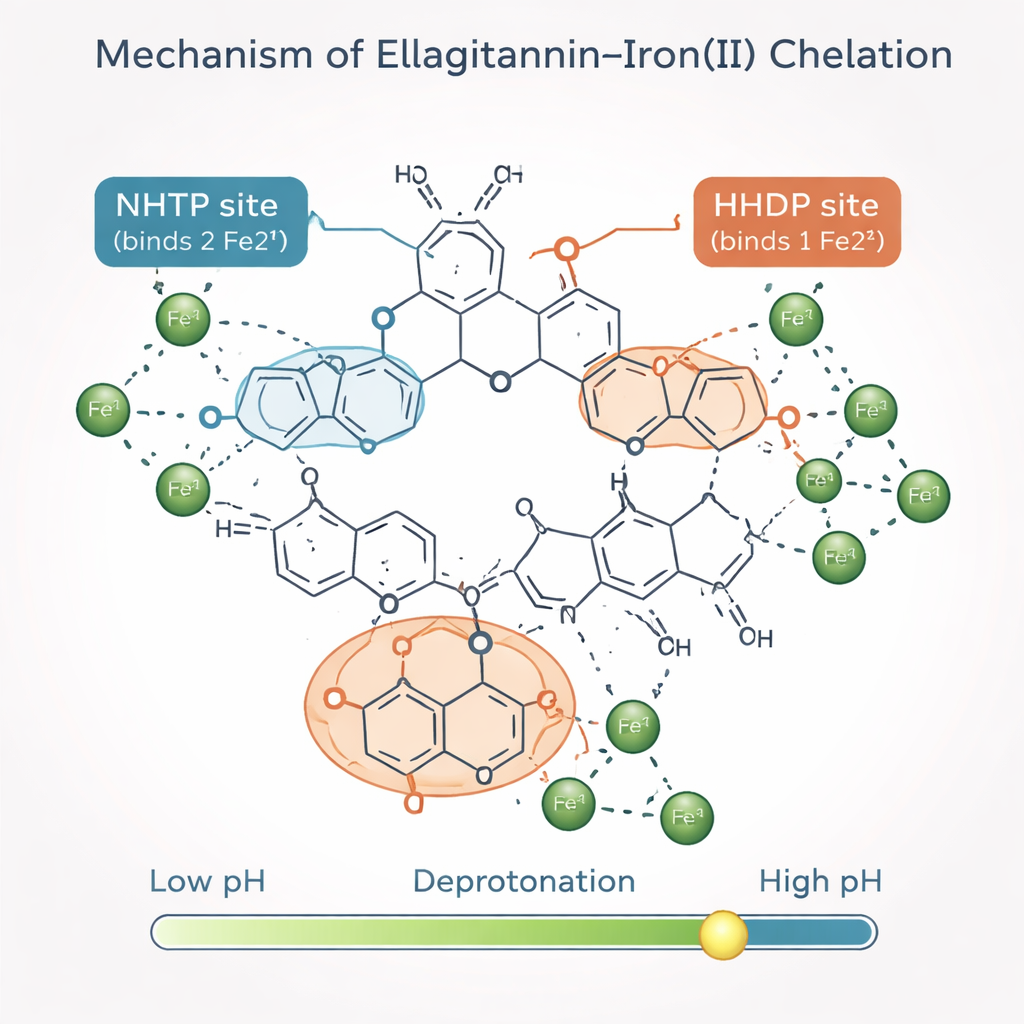
Eine vorhersagende Karte der eisenbindenden Hotspots
Über die bloße Zählung gebundener Eisenionen hinaus wollten die Autorinnen und Autoren wissen, welche strukturellen „Module“ der Ellagitannine die Bindung leisten. Sie entwickelten ein mathematisches Modell, das jedes Ellagitannin-Molekül als Sammlung wiederkehrender Bausteine behandelt. Zwei Schlüsselmodule, genannt NHTP- und HHDP-Gruppen, bieten jeweils spezifische Bindungsstellen für Eisen, sobald sie ihre am leichtesten abzuspaltenen Protonen verloren haben. Durch die Kombination ihrer neuen Messungen mit früheren Kernspinresonanz- und Spektroskopiedaten zeigten sie, dass jede NHTP-Gruppe typischerweise zwei Eisenionen bindet, während jede HHDP-Gruppe eines bindet. Mit nur wenigen anpassbaren Parametern reproduzierte ihr Modell die experimentellen Job-Plots nicht nur für die einfacheren Ellagitannine, sondern auch für die größeren Roburine, die nicht zur Kalibrierung des Modells verwendet wurden.
Folgen für eine umweltfreundlichere Landwirtschaft
Einfach ausgedrückt macht diese Arbeit die komplexe Chemie von Tanninen und Eisen in eine anwendbare Anleitung überführbar. Sie zeigt, dass man durch das Zählen von NHTP- und HHDP-Einheiten in einem Ellagitannin vorhersagen kann, wie viele Eisenionen ein gegebenes Molekül unter leicht sauren Bedingungen fangen wird. Da roburinreiche Kastanienextrakte mehr Eisen binden als kleinere Tannine oder einfache Pflanzensäuren, sind sie starke Kandidaten, um die Eisenzufuhr für schädliche Darmbakterien bei Nutztieren zu begrenzen. Zwar sind weitere Untersuchungen nötig — insbesondere für andere Tanninstrukturen und für Eisen in anderen Formen —, doch kann dieses Modell die Entwicklung und Auswahl pflanzenbasierter Futterzusätze leiten, die den Einsatz konventioneller Antibiotika reduzieren und eine nachhaltigere, „grünere“ Tierproduktion unterstützen.
Zitation: Frešer, F., Hostnik, G. & Bren, U. Model for the description of interactions between ellagitannins and Fe(II) ions. Sci Rep 16, 6631 (2026). https://doi.org/10.1038/s41598-026-37616-6
Schlüsselwörter: Ellagitannine, Eisenchelation, Tannine im Tierfutter, Alternativen zu Antibiotika, Kastanienholzextrakt