Clear Sky Science · de
Computergestützte Identifizierung multi‑target natürlicher Verbindungen aus Sesbania grandiflora als potenzielle Wirkstoffe gegen Klebsiella pneumoniae
Warum ein altes Heilmittel für neue Superkeime wichtig ist
Infektionen mit antibiotikaresistenten Erregern werden zunehmend schwerer zu behandeln; einer der schlimmsten Übeltäter ist ein Krankenhauskeim namens Klebsiella pneumoniae. Wenn dieses Bakterium unsere besten Wirkstoffe überlistet, können Ärzten die Optionen ausgehen. Diese Studie stellt eine hoffnungsvolle Frage: Könnten natürliche Substanzen aus dem traditionellen Heilbaum Sesbania grandiflora (auch bekannt als „Gemüse‑Kolibri“) so weiterentwickelt werden, dass sie als moderne Medikamente mehrere Schwachstellen des Erregers gleichzeitig angreifen?
Ein hartnäckiges Bakterium, das Medikamente austrickst
Klebsiella pneumoniae verursacht schwere Erkrankungen wie Lungenentzündung, Harnwegsinfektionen, Sepsis und Meningitis, insbesondere bei Menschen mit geschwächtem Immunsystem. In den letzten zehn Jahren haben viele Stämme selbst gegenüber Carbapenemen Resistenzen entwickelt, Antibiotika, die meist als „letzte Rettung“ aufbewahrt werden. Das Bakterium verteidigt sich durch den Abbau von Wirkstoffen, aktives Herunterpumpen von Antibiotika, Versiegelung der Außenmembran und Bildung schützender Biofilme. Weil es gleichzeitig viele verschiedene Strategien nutzt, ist ein Einzelzielwirkstoff leicht zu umgehen. Die Autorinnen und Autoren argumentieren, dass es wirkungsvoller ist, mehrere lebenswichtige Prozesse gleichzeitig zu blockieren, was es dem Keim deutlich schwerer macht, Resistenzen zu entwickeln.
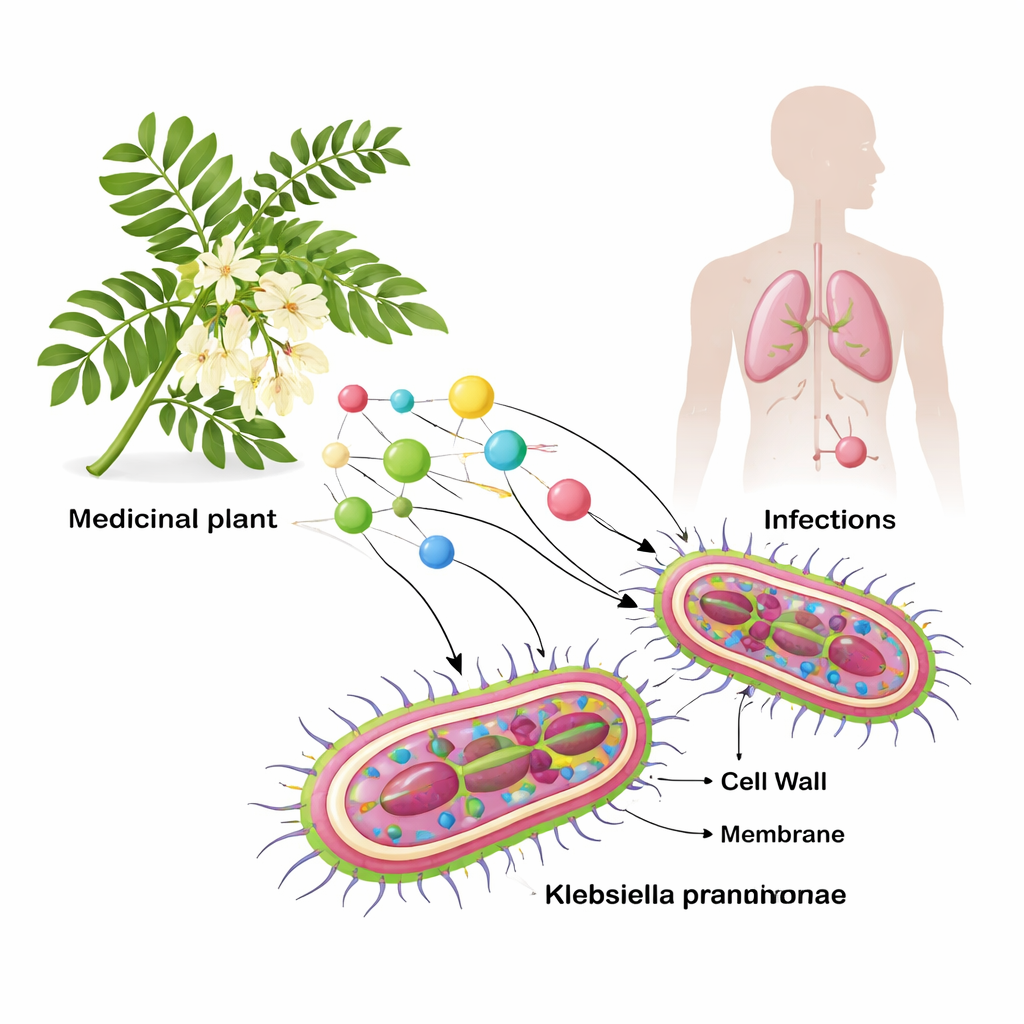
Auf der Suche nach Hinweisen in einem Heilbaum
Sesbania grandiflora hat eine lange Tradition in der Volksmedizin und zeigte Aktivität gegen verschiedene krankheitserregende Mikroben. Statt Pflanzenextrakte direkt im Labor zu testen, nutzten die Forschenden Computer für ein groß angelegtes virtuelles Screening. Zuerst durchsuchten sie das komplette Proteom von Klebsiella und reduzierten die Liste mithilfe strenger Qualitäts‑ und Literaturfilter auf sechs besonders wichtige bakterielle Komponenten. Dazu gehören Enzyme, die für den Aufbau von Außenhülle und Zellwand nötig sind, ein Resistenzenzym, das starke Antibiotika zerstört, und ein Strukturprotein, das dem Bakterium hilft, mit menschlichen Zellen zu interagieren. Parallel sammelten sie 73 bekannte Pflanzenstoffe aus S. grandiflora und erstellten dreidimensionale Modelle sowohl der Verbindungen als auch der bakteriellen Zielproteine.
Pflanzenstoffe finden, die viele Ziele treffen
Das Team nutzte Molekulardocking, eine Methode, die vorhersagt, wie gut sich jedes Pflanzenmolekül in die Taschen der bakteriellen Proteine einfügen könnte. Die meisten getesteten Verbindungen konnten an allen sechs Zielen mit günstiger vorhergesagter Stärke andocken, und eine kleinere Gruppe zeigte besonders starke Bindungen. Eine Netzwerkanalyse ergab, dass drei Ziele — FabG, KPC‑2 und OmpA — mit fast allen Verbindungen verknüpft waren, was auf eine breite Abdeckung hindeutet. Anschließend wendeten die Forschenden gängige Regeln zur Arzneimittelähnlichkeit sowie computergestützte Modelle zu Absorption und Toxizität an, um Moleküle auszufiltern, die wahrscheinlich nicht sicher oder wirksam im Körper wären. Dieser Auswahlprozess reduzierte die Liste auf neun vielversprechende Kandidaten, von denen viele gemeinsame Strukturmerkmale aufwiesen — etwa ringförmige Kerne und mehrere sauerstoffreiche Gruppen —, die stabile Kontakte zu Proteinen begünstigen.
Fokussiert auf einen Spitzenkandidaten
Unter diesen neun stach eine Verbindung, Sonchuionoside A, hervor, weil sie stark an alle sechs bakteriellen Ziele dockte und gleichzeitig die Sicherheits‑ und Nutzbarkeitsfilter erfüllte. Um die Robustheit dieser Interaktionen zu prüfen, führten die Autorinnen und Autoren lange Molekulardynamik‑Simulationen durch, bei denen sie im Grunde beobachteten, wie sich jeweils das Protein und die Verbindung über Hunderte von Nanosekunden in einer virtuellen Wasserumgebung gemeinsam bewegen. In allen sechs Zielproteinen blieb Sonchuionoside A gebunden, ohne die Proteinstabilität zu stören, und sorgte oft dafür, dass die Proteine etwas kompakter und geordneter wurden. Detaillierte Analysen der Bewegung, der Oberflächenexposition, der Wasserstoffbrücken und der geschätzten Bindungsenergien deuteten auf besonders starke und günstige Interaktionen mit zwei Enzymen hin, die am Aufbau essentieller Zellkomponenten beteiligt sind (LpxH und FabG), sowie auf solide Bindungen zum Resistenzenzym KPC‑2 und zum Außenmembranprotein OmpA.
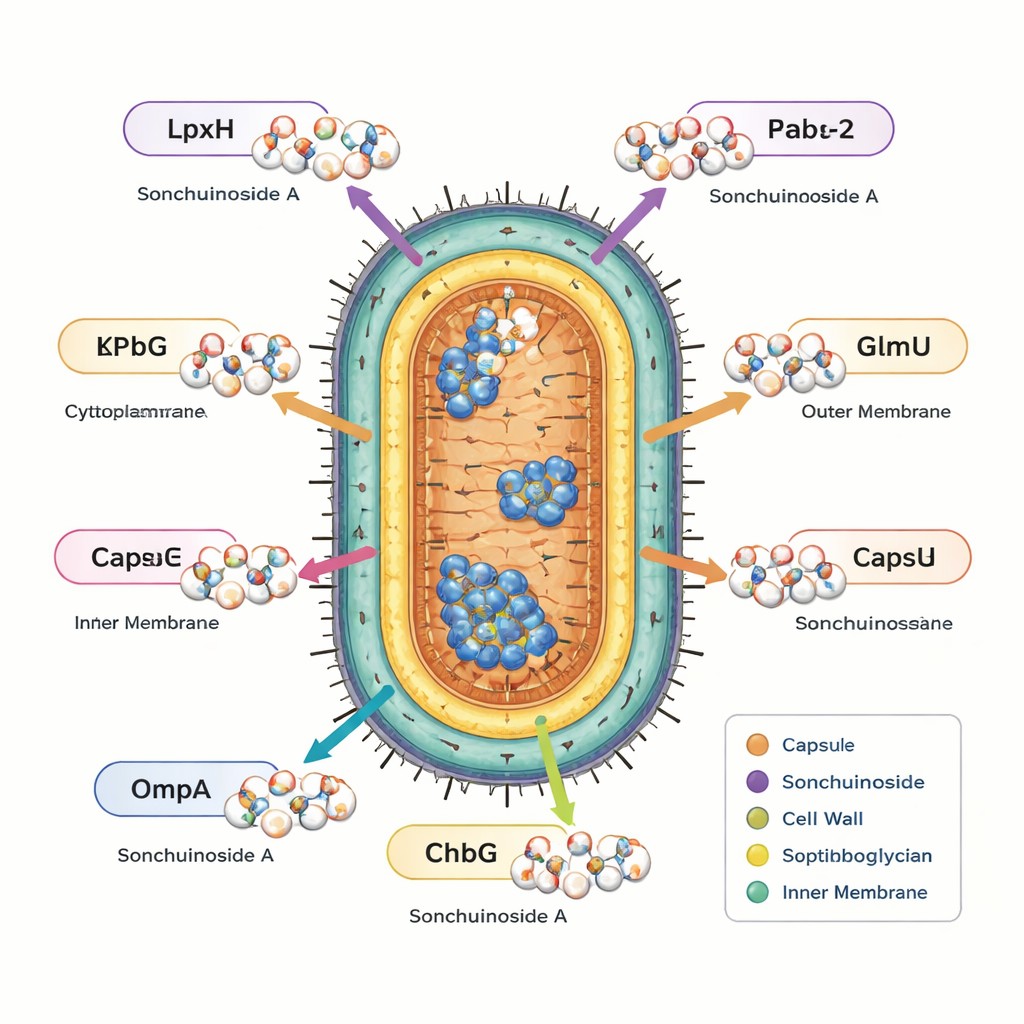
Was das für künftige Behandlungen bedeuten könnte
Diese Forschung liefert noch kein sofort einsetzbares Medikament, und alle Ergebnisse stammen aus Computer‑Modellen statt aus Tier‑ oder Humanstudien. Dennoch bietet sie eine überzeugende Roadmap. Die Arbeit zeigt, dass eine einzelne Pflanzenverbindung wie Sonchuionoside A so weiterentwickelt werden könnte, dass sie Klebsiella pneumoniae auf mehreren Fronten angreift — die Zellabwehr schwächt, die Resistenzmechanismen untergräbt und die Fähigkeit, Krankheit zu verursachen, abschwächt. Einfach gesagt legt die Studie nahe, dass ein traditioneller Heilbaum Inspiration für zukünftige mehrgleisige Antibiotika liefern könnte, mit denen Ärztinnen und Ärzte gefährlichen, medikamentenresistenten Infektionen einen Schritt voraus bleiben können.
Zitation: Sajal, H., Mohan, A., Ravi, V. et al. Computational identification of multi-target natural compounds from Sesbania grandiflora as potential therapeutic agents against Klebsiella pneumoniae. Sci Rep 16, 7782 (2026). https://doi.org/10.1038/s41598-026-37613-9
Schlüsselwörter: Antibiotikaresistenz, Klebsiella pneumoniae, Heilpflanzen, natürliche Verbindungen, Multi‑Target‑Medikamente