Clear Sky Science · de
LIMK2-Inaktivierung unterdrückt mechanisch induzierte Differenzierung dermaler Fibroblasten und die Resistenz gegen Apoptose
Warum manche Narben außer Kontrolle geraten
Die meisten Schnitte und chirurgischen Wunden hinterlassen eine dünne, flache Linie. Bei manchen Menschen läuft der Heilungsprozess jedoch auf Hochtouren und es entstehen dicke, erhabene Narben, sogenannte hypertrophe Narben oder Keloide, die jucken, schmerzen und die Bewegung einschränken können. Diese Studie untersucht, warum gewöhnliche Hautzellen manchmal zu übertriebenen Narbenbildnern werden, und zeigt auf einen einzelnen molekularen Schalter namens LIMK2, der heruntergeregelt werden könnte, um ein unkontrolliertes Narbenwachstum zu verhindern.
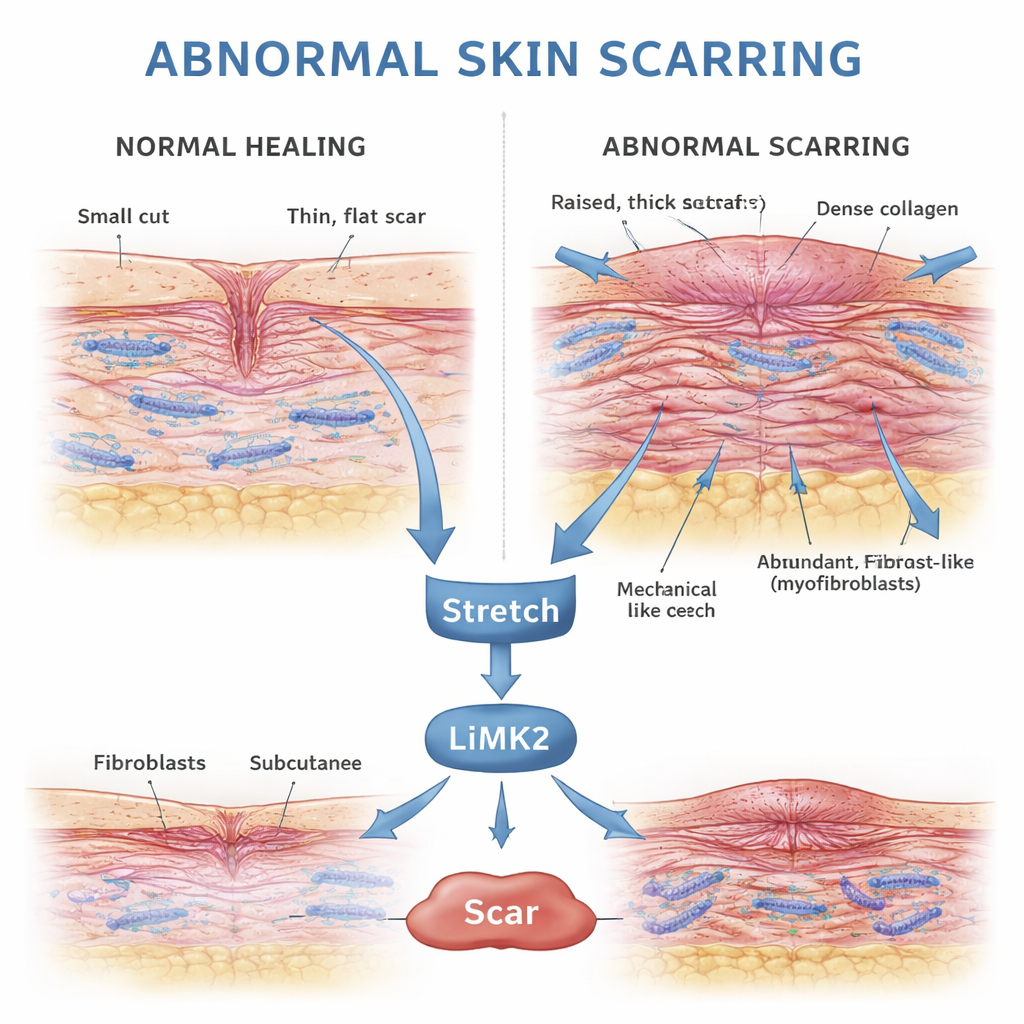
Wie die Haut nach einer Verletzung normalerweise heilt
Bei Hautverletzungen startet der Körper ein zeitlich abgestimmtes Reparaturprogramm. Fibroblasten — die Aufbauarbeiter der tieferen Hautschicht — wandern in die Wunde, vermehren sich und legen Kollagen ab, das Proteingerüst des neuen Gewebes. Viele dieser Fibroblasten wandeln sich vorübergehend in eine stärkere, kontraktilere Form um, die als Myofibroblasten bezeichnet wird und dabei hilft, die Wundränder zusammenzuziehen. Sobald die Oberfläche geschlossen und das neue Gewebe stabilisiert ist, sollen diese Myofibroblasten durch einen kontrollierten Prozess namens Apoptose absterben, sodass eine maßvolle, flexible Narbe zurückbleibt.
Wenn alltägliche Kräfte Narben verschlimmern
Abnorme Narben treten häufig an Stellen auf, an denen die Haut ständig gedehnt wird — über Brust, Schultern oder Unterbauch. Diese Beobachtung ließ Forscher vermuten, dass mechanische Kräfte wie Ziehen und Spannung über eine heilende Wunde Fibroblasten dazu bringen können, zu lange aktiv zu bleiben. Frühere Arbeiten zeigten, dass Dehnen dieser Zellen im Labor das Protein α-SMA erhöht, ein Kennzeichen von Myofibroblasten, und Gene anschaltet, die den Zellen helfen, der Apoptose zu widerstehen. Die neue Studie konzentriert sich auf LIMK2, einen wichtigen Bestandteil einer mechanischen Signalgebungskette innerhalb der Zelle, die physikalische Dehnung mit Veränderungen im inneren Gerüst aus Aktinfilamenten verbindet.
Ein zentraler Schalter für narbenbildende Zellen
Um die Rolle von LIMK2 zu prüfen, verwendeten die Forscher humane dermale Fibroblasten aus normaler Haut und aus Keloidgewebe. Sie führten in einige Zellen eine deaktivierte Version von LIMK2 ein, ließen andere unverändert oder gaben ihnen eine immer aktive Version als Kontrolle. Wenn die Zellen mechanisch gedehnt wurden, reagierten normale Fibroblasten wie erwartet: ein rascher Anstieg phosphorylierter Cofilin-Werte und stärkere Aktinfasern, erhöhte α-SMA-Werte, mehr Kollagenproduktion und höhere Spiegel von Bcl-2, einem Protein, das vor Zelltod schützt, begleitet von niedrigeren Werten des pro-apoptotischen Proteins BAX. Im auffälligen Kontrast veränderten sich Fibroblasten mit inaktivem LIMK2 unter Dehnung kaum. Sie steigerten α-SMA nicht, erhöhten den schützenden Bcl-2-Wert nicht und verringerten BAX nicht, und zeigten weniger Kollagen. Diese Zellen kontrahierten auch Kollagengele schwächer und krabbelten in einem wundenähnlichen Test langsamer, was auf geringere Zugkraft und verminderte Fähigkeit hinweist, umliegendes Gewebe zu durchdringen.
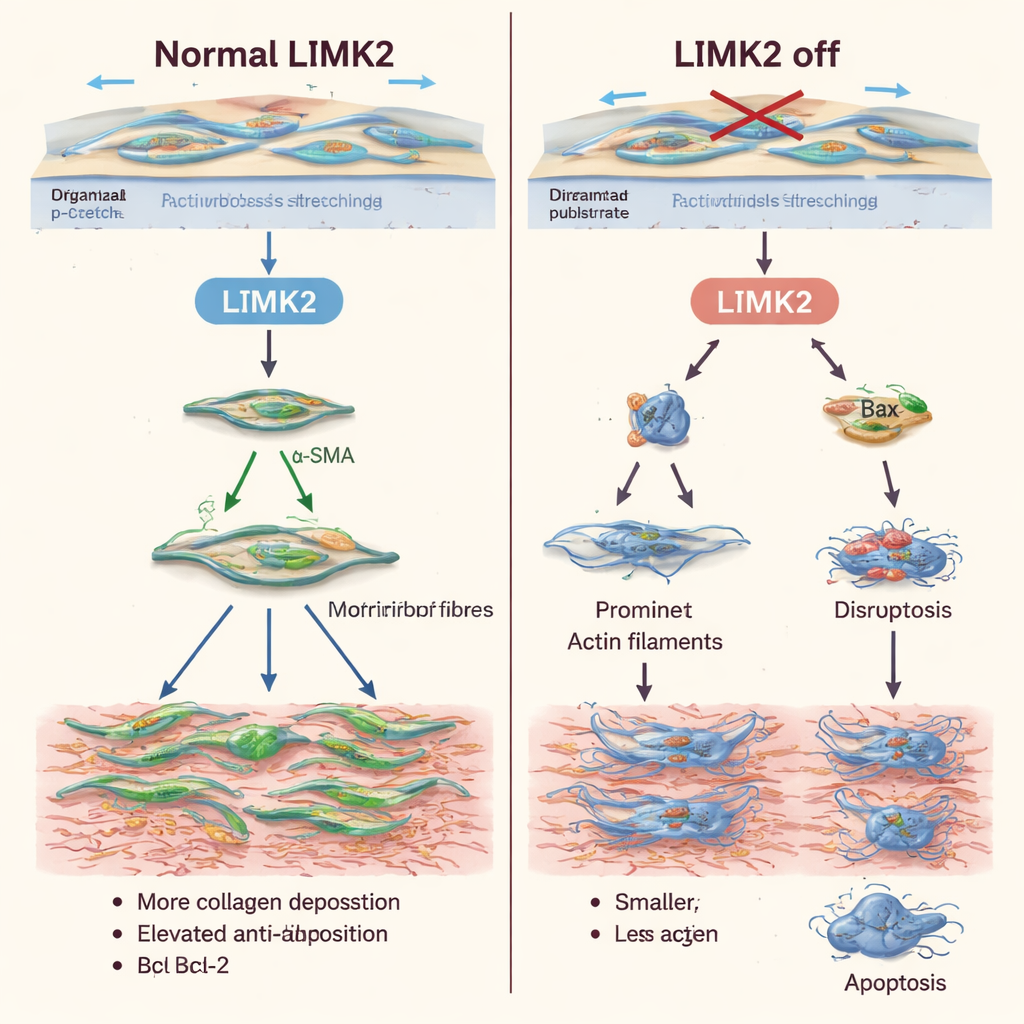
Hartnäckigere Narbenzellen leichter entfernbar machen
Über die veränderte Reaktion auf Dehnung hinaus machte das Abschalten von LIMK2 die Zellen anfälliger für Tod und weniger teilungsfreudig. Zellen mit inaktivem LIMK2 zeigten höhere Ausgangslevel an Apoptose, und mechanische Dehnung — normalerweise ein Überlebenssignal — schützte sie nicht mehr. Durchflusszytometrie und fluoreszierende Färbungen bestätigten, dass mehr Zellen sich in frühen oder späten Stadien des programmierten Zelltods befanden. Gleichzeitig zeigten Zellzählungen und DNA-Markierungstests, dass sich diese Zellen deutlich seltener teilten als normale Zellen. Ähnliche Muster traten auf, wenn das Team Latrunculin A einsetzte, ein Medikament, das Aktinfilamente stört, was die Idee stützt, dass LIMK2 hauptsächlich durch Steuerung des inneren Zellgerüsts wirkt.
Was das für künftige Narbenbehandlungen bedeuten könnte
Die Ergebnisse deuten darauf hin, dass LIMK2 an einer Weggabelung sitzt, an der mechanische Kräfte, Zellüberleben und narbenbildende Aktivität zusammentreffen. Ist LIMK2 aktiv, treibt Dehnung Fibroblasten in einen robusten, persistenten Myofibroblasten-Zustand: Sie kontrahieren stark, widerstehen dem Tod und produzieren zusätzliches Kollagen — Faktoren, die dicke, erhabene Narben begünstigen. Das Ausschalten von LIMK2 kehrt vieles davon um — Fibroblasten werden weniger kontraktil, weniger mobil, weniger proliferativ und eher bereit, Apoptose zu durchlaufen. Für Patientinnen und Patienten deutet dies auf eine Zukunft hin, in der Cremes, Injektionen oder Verbände, die LIMK2 oder dessen nachgeschaltete Aktinveränderungen sanft blockieren, helfen könnten, dass Wunden mit flacheren, komfortableren Narben heilen.
Zitation: Ishii, M., Kuroda, K., Otani, N. et al. LIMK2 inactivation suppresses mechanical stimulation-induced dermal fibroblast differentiation and resistance to apoptosis. Sci Rep 16, 7453 (2026). https://doi.org/10.1038/s41598-026-37610-y
Schlüsselwörter: Keloidnarben, Wundheilung, Fibroblasten, mechanische Spannung, Apoptose