Clear Sky Science · de
SMAD2-Ubiquitinierung über das PY-Motiv reguliert die Skelettmuskulatur und fibrotische Degeneration
Warum diese Muskelstudie wichtig ist
Mit dem Alter merken viele von uns, dass Muskeln schwächer und kleiner werden, und bei chronischer Krankheit oder Verletzung kann Muskelgewebe allmählich durch steifes Narbengewebe ersetzt werden. Diese Studie geht einer grundlegenden Frage hinter diesen Veränderungen nach: Wie verhindern Muskelzellen, dass ein stark wachstumshemmendes Signal, genannt TGF‑beta, über das Ziel hinausschießt und Muskelschwund sowie Fibrose (Narbenbildung) verursacht? Indem sie einen winzigen eingebauten „Ausschalter“ in einem zentralen TGF‑beta‑Protein aufdecken, zeigen die Autoren einen neuen Mechanismus, der hilft, Muskelmasse und gesunde Gewebestruktur zu bewahren.
Eine eingebaute Bremse für ein starkes Signal
TGF‑beta ist ein Signalmolekül, das Zellen sagt, wann sie das Wachstum verlangsamen, ihre Identität ändern oder Bindegewebe produzieren sollen. Im Skelettmuskel führt zu viel TGF‑beta zu schrumpfenden Fasern und fördert Fibrose; zu wenig kann die normale Wachstumssteuerung stören. Innerhalb der Zellen wirkt TGF‑beta hauptsächlich über das Relay‑Protein SMAD2. Nachdem TGF‑beta an seine Rezeptoren an der Zelloberfläche gebunden hat, wird SMAD2 aktiviert und wandert in den Zellkern, um die Genaktivität zu verändern. Damit dies nicht dauerhaft wird, markieren Zellen SMAD2 chemisch mit kleinen Ubiquitin‑Molekülen, die seinen Abbau einleiten. Eine kurze Sequenz in SMAD2, das sogenannte PY‑Motiv, ist die Andockstelle für Enzyme, die diese Ubiquitin‑Anhänge anbringen. Die Forscher fragten: Wenn diese Andockstelle in einem lebenden Tier entfernt wird, versagt dann die SMAD2‑Bremse, und was passiert mit den Muskeln im Laufe der Zeit?
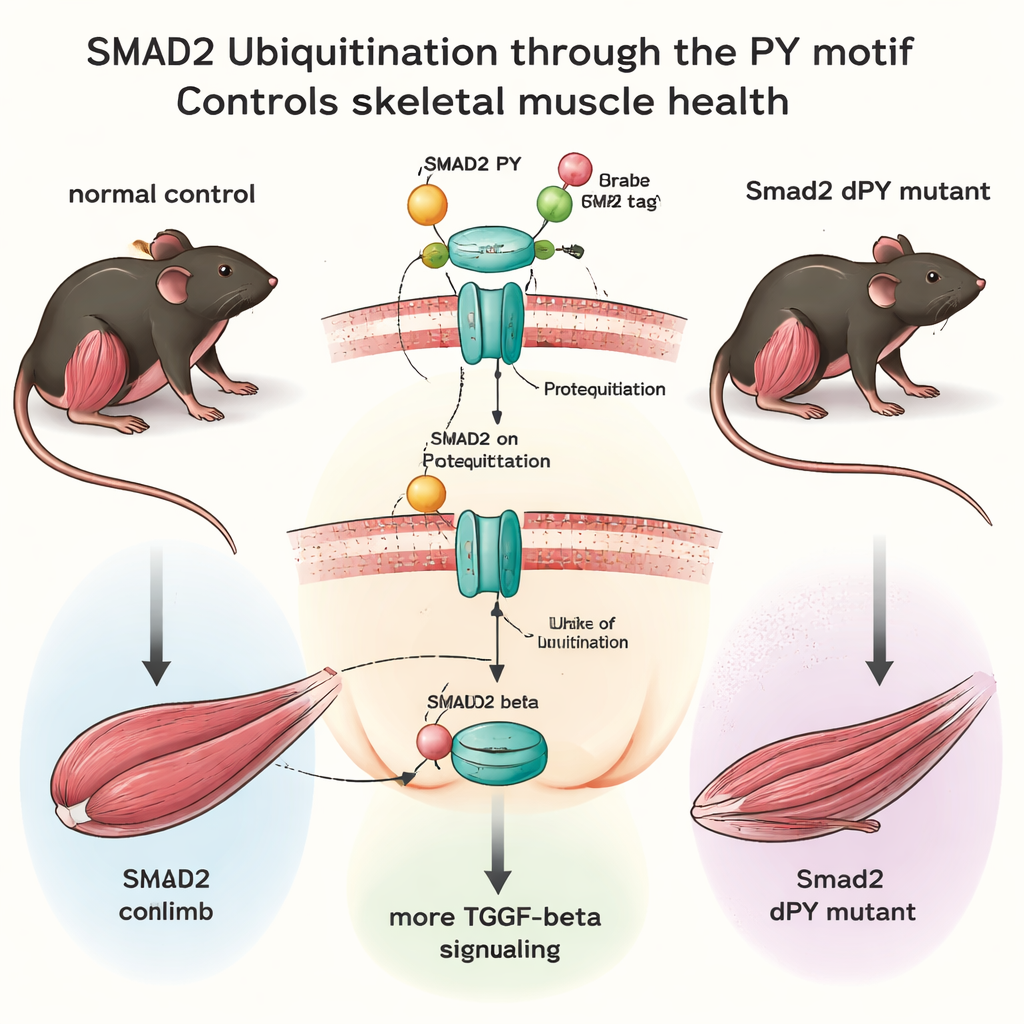
Mäuse mit fehlendem Sicherheitstag konstruieren
Mithilfe moderner Genom‑Editierungstools erzeugte das Team Mäuse, bei denen nur 15 DNA‑„Buchstaben“ aus dem Smad2‑Gen entfernt wurden, wodurch das PY‑Motiv präzise entfernt wurde, ohne den Rest des Proteins zu stören. Diese Smad2dPY‑Mäuse wurden normal geboren, wuchsen bis ins Erwachsenenalter und waren fruchtbar, was zeigt, dass dieses Feinsteuerungssystem unter Standardlaborkonditionen nicht essentiell für die grundlegende Entwicklung ist. Bei genauerer Untersuchung ihrer Muskeln zeigte sich jedoch ein anderes Bild. Junge erwachsene Mäuse wiesen nur subtile Veränderungen auf, aber mit 12 Monaten — etwa mittleres Alter für eine Maus — wogen die großen Hinterbeinmuskeln weniger und einzelne Fasern waren im Vergleich zu normalen Nestlingen kleiner. Im Inneren dieser Muskeln lagen die SMAD2‑Proteinspiegel höher, während seine Ubiquitinierung reduziert war, was bestätigt, dass das fehlende PY‑Motiv SMAD2 stabiler und weniger abbaubar machte.
Überempfindliche Muskelzellen und stockende Reparatur
Um zu verstehen, was das auf zellulärer Ebene bedeutet, isolierten die Forscher Muskelvorläuferzellen (Myoblasten) aus den mutanten Mäusen. Bei Exposition gegenüber TGF‑beta in der Kultur zeigten diese Myoblasten eine stärkere Aktivierung von SMAD2 und eine stärkere Induktion TGF‑beta‑responsiver Gene als Zellen aus normalen Mäusen. Gleichzeitig war ihre Fähigkeit, zu langen, mehrkernigen Muskelfasern zu fusionieren — ein zentraler Schritt für Muskelwachstum und Regeneration — beeinträchtigt. Ähnliche Veränderungen wurden in Fibroblasten beobachtet, den Bindegewebszellen zwischen den Muskelfasern: Mutante Fibroblasten reagierten stärker auf TGF‑beta und exprimierten eher Gene, die mit narbenbildenden Myofibroblasten in Verbindung stehen. Zusammen deuten diese Befunde darauf hin, dass ohne das PY‑Motiv sowohl muskelbildende Zellen als auch Stützzellen gegenüber TGF‑beta hypersensitiv werden und das Gleichgewicht zugunsten kleinerer Fasern und verstärkter Bindegewebsbildung kippt.
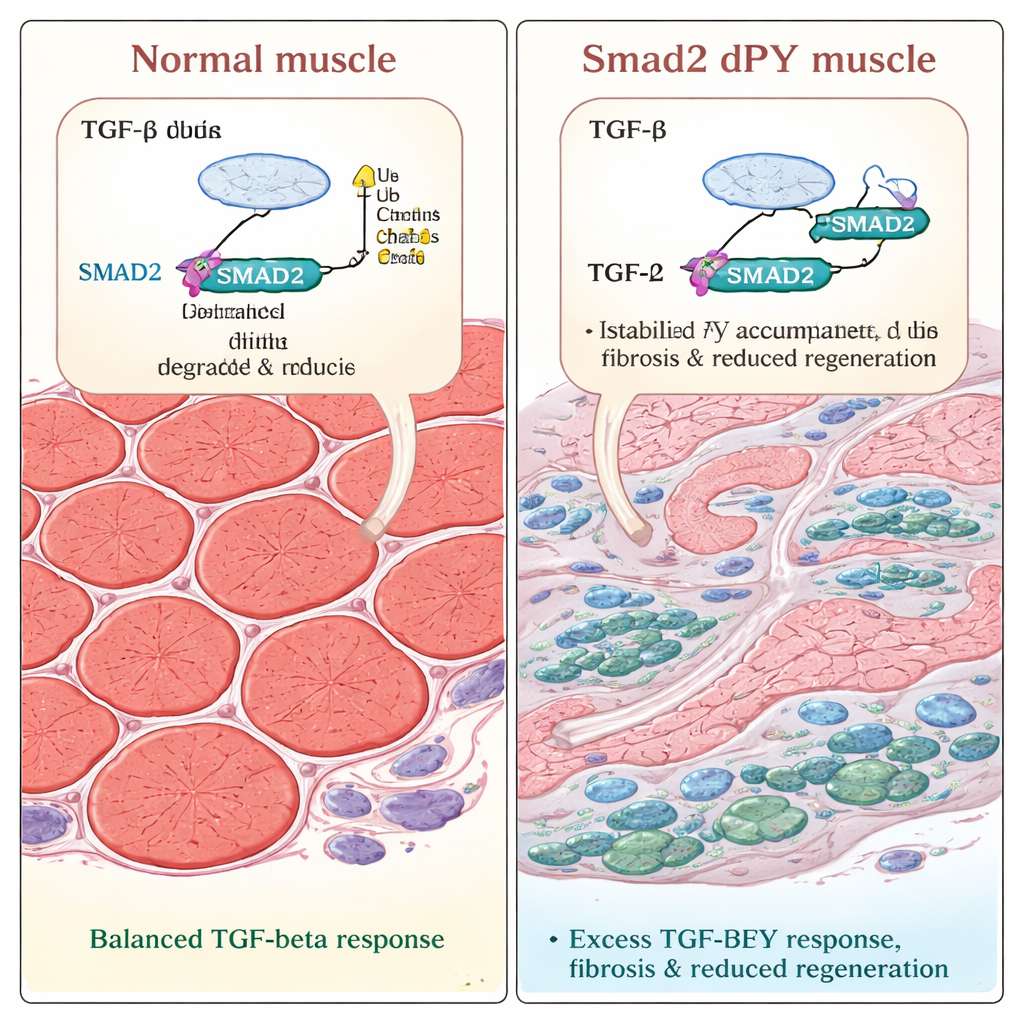
Bei Verletzung gewinnt die Narbenbildung
Das Team prüfte dann, wie diese veränderten Muskeln mit Schäden umgehen. Sie injizierten ein Toxin in Beinmuskeln, um Verletzung und Reparatur auszulösen — ein gut etabliertes Modell der Regeneration. Sowohl bei normalen als auch bei mutanten Mäusen brachen geschädigte Fasern zunächst auseinander und begannen dann nachzuwachsen. Aber drei Wochen nach der Verletzung waren die regenerierten Fasern bei den Smad2dPY‑Mäusen deutlich dünner. Die Mikroskopie zeigte größere Bereiche, die mit Kollagen gefüllt waren, dem Hauptbestandteil von Narbengewebe, und eine erhöhte Zahl alpha‑glattmuskel‑Aktin‑positiver Myofibroblasten, Zellen, die zur Fibrose beitragen. Diese Ergebnisse zeigen, dass wenn SMAD2 nicht richtig markiert und abgebaut werden kann, der Reparaturprozess verzerrt ist: Statt starkes Muskelgewebe vollständig wiederherzustellen, heilt das Gewebe mit überschüssiger Narbenbildung und verringerter Kontraktilmasse.
Was das für die Muskelgesundheit bedeutet
Für Nicht‑Fachleute lautet die Hauptbotschaft: Ein sehr kleines molekulares Merkmal — das PY‑Motiv auf SMAD2 — wirkt als stille, aber wichtige Schutzvorrichtung im Skelettmuskel. Es ermöglicht den Zellen, TGF‑beta‑Signalgebung herunterzuregeln, indem es den Abbau von SMAD2 fördert, wodurch normale Muskelgröße erhalten und Fibrose begrenzt wird, insbesondere da TGF‑beta‑Spiegel mit Alter oder chronischen Verletzungen natürlicherweise ansteigen. Wenn diese Schutzvorrichtung bei Mäusen deaktiviert wird, werden Muskeln im Laufe der Zeit kleiner und narbenanfälliger und erholen sich nach Schäden nicht vollständig. Obwohl diese Arbeit noch an Tieren durchgeführt wurde, macht sie die Ubiquitinierung von SMAD2 zu einem potenziellen Zielweg für künftige Strategien, die darauf abzielen, Muskelmasse zu erhalten und fibrotische Degeneration im Alter oder bei Krankheit zu verhindern.
Zitation: Yamasaki, Y., Sakamoto, K., Yashiro, S. et al. SMAD2 ubiquitination through PY motif regulates skeletal muscle mass and fibrotic degeneration. Sci Rep 16, 6666 (2026). https://doi.org/10.1038/s41598-026-37582-z
Schlüsselwörter: Skelettmuskel, TGF-beta-Signalgebung, SMAD2, Ubiquitinierung, Fibrose