Clear Sky Science · de
Veränderungen der EGFR-Aktivität nach CRISPR/Cas9‑Bearbeitung der EGF-Bindedomäne
Warum das Umlenken eines Krebs‑Signals wichtig ist
Gebärmutterhalskrebs hängt häufig von einem kraftvollen Wachstumsschalter ab, dem epidermalen Wachstumsfaktor‑Rezeptor (EGFR). Viele Tumoren tragen sehr große Mengen dieses Rezeptors, doch Medikamente, die darauf zielen, ihn zu blockieren, haben nur einem Teil der Patienten geholfen. Diese Studie stellte eine grundlegende Frage mit wichtigen Therapie‑Implikationen: Was passiert, wenn man die Fähigkeit von EGFR, sein bevorzugtes Wachstumssignal — den epidermalen Wachstumsfaktor (EGF) — zu binden, entfernt, ohne den Rezeptor selbst zu entfernen?
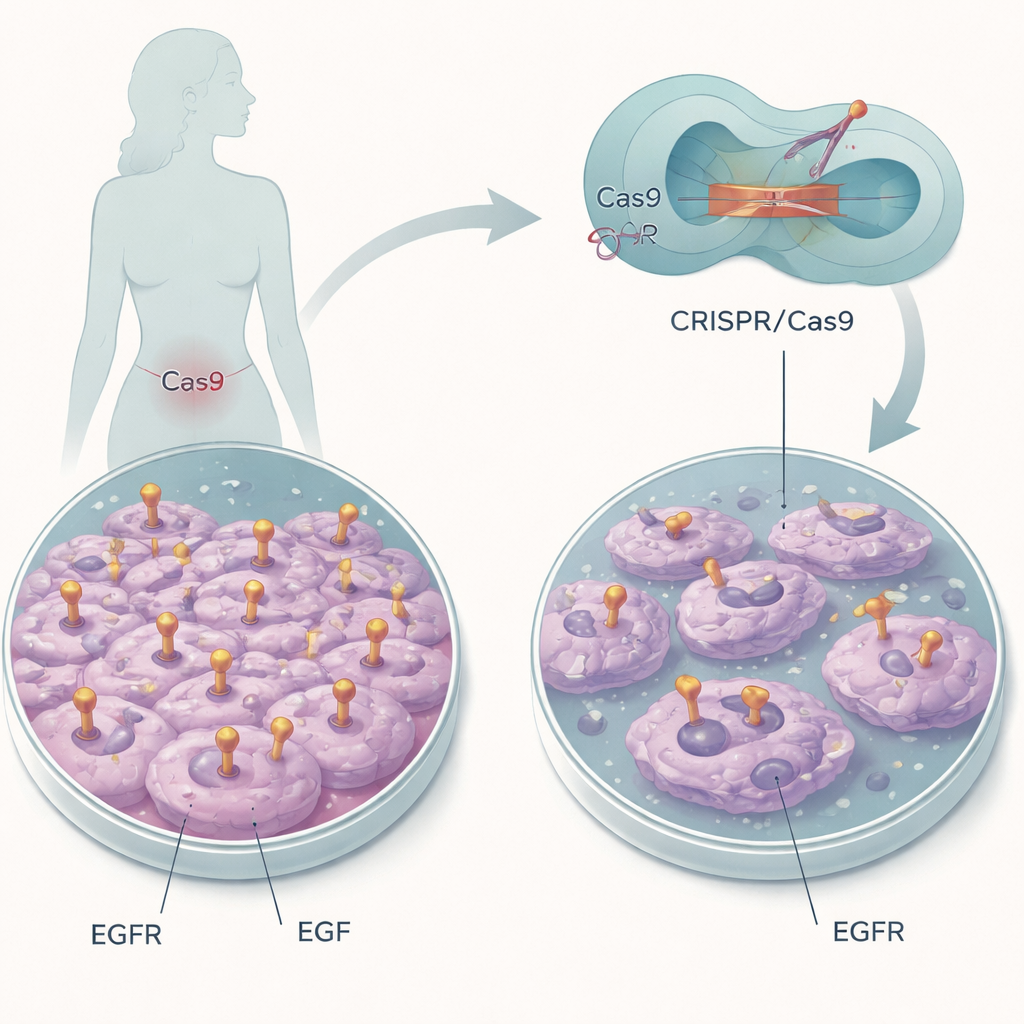
Ein molekularer „Ein‑Schalter“ wird ausgeschaltet
Die Forschenden konzentrierten sich auf eine Zelllinie von Gebärmutterhalskrebs, die große Mengen ansonsten normaler EGFR exprimiert. Anstatt das Gen zu zerstören, nutzten sie CRISPR/Cas9‑Genomeditierung als molekularen Skalpell, um nur wenige Aminosäuren in der EGF‑Bindetasche von EGFR zu verändern. Zwei Stellen, bezeichnet als L14 und Y45, helfen EGF, am Rezeptor anzudocken. Durch den Austausch dieser Bausteine gegen andere beabsichtigte das Team, EGFR im Zellbestand zu belassen, es aber gegenüber EGF blind zu machen, sodass die Rolle dieser einzelnen Interaktion im Verhalten der Krebszellen isoliert werden konnte.
Designer‑Krebszelllinien erzeugen
Im ersten Schritt testete das Team diese Mutationen in Zellen mittels Plasmiden, die vorübergehend entweder normales oder verändertes EGFR produzierten. Fluoreszenzmarkiertes EGF zeigte, dass alle Mutanten deutlich weniger Ligand binden als der normale Rezeptor, besonders wenn sowohl L14 als auch Y45 gemeinsam verändert wurden. Anschließend führten die Forschenden diese Veränderungen direkt in das Genom der Krebszellen mit CRISPR/Cas9 ein und erzeugten mehrere neue Zellklone. Einige trugen eine einzelne Mutation, andere die doppelte Mutation auf einer EGFR‑Kopie und inaktivierende Veränderungen auf der zweiten. Computerbasierte Modellierung der resultierenden Proteinstrukturen zeigte, dass diese Alterationen die Bindungsstelle so verzerrten, dass das Andocken von EGF abgeschwächt oder aufgehoben wurde, was mit den Bindungstests übereinstimmte.
Der Rezeptor bewegt sich — die Zellen überleben
Detaillierte Bildgebung offenbarte, dass sich die editierten Rezeptoren innerhalb der Zelle sehr unterschiedlich verhielten. In unveränderten Krebszellen sitzt EGFR auf der Zelloberfläche, fängt EGF ein und bewegt sich dann nach innen, während es durch Phosphorylierung chemisch aktiviert wird. In Klonen mit der Doppelmutation verschwand die EGF‑Bindung faktisch und EGFR war nicht mehr an der Membran zu sehen; stattdessen sammelte sich die geringe verbleibende Rezeptormenge im Zellinneren an. Selbst eine einzelne Y45‑Veränderung verringerte die Bindung deutlich und senkte die Gesamtmenge an EGFR. Dennoch blieben die Krebszellen trotz dieser Störung der klassischen EGF–EGFR‑Signalroute lebensfähig und wuchsen in Kultur weiter, mit nur moderaten Veränderungen ihrer Zellzyklusrhythmen.
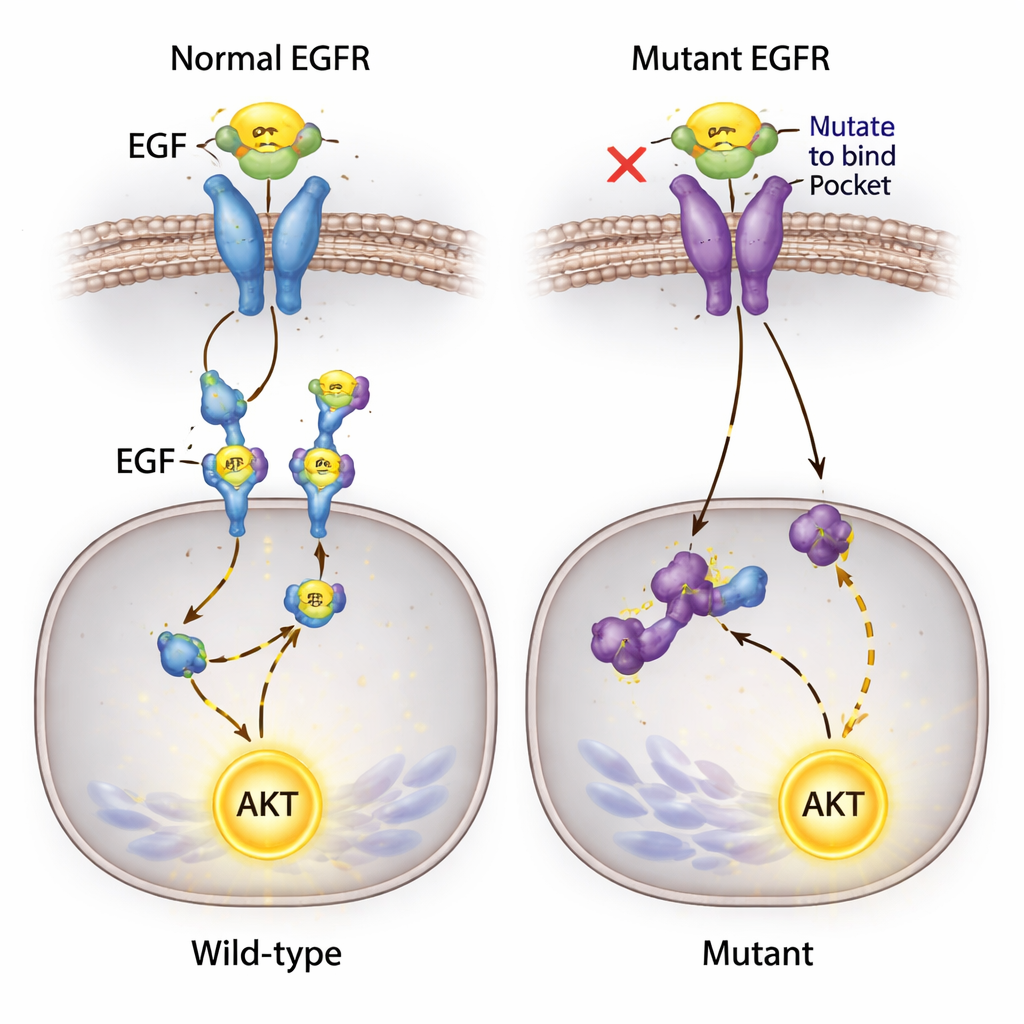
Ein hartnäckiges Signal, das nicht aufhört
Eines der überraschendsten Ergebnisse betraf AKT, ein zentrales Protein, das Überleben fördert und üblicherweise stromabwärts von EGFR aktiviert wird. Die Forschenden erwarteten, dass das Blockieren von EGF–EGFR‑Bindung diesen Pfad zum Schweigen bringen würde. Stattdessen wurde AKT beim Hinzufügen von EGF zum Medium in allen Zelllinien stark aktiviert — auch in solchen, in denen EGF nicht mehr an EGFR binden konnte und in denen Rezeptor‑Phosphorylierung nicht nachweisbar war. Da diese Zellen bereits eine bekannte Mutation in einem anderen Signalgen, PIK3CA, tragen, vermutet das Team, dass alternative Routen existieren, die es EGF erlauben, zur AKT‑Aktivierung beizutragen, möglicherweise über andere Oberflächenproteine oder Hintergrundmutationen und damit am editierten EGFR vorbei.
Verborgene genetische Veränderungen und künftige Therapien
Um sicherzustellen, dass CRISPR keine weitreichenden unbeabsichtigten Schnitte verursachte, sequenzierten die Wissenschaftler das gesamte Genom der neuen Zelllinien. Sie bestätigten, dass die gewünschten EGFR‑Mutationen vorhanden waren, und fanden keine Hinweise auf Schnitte an vorhergesagten Off‑Target‑Stellen der CRISPR‑Leitfäden. Allerdings entdeckten sie zahlreiche spontane Mutationen, verteilt über das Genom, von denen einige das Zellverhalten beeinflussen könnten. Das unterstreicht, dass selbst wenn CRISPR die beabsichtigte Zielstelle trifft, die naturgemäße Instabilität der DNA von Krebszellen die Interpretation experimenteller Ergebnisse und die Entwicklung präziser gentherapeutischer Ansätze verkomplizieren kann.
Was das für Patientinnen und Patienten bedeutet
Für Laien lautet die Kernbotschaft: Das einfache Blockieren des Handschlags zwischen EGF und EGFR — selbst sehr präzise auf atomarer Ebene — stoppt nicht automatisch die «Wachstums‑und‑Überleben»-Signale in Krebszellen. Die Studie zeigt, dass Krebszellen Schlüsselpfade wie die AKT‑Aktivierung umleiten können, wenn ein Rezeptor blockiert ist, und dass CRISPR‑Bearbeitungen in solchen instabilen Genomen sorgfältig bewertet werden müssen. Diese konstruierten Zelllinien bieten jetzt ein leistungsfähiges Labor‑Modell, um nach Backup‑Wege zu suchen, die EGFR‑abhängige Tumoren erhalten — Informationen, die letztlich zu Kombinationsbehandlungen führen könnten, die sowohl EGFR als auch seine verborgenen Komplizen anvisieren.
Zitation: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Schlüsselwörter: EGFR, Gebärmutterhalskrebs, CRISPR, EGF-Signalgebung, AKT-Signalweg