Clear Sky Science · de
DNA-Konjugation auf funktionalisierten Kunststoffoberflächen für sequenzielle, iterative Einzelmolekül-Sequenzierung
Daten von morgen in winzigen Strängen speichern
Stellen Sie sich vor, Sie sichern Ihre Fotos, Bücher oder wissenschaftlichen Aufzeichnungen in einer Form, die Jahrhunderte überdauern kann und in ein Partikel passt, das kleiner ist als ein Sandkorn. DNA – das gleiche Molekül, das unsere Gene trägt – zeichnet sich zunehmend als vielversprechender Kandidat für extrem dichte, langlebige Datenspeicherung aus. Dieser Artikel untersucht eine neue Methode, DNA-Daten sicher an der Innenseite gewöhnlicher Kunststoff-Labormikroröhrchen zu „parken“ und sie wiederholt auszulesen, ohne die Originalmoleküle zu zerstören.
Eine neue Art von Daten-„Daumenlaufwerk”
Heutige Festplatten und Flash-Speicher nutzen sich ab und speichern pro Gramm weitaus weniger Informationen, als DNA potenziell kann. Forscher haben bereits gezeigt, wie digitale Dateien in DNA-Basenfolgen übersetzt werden können. Aber jedes Mal, wenn diese DNA-Stränge kopiert oder sequenziert werden, geht ein Teil des Originals verloren – ähnlich wie Tinte beim wiederholten Fotokopieren ausbleicht. In dieser Studie verwandelten die Autorinnen und Autoren das schlichte Kunststoff-PCR-Röhrchen – bereits Standard in Biologie-Labors – in ein wiederverwendbares physisches Speichergerät. Sie hefteten chemisch DNA-Stränge mit kodierten Daten an die Innenfläche des Röhrchens, sodass die DNA fixiert bleibt, während Kopien wiederholt erzeugt und gelesen werden. 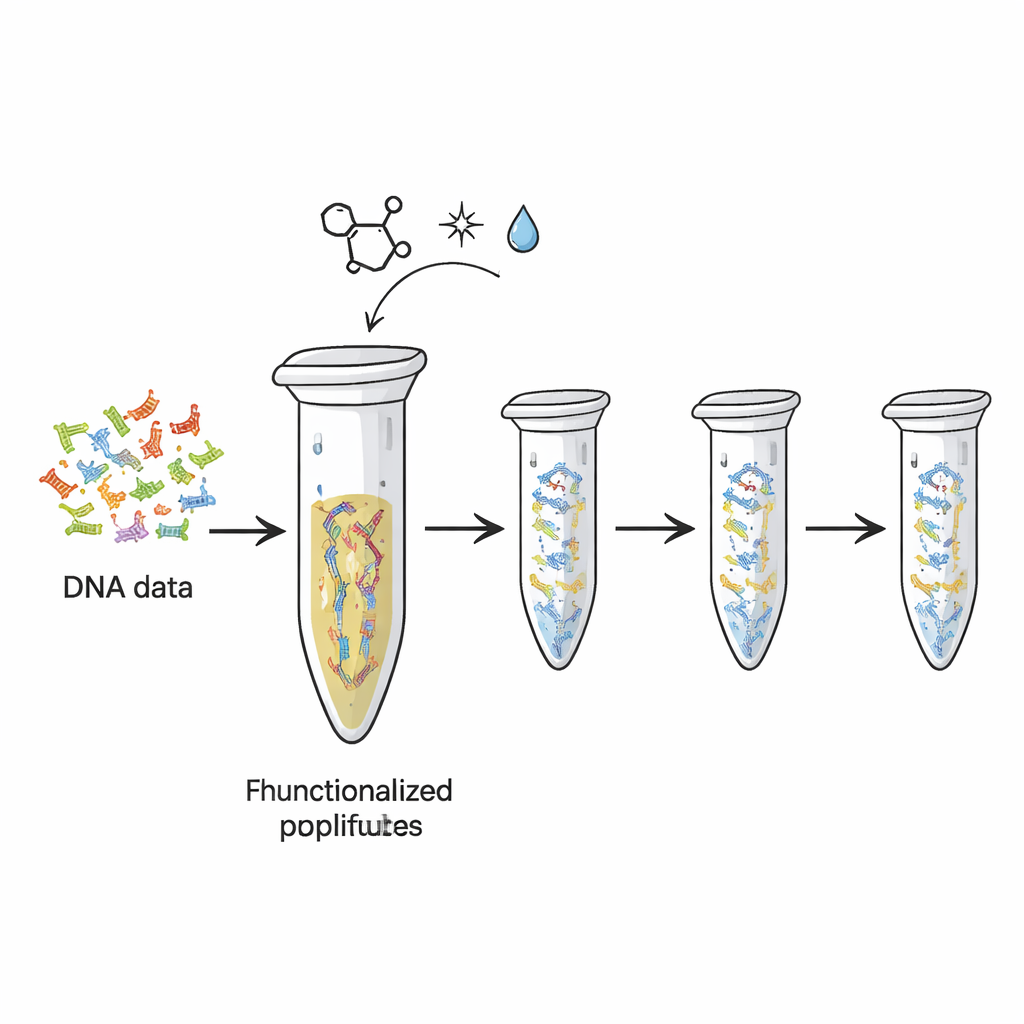
DNA auf Kunststoff „anklicken”
Das Team nutzte eine Form hochspezifischer „Click-Chemie“ – Reaktionen, die für Schnelligkeit, Zuverlässigkeit und milde Bedingungen geschätzt werden. Zunächst versahen sie die Enden der DNA-Stränge, die verschiedene Daten-„Dateien“ repräsentierten, mit speziellen chemischen Anhängseln. Diese Anhängsel, basierend auf einem Molekül namens TCO, sind so entworfen, dass sie an passende Gruppen (MTz) binden, die auf die Kunststoffoberfläche des Röhrchens aufgebracht wurden. Treffen beide aufeinander, bilden sie eine stabile kovalente Bindung und kleben die DNA effektiv an den Kunststoff. Tests mit einem Kontroll-DNA-Fragment zeigten, dass nach der Inkubation nahezu die gesamte DNA aus der Lösung verschwunden war, was darauf hindeutet, dass sie nun an der Röhrchenwand immobilisiert war. Die Plattform konnte Mengen im Bereich von hunderten Femtomol halten, was auf eine ausreichend große Kapazität für praktische Datensätze hindeutet.
Digitale „Dateien“ bei Bedarf abrufen
Um zu prüfen, ob diese oberflächengebundene DNA weiterhin als praktikables Archiv funktioniert, kodierten die Forschenden Text und andere Daten in einen Pool von etwa 15.000 kurzen DNA-Strängen, gruppiert in 18 „Dateigruppen“. Jede Gruppe konnte selektiv mit ihrem eigenen Primerpaar kopiert werden – kurzen Startsequenzen, die die Kopiermaschinerie zu den richtigen Zielen lenken. Das Team führte wiederholt Standard-PCR-Reaktionen im selben Röhrchen durch und wählte dabei jedes Mal eine andere Dateigruppe zur Amplifikation. Nach jedem Lauf entfernten sie die kopierte DNA, reinigten das Röhrchen mit Enzymen, die verbleibende Produkte in Lösung verdauten, und gingen zur nächsten Datei über. Nanoporen-Sequenzierung des kopierten Materials zeigte, dass die meisten Dateigruppen mit hoher Genauigkeit abgerufen wurden und Kreuzkontaminationen aus früheren Läufen äußerst gering blieben, typischerweise bei etwa 1 Prozent oder weniger.
Eine schonendere Art des Auslesens finden
Es gab jedoch einen Haken: Als sie die PCR im selben Röhrchen bis zu 18 Mal wiederholten, nahm die Menge der abgerufenen DNA stetig ab. PCR beruht auf schnellen Temperaturwechseln, und die Autorinnen und Autoren folgerten, dass die wiederholten hohen Temperaturen die immobilisierte DNA oder ihre Verbindung mit dem Kunststoff schädigten, obwohl Kontrolltests nahelegten, dass die DNA nicht einfach in Lösung ausgewaschen wurde. Zur Lösung dieses Problems griffen sie auf die Rekombinase-Polymerase-Amplifikation (RPA) zurück, eine neuere Methode, die bei einer einzigen, vergleichsweise niedrigen Temperatur nahe der Körpertemperatur arbeitet. Mit RPA auf frisch DNA-beschichteten Röhrchen fragten sie erneut alle 18 Dateigruppen nacheinander ab. Diesmal waren die Ausbeuten hoch – etwa 60 ng/µL – und zeigten keinen ähnlichen Abwärtstrend. Das Muster, welche Stränge beim Kopieren bevorzugt oder benachteiligt wurden, stimmte zudem gut mit dem überein, was beobachtet wurde, wenn die DNA frei in Lösung vorlag. 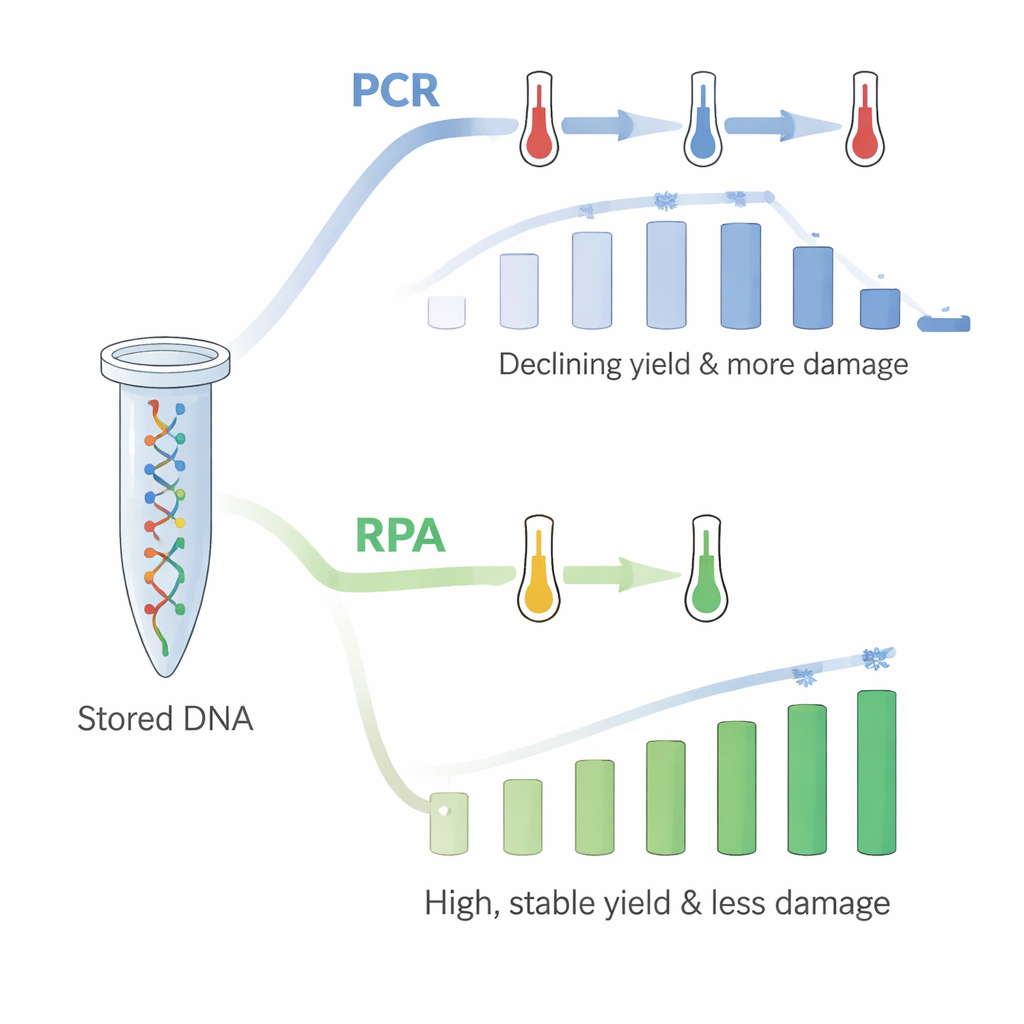
Auf dem Weg zu tragbarem, langlebigem DNA-Speicher
Durch die Kombination robuster Click-Chemie mit niedertemperaturigem DNA-Kopieren zeigt diese Arbeit einen praktikablen Weg, einfache Kunststoffröhrchen in wiederverwendbare DNA-Datenkassetten zu verwandeln. Die DNA bleibt physikalisch am Röhrchen verankert, wo sie wiederholt für spezifische „Dateien“ abgefragt werden kann, ohne die Originalmoleküle zu verbrauchen – insbesondere bei Verwendung der schonenderen RPA-Methode. Für Nicht-Spezialisten lautet die Kernbotschaft: DNA ist nicht nur der Code des Lebens – sie kann auch als kompakte, dauerhafte Speichermedium für digitale Informationen dienen. Methoden wie diese rücken uns näher an eine Zukunft, in der Ihre langfristigen Backups nicht mehr auf rotierenden Scheiben liegen, sondern in sorgfältig konstruierten Molekülen still auf einem Laborregal ruhen.
Zitation: Roy, S., Ji, H.P. & Lau, B.T. DNA conjugation on functionalized plastic surfaces for sequential, iterative single molecule sequencing. Sci Rep 16, 6467 (2026). https://doi.org/10.1038/s41598-026-37575-y
Schlüsselwörter: DNA-Datenspeicherung, Click-Chemie, Konjugation an Kunststoffoberflächen, Rekombinase-Polymerase-Amplifikation, Nanoporen-Sequenzierung