Clear Sky Science · de
Vervielfältigung der Genkopien treibt IFI30-Überexpression und koordinierte Immunaktivierung voran und identifiziert ein neues diagnostisches und therapeutisches Ziel beim Magenadenokarzinom
Warum ein Protein im Magen wichtig ist
Magenkrebs gehört zu den tödlichsten Krebsarten weltweit, vor allem weil er häufig spät entdeckt wird und schwer zu behandeln sein kann. Diese Studie konzentriert sich auf ein wenig bekanntes Protein namens IFI30, das in Zellen vorkommt, die dem Immunsystem helfen, Bedrohungen zu erkennen. Indem die Forschenden nachverfolgen, wie IFI30 in Magentumoren verändert ist und wie es die Abwehr des Körpers beeinflusst, legen sie nahe, dass es ein wirksames Instrument für frühere Diagnosen und die Auswahl wirksamer, personalisierter Therapien werden könnte.
Ein verborgenes Signal in Magentumoren
Das Team begann mit einer grundlegenden Frage: Ist IFI30 in gesundem gegenüber krebsartigem Magengewebe unterschiedlich ausgeprägt? Anhand großer öffentlicher Datensätze, die Genaktivität aus Tausenden von Proben zusammenführen, stellten sie fest, dass IFI30 beim Magenadenokarzinom – der häufigsten Form von Magenkrebs – durchgängig deutlich höher ist als im normalen Magenepithel. Dies galt über mehrere unabhängige Patientengruppen hinweg und sowohl auf RNA- als auch auf Proteinebene. Als die Autor:innen prüften, wie gut IFI30 allein Tumorgewebe von gesundem Gewebe unterscheiden kann, war die Leistung beeindruckend: eine diagnostische Genauigkeit (AUC) von 0,92, was für einen einzelnen Marker als ausgezeichnet gilt. Mikroskopische Aufnahmen zeigten IFI30 außerdem im intrazellulären Recycling-System, wo Antigene für die Immunerkennung verarbeitet werden.
DNA‑Veränderungen, die IFI30 hochfahren
Im nächsten Schritt untersuchten die Forschenden, warum IFI30 in diesen Tumoren so stark erhöht ist. Beim Durchsuchen von Krebsgenomen aus The Cancer Genome Atlas fanden sie, dass zusätzliche Kopien des IFI30-Gens – sogenannte Kopienzahlamplifikationen – der Haupttreiber seiner Überexpression sind. Tumoren mit amplifiziertem IFI30 zeigten tendenziell eine größere genomische Instabilität und trugen häufig bekannte Krebsmutationen wie TP53 und PIK3CA. Mit steigender IFI30-Kopienzahl stiegen auch die RNA-Spiegel an, was auf eine direkte Verbindung zwischen strukturellen DNA‑Veränderungen und der erhöhten Produktion dieses Proteins hindeutet. Dies zeichnet IFI30 nicht als passiven Beobachter, sondern als Teil eines breiteren Musters aggressiver Tumorbiologie.
Immun‑Crosstalk rund um den Tumor
Da IFI30 an der Verarbeitung von Material beteiligt ist, das Immunzellen als „Gesucht“-Poster für T‑Zellen präsentieren, untersuchten die Forschenden, wo genau es im Tumormikromilieu lokalisiert ist. Einzelzellsequenzierung, die Gene in einzelnen Zellen ausliest, zeigte, dass IFI30 besonders in dendritischen Zellen, Makrophagen und CD8‑T‑Zellen angereichert ist – Schlüsselakteure beim Auslösen und Aufrechterhalten der Antitumorimmunität. Netzwerkanalysen offenbarten dichte Kommunikation zwischen IFI30‑reichen Immunzellen und den umgebenden Tumor‑ und Stützstrukturen. Tumoren mit hohem IFI30 wiesen eine starke Aktivierung von Wegen auf, die mit Antigenpräsentation, Entzündungssignalen und Kommunikationsmolekülen zusammenhängen, die Immunzellen anziehen und organisieren. Gleichzeitig zeigten diese Tumoren Merkmale von Invasion und Stress, wie beschleunigten Zellzyklus, Gewebeumgestaltung und Anpassung an niedrige Sauerstoffbedingungen, was IFI30s Rolle an der Schnittstelle von Angriff und Abwehr im Krebs unterstreicht.
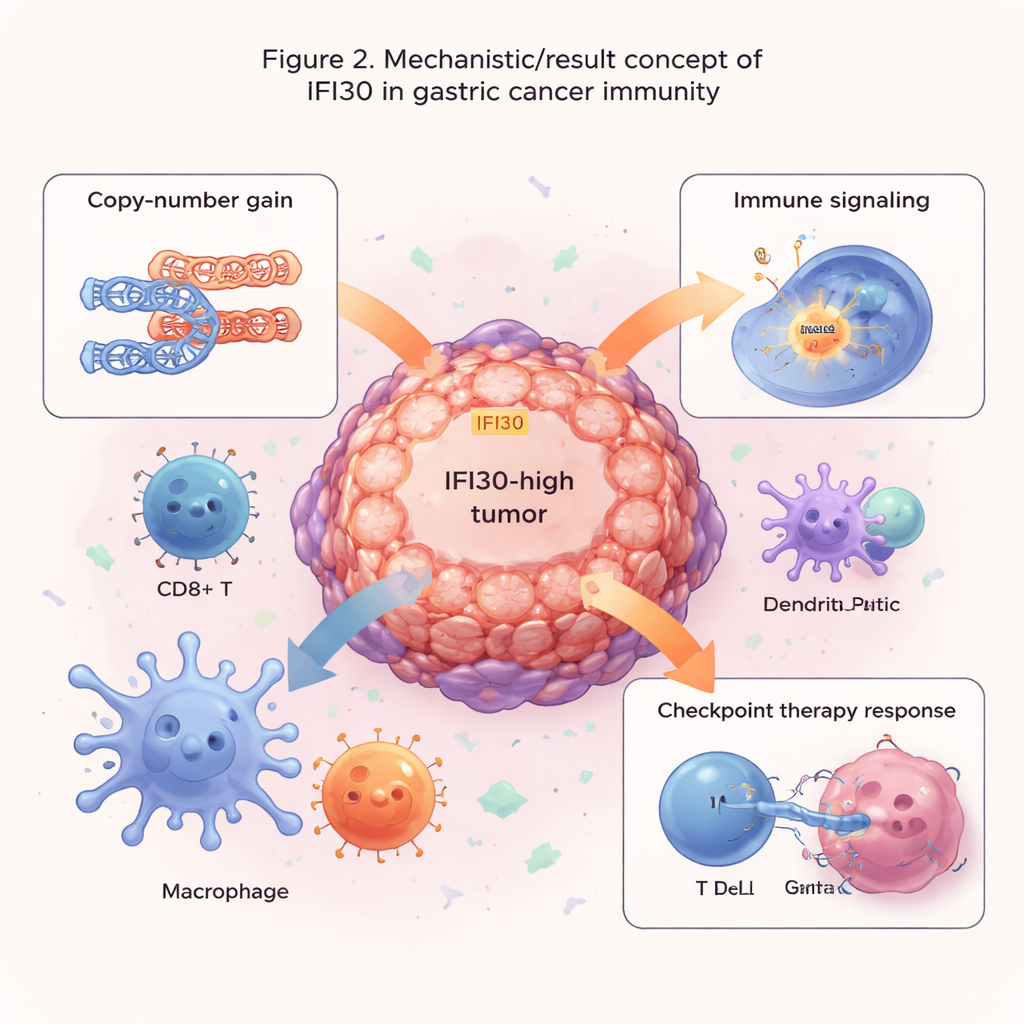
Anhaltspunkte für Wirkstoffwahl und Immuntherapie
Die Autor:innen fragten dann, ob IFI30 helfen könnte vorherzusagen, wie Tumoren auf Behandlungen reagieren. Durch die Verknüpfung von IFI30‑Spiegeln mit großen Arzneimittel‑Antwortdatensätzen fanden sie, dass IFI30‑hohe Tumoren dazu neigen, gegen einige Mittel, die die Zellteilung oder einen häufigen Wachstumsweg (MAPK) angreifen, resistent zu sein, jedoch empfindlicher gegenüber Wirkstoffen erscheinen, die EGFR‑ und PI3K/AKT‑Signalwege blockieren. Bemerkenswert ist, dass IFI30‑Spiegel eng mit PD‑L1 korrelierten, einer wichtigen Bremse der T‑Zellen, die von aktuellen Checkpoint‑Inhibitoren angegriffen wird. In mehreren Studien zur Immuntherapie sprachen Patient:innen mit Tumoren mit höherer IFI30‑Expression eher auf Checkpoint‑Blockade an als solche mit niedrigen Werten. Ein IFI30‑basierter Score übertraf etablierte Maße wie die Tumormutationslast und PD‑L1 allein und war besonders in Tumoren mit hoher mikrosatelliteninstabilität angereichert, einer Untergruppe, von der bereits bekannt ist, dass sie besser auf Immuntherapie anspricht.
Vom Labor zur potenziellen neuen Zielstruktur
Um zu prüfen, ob IFI30 nur ein Marker ist oder auch das Krebswachstum fördert, senkte das Team dessen Spiegel in Magenkrebszelllinien mit genetischen Werkzeugen. Bei reduziertem IFI30 wuchsen die Krebszellen langsamer, was auf eine direkte Rolle bei der Aufrechterhaltung der Tumorproliferation hinweist. Zusammengenommen deuten die Daten darauf hin, dass IFI30 sowohl ein Indikator für Immunaktivität als auch ein Beitrag zu malignem Verhalten ist. Für Patient:innen bedeutet das, dass eine einfache Messung von IFI30 eines Tages Ärzt:innen helfen könnte, Magenkrebs zuverlässiger zu erkennen, vorherzusagen, wer von bestimmten zielgerichteten Medikamenten oder Immuntherapien profitiert, und möglicherweise neue Behandlungen zu lenken, die die tumorfördernden Wirkungen von IFI30 direkt oder indirekt blockieren.
Zitation: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
Schlüsselwörter: Magenkrebs, IFI30, Biomarker, Tumorimmunität, Immuntherapie