Clear Sky Science · de
Computergestützte Analyse von X2CaZnH6 (X = K, Rb und Cs)-Hydriden für die Wasserstoffspeicherung
Wasserstoff in einer Box
Wasserstoff wird oft als sauberer Kraftstoff der Zukunft gepriesen, doch seine sichere und kompakte Speicherung bleibt ein zentrales Hindernis. Diese Studie untersucht eine neue Familie kristalliner Materialien, die Wasserstoff in ihrem atomaren Gerüst aufnehmen können, ähnlich wie Wasser in einem Schwamm. Indem die Verbindungen zuerst am Rechner entworfen werden, bevor sie im Labor hergestellt werden, zeigen die Autorinnen und Autoren, wie sie als feste Brennstoffe für künftige wasserstoffbetriebene Technologien dienen könnten.
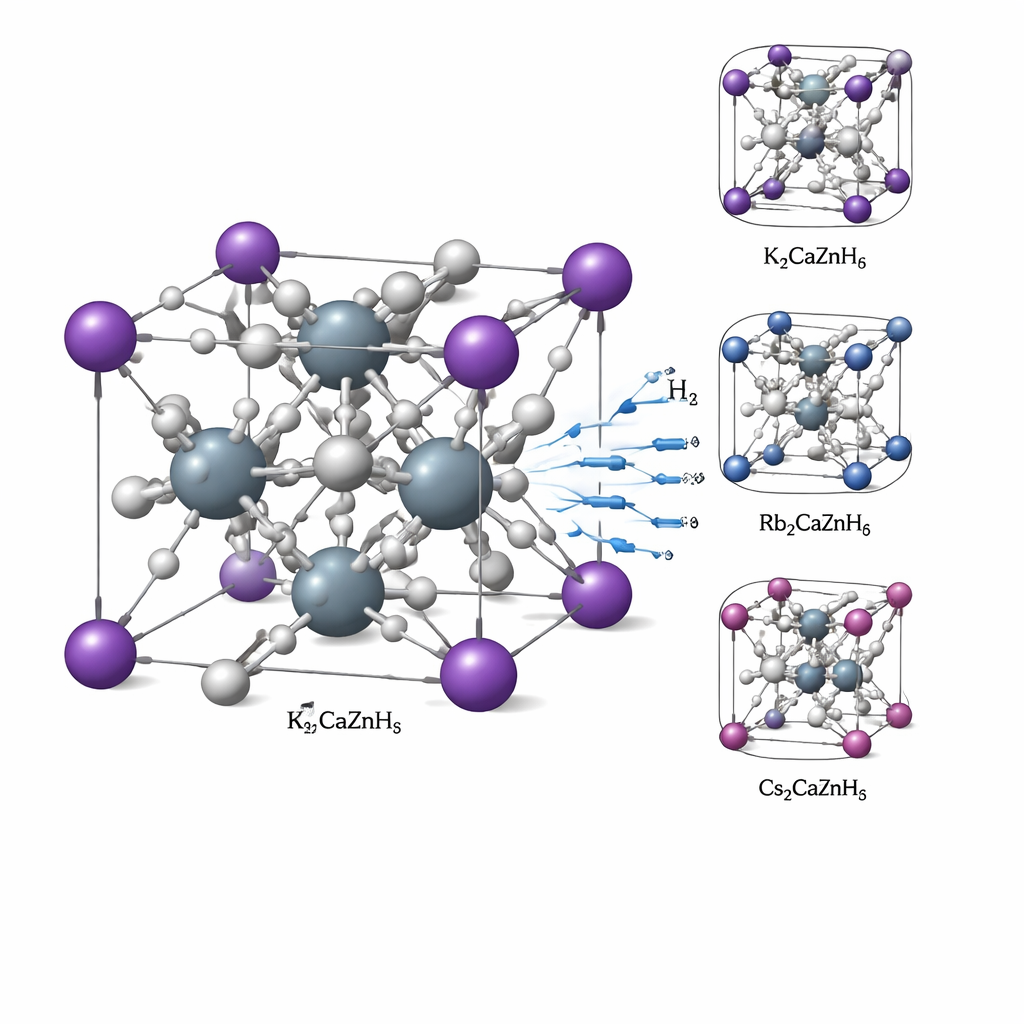
Ein Kristall aufgebaut wie ein 3D-Gitter
Die untersuchten Materialien werden Doppel-Perowskit-Hydride genannt und haben die Formel X2CaZnH6, wobei X Kalium (K), Rubidium (Rb) oder Cäsium (Cs) sein kann. Alle drei bilden eine einfache würfelähnliche Struktur, in der schwere Atome an wohlgeordneten Positionen sitzen und Wasserstoffatome die Zwischenräume besetzen. Mithilfe quantenmechanischer Rechnungen bestätigen die Autorinnen und Autoren, dass diese Kristalle strukturell stabil sind: Die Atome passen von den Größen her zusammen, die Gesamtenergie des Materials ist niedrig genug, dass es sich natürlich bilden sollte, und die Atomschwingungen deuten nicht auf versteckte Instabilitäten hin. Mechanische Tests im Computer zeigen, dass die Kristalle steif, aber nicht übermäßig spröde sind — ein Gleichgewicht, das ihnen hilft, ihre Form zu bewahren und zugleich kleine Umordnungen zu erlauben, wenn Wasserstoff aufgenommen oder freigesetzt wird.
Wie viel Wasserstoff können sie aufnehmen?
Für jedes Speichermaterial sind zwei Kennzahlen wichtig: wie viel Wasserstoff es nach Masse (gravimetrische Kapazität) und nach Volumen (volumetrische Kapazität) aufnehmen kann, sowie die Temperatur, bei der Wasserstoff freigesetzt wird. Die drei hier untersuchten Verbindungen speichern etwa 1,6 bis 3,2 % ihres Gewichts als Wasserstoff und rund 15 bis 18 Kilogramm Wasserstoff pro Kubikmeter Material. Die Kalium-Variante K2CaZnH6 speichert am meisten Wasserstoff, benötigt aber höhere Temperaturen (etwa 658 K bzw. 385 °C) zur Freisetzung. Die Cäsium-Variante speichert etwas weniger und verlangt ebenfalls relativ hohe Temperaturen. Das Rubidiumverbindung Rb2CaZnH6 sticht hervor: Sie gibt Wasserstoff bei ungefähr 385 K (etwa 110 °C) frei — ein Bereich, der deutlich näher an dem liegt, was als praktisch für reale Geräte gilt, und dabei eine respektable Speicherdichte beibehält.
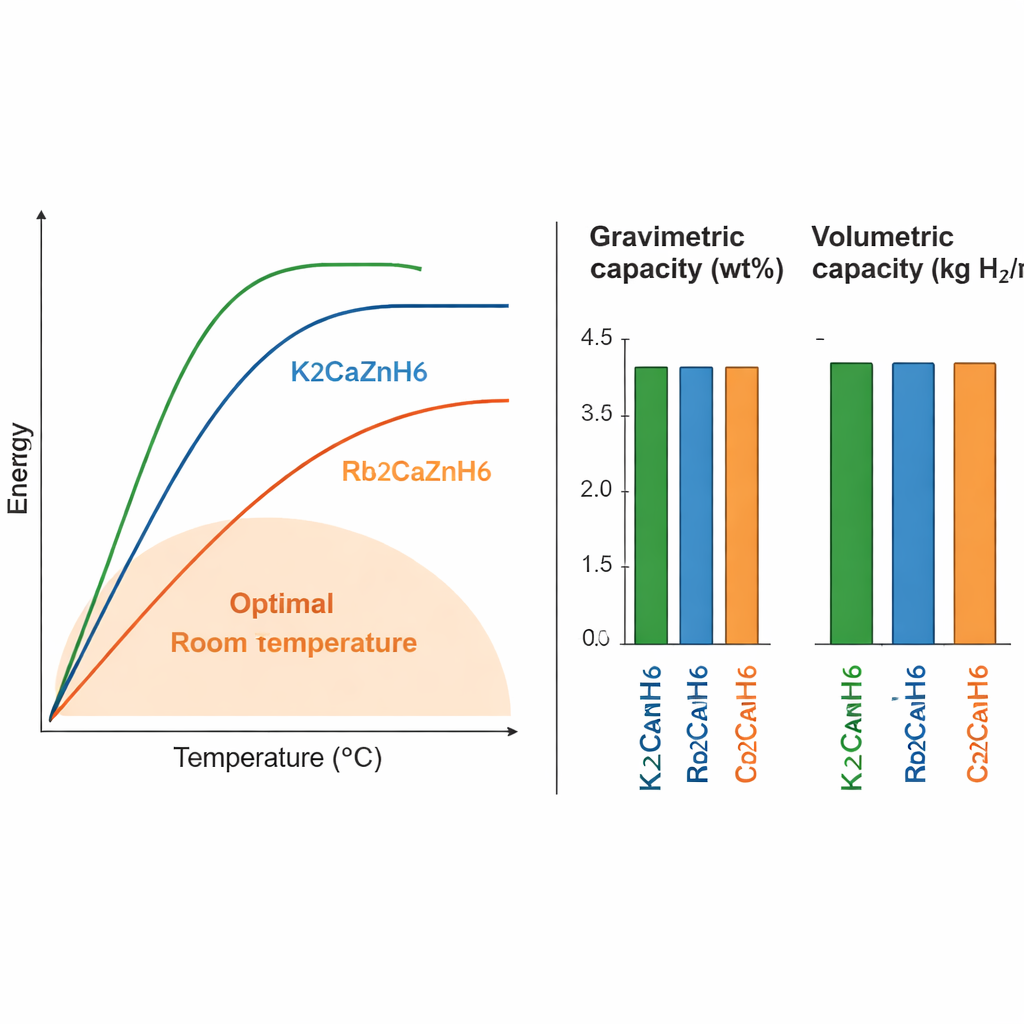
Warum Atome und Elektronen wichtig sind
Um zu verstehen, warum sich diese Materialien so verhalten, untersuchen die Autorinnen und Autoren, wie Elektronen zwischen Atomen geteilt werden und wie das die Bindungen beeinflusst. In allen drei Verbindungen wirken Kalium, Rubidium oder Cäsium als Elektronendonoren, während Zink, Calcium und Wasserstoff Elektronen anziehen. Die Wasserstoffatome nehmen eine teilweise negative Ladung an, und ihre Bindungen zu Calcium und Zink sind überwiegend ionisch mit einem Hauch kovalenter Charaktere. Diese Art der Bindung hält Wasserstoff so stark, dass er nicht leicht entweicht, aber nicht so fest, dass er sich nicht durch Erwärmen freisetzen ließe. Wichtig ist auch, dass Wasserstoffatome im Kristall keine starken H–H-Bindungen ausbilden, das heißt der Wasserstoff liegt als getrennte Atome vor und nicht als bereits gebildete Moleküle — ein Zustand, der eine kontrollierte Freisetzung begünstigt.
Leicht, elektrisch und mechanisch stabil
Diese Kristalle sind außerdem Halbleiter mit einer moderaten Energie-Lücke zwischen besetzten und unbesetzten elektronischen Zuständen. Das bedeutet, sie können mit Licht über ein weites Farbspektrum interagieren, insbesondere im sichtbaren und ultravioletten Bereich. Die Rechnungen zeigen starke Lichtabsorption und nennenswerte optische Leitfähigkeit, was die Möglichkeit eröffnet, dass Licht die Wasserstofffreisetzung unterstützen könnte — eine Art sonnenunterstützte Speicherung. Gleichzeitig erfüllen die Materialien gängige Kriterien mechanischer Stabilität: Sie widerstehen Kompression, Scherung und Brüchen innerhalb vernünftiger Grenzen, und ihre atomaren Schwingungen bleiben bei computergestützten Aufheiztests bei Raumtemperatur gutartig. Zusammengenommen deuten diese Eigenschaften auf ein robustes Gerüst hin, das wiederholtes Laden und Entladen von Wasserstoff aushalten kann.
Was das für zukünftige Energiesysteme bedeutet
Alltagssprachlich identifiziert die Studie drei neue „Wasserstoff-Schwamm“-Materialien, die stabil, relativ robust und in der Lage sind, Wasserstoff in einem kompakten Feststoff unterzubringen. Obwohl ihr Wasserstoffgehalt nach Masse noch nicht die ambitioniertesten Zielvorgaben erreicht, ist ihre volumetrische Speicherung vielversprechend, und besonders die rubidiumbasierte Verbindung arbeitet bei Temperaturen, die mit vielen praktischen Systemen kompatibel sind. Da sich ihr Verhalten durch den Austausch eines Alkali-Elements leicht einstellen lässt, bieten diese Doppel-Perowskit-Hydride eine flexible Grundlage, um bessere feste Wasserstoffbrennstoffe zu entwerfen und möglicherweise Speicherung mit lichtgesteuerter Kontrolle in künftigen sauberen Energietechnologien zu kombinieren.
Zitation: Al-Zoubi, N., Almahmoud, A., Almahmoud, A. et al. Computational analysis of X2CaZnH6 (X = K, Rb and Cs) hydrides for hydrogen storage. Sci Rep 16, 6889 (2026). https://doi.org/10.1038/s41598-026-37564-1
Schlüsselwörter: Wasserstoffspeicherung, Metallhydride, Doppel-Perowskit, Festkörperenergie, saubere Brennstoffe