Clear Sky Science · de
Vorkommen und Genotypisierung von Pseudomonas aeruginosa aus Lebensmitteln und menschlichen Quellen
Warum ein verbreiteter Keim für den Alltag wichtig ist
Pseudomonas aeruginosa ist ein umständlicher Name, aber es handelt sich um einen Keim, der sich still von Wasser und rohen Lebensmitteln in Krankenhäuser und Menschen verbreiten kann und dabei gelegentlich schwere, schwer behandelbare Infektionen verursacht. Diese Studie, durchgeführt in einer ägyptischen Stadt, verfolgte, wo dieses Bakterium in Alltagsgegenständen wie Leitungswasser, Fisch, Fleisch und Milch sowie in Wundinfektionen von Patienten auftaucht. Untersucht wurde außerdem, wie widerstandsfähig es gegenüber Antibiotika ist und ob es genetische „Werkzeuge“ trägt, die es gefährlicher machen. Die Ergebnisse helfen zu erklären, weshalb Lebensmittelhygiene, sauberes Wasser und ein umsichtiges Antibiotika‑Management zusammenhängen, wenn es um den Schutz der öffentlichen Gesundheit geht.
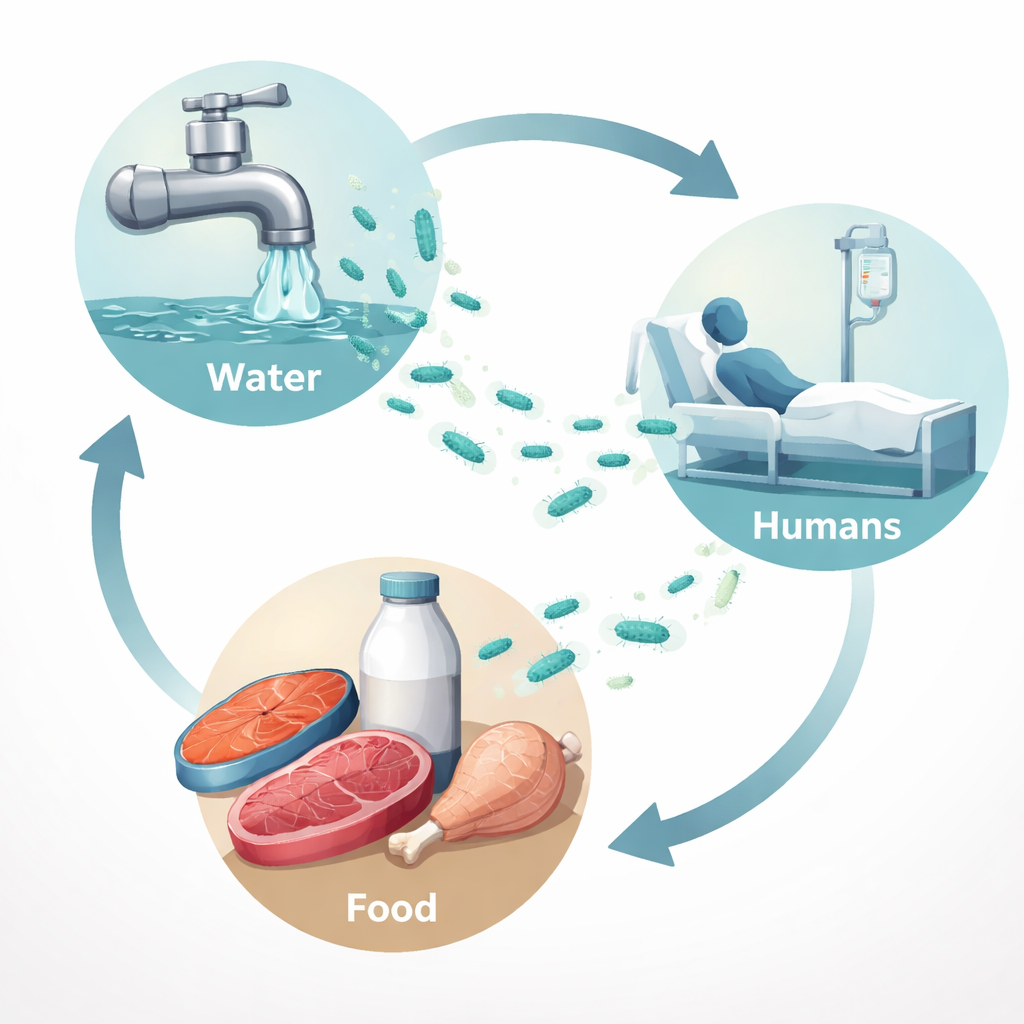
Dem Keim vom Markt bis ins Krankenhaus folgen
Die Forschenden sammelten 350 Proben aus der Umgebung von Sadat City in der Gouverneurschaft Menoufia, Ägypten. Dazu gehörten menschliches Eitermaterial aus infizierten Wunden, Leitungswasser, Fischabstriche, Hühnerfleisch, Hackfleisch, Rohmilch und Oberflächenproben aus Krankenhäusern. Gesucht wurde gezielt nach P. aeruginosa. Insgesamt wurde das Bakterium in etwa einer von sieben Proben nachgewiesen. Am häufigsten trat es in menschlichen Wundproben auf (etwa eine von vier), es war aber auch in Leitungswasser, Fisch und Rohmilch zu finden und in geringerem Maße in Huhn und Hackfleisch. Interessanterweise fielen keine der Krankenhausoberflächenabstriche positiv aus, was darauf hindeutet, dass in diesem Setting möglicherweise eher Lebensmittel und Wasser in das Krankenhaus eingeschleust werden als kontaminierte Arbeitsflächen und Geräte.
Wie gefährlich sind diese Bakterien?
Das Auffinden des Keims ist nur ein Teil der Geschichte; sein Verhalten ist ebenso bedeutsam. Das Team testete jede Isolatform mit standardisierten Laborverfahren darauf, ob sie einen schleimigen Schutzfilm bilden kann, einen sogenannten Biofilm. Etwa ein Drittel der Isolate bildete solche Biofilme, einige davon stark und dicht. Biofilme machen Bakterien deutlich schwerer zu beseitigen, weil sie die Zellen vor Reinigungsmitteln und Antibiotika abschirmen. Genetische Untersuchungen der biofilmproduzierenden Stämme zeigten, dass sie mehrere „Virulenz“-Gene trugen, die Proteine kodieren, welche Gewebe schädigen oder den Bakterien helfen, an Oberflächen zu haften und dem Immunsystem zu entgehen. Einfach ausgedrückt: Viele der gefundenen Stämme waren nicht nur vorhanden, sondern gut ausgerüstet, um Krankheit zu verursachen.
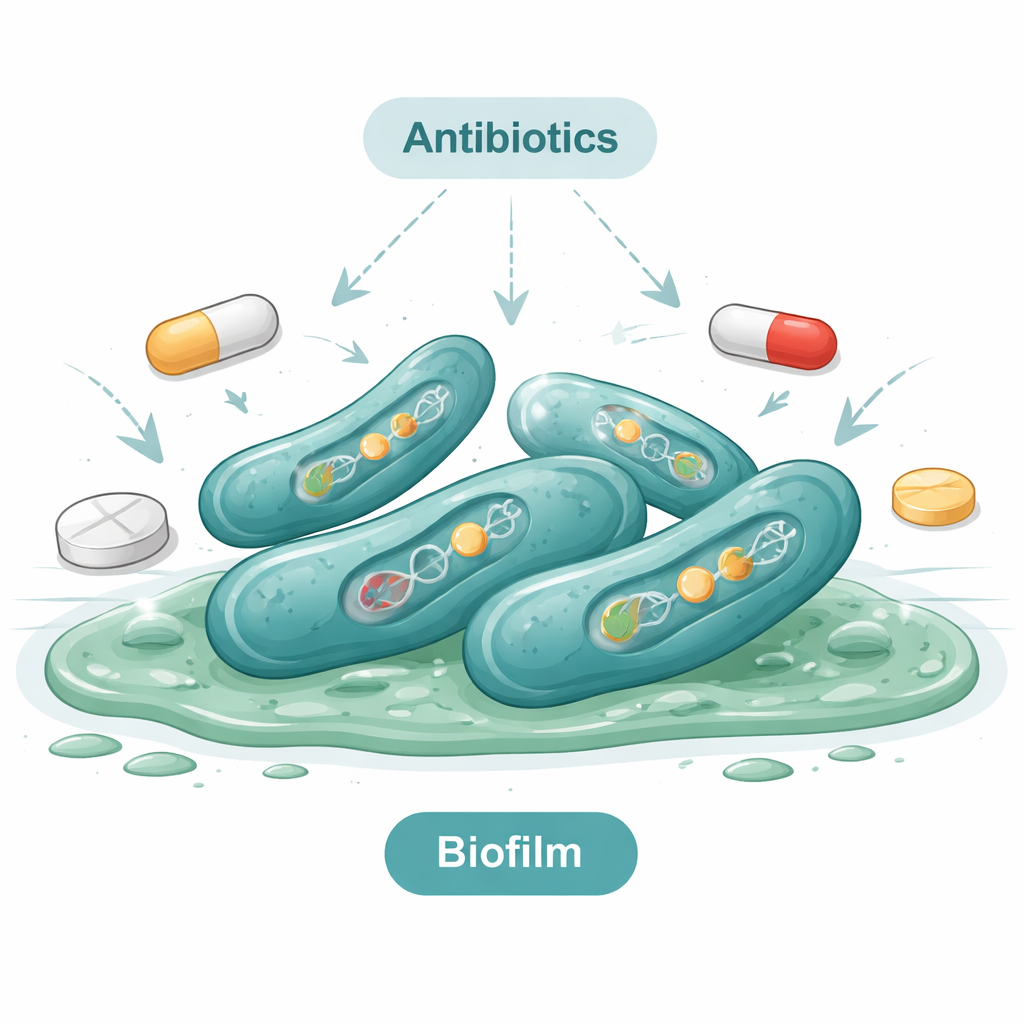
Antibiotika, die versagen — und einige, die noch wirken
Die Studie stellte dann die drängende Frage: Gegen welche Antibiotika sind diese Stämme noch empfindlich? Als die Forschenden 50 Isolate 16 verschiedenen Wirkstoffen aussetzten, zeigte sich, dass viele gängige Antibiotika kaum noch wirksam sind. Alle Isolate waren resistent gegen Amoxicillin, und nahezu alle zeigten Resistenz gegenüber Erythromycin und mehreren anderen älteren Wirkstoffen. Die meisten ließen sich außerdem von Colistin, einem oft als letztes Mittel eingesetzten Antibiotikum, kaum beeindrucken. Positiv zu vermerken ist, dass einige wenige Antibiotika — darunter Imipenem und verwandte Substanzen — bei vielen Isolaten noch wirksam waren. Trotz dessen waren mehr als vier von fünf Stämmen gegen mehrere Antibiotikaklassen gleichzeitig resistent, ein Zustand, der als Multiresistenz bezeichnet wird. Genetische Tests bestätigten dies: Die Bakterien trugen Resistenzgene, die ihnen helfen, Antibiotika zu inaktivieren oder aus ihren Zellen hinauszupumpen.
Verbindung zwischen Lebensmitteln, Wasser und menschlichen Infektionen
Um zu untersuchen, wie verwandt die Stämme aus den verschiedenen Quellen sind, verwendete das Team die DNA‑„Fingerprinting“-Methode ERIC‑PCR an einer Auswahl klinischer Isolate. Dieses Verfahren gruppiert Bakterien anhand wiederkehrender Muster in ihren Genomen. Die Analyse teilte die Stämme in Cluster, die Proben sowohl von Menschen als auch von Lebensmitteln wie Fisch, Milch, Huhn und Hackfleisch enthielten. Dieses Muster legt nahe, dass Lebensmittel und Wasser als Zwischenstationen dienen können, wodurch ähnliche P. aeruginosa‑Stämme zwischen der Umwelt und menschlichen Patienten zirkulieren. Praktisch bedeutet das: Der in einem rohen Fisch auf dem Markt nachgewiesene Keim kann eng verwandt sein mit dem, der eine Wundinfektion in einem nahegelegenen Krankenhaus verursacht.
Was das für die Gesundheit im Alltag bedeutet
Für Laien ist die Botschaft klar: Ein verbreiteter Umweltkeim findet seinen Weg aus Wasser und tierischen Lebensmitteln in Menschen, und viele seiner Stämme sind mit Genen ausgestattet, die sie zäh, hartnäckig und schädlich machen. Da so viele Isolate gegen mehrere Antibiotika resistent sind, wird die Behandlung von Infektionen komplizierter, kostenintensiver und riskanter. Die Autorinnen und Autoren plädieren deshalb für bessere Hygiene in der Lebensmittelproduktion und -handhabung, sicherere Wassersysteme und einen vorsichtigeren Einsatz von Antibiotika sowohl beim Menschen als auch in der Tierhaltung, um die Verbreitung dieser robusten Stämme zu verlangsamen. Sie fordern außerdem eine kontinuierliche Überwachung und detailliertere genetische Studien, um nachzuzeichnen, wie P. aeruginosa durch die Lebensmittelkette und in Krankenhäuser wandert, damit künftige Ausbrüche besser vorhergesagt und verhindert werden können.
Zitation: Mousa, W.S., Abdeen, E.E., El-Gendy, H.F. et al. Prevalence and genotyping of Pseudomonas aeruginosa from food and human sources. Sci Rep 16, 7179 (2026). https://doi.org/10.1038/s41598-026-37559-y
Schlüsselwörter: Pseudomonas aeruginosa, gesundheitlich relevante Lebensmittelkeime, Antibiotikaresistenz, Biofilm, Wasserverunreinigung