Clear Sky Science · de
Computergestützte Identifizierung von Phytochemikalien aus Terminalia arjuna als potenzielle 3α-HSD3-Inhibitoren
Warum diese Forschung wichtig ist
Brustkrebs ist die häufigste Krebserkrankung bei Frauen, und viele Tumoren wachsen als Reaktion auf Hormone. Diese Studie stellt eine aktuelle Frage: Können natürliche Substanzen aus dem traditionellen Heilbaum Terminalia arjuna zu modernen Wirkstoffkandidaten weiterentwickelt werden, die ein zentrales hormonverarbeitendes Enzym sanft „herunterregeln“, das mit Tumorwachstum verbunden ist? Anstatt Tierversuche zu nutzen, setzen die Forschenden fortgeschrittene Computersimulationen ein, um Pflanzenverbindungen zu finden, die eines Tages ergänzend zu bestehenden Hormontherapien wirken oder diese verbessern könnten.
Hormone, ein einzelnes Enzym und Tumorwachstum
Bei bestimmten Brustkrebsarten, insbesondere dem häufig untersuchten MCF-7-Typ, wird das Wachstum stark vom weiblichen Hormon Östrogen angetrieben. Normalerweise können Androgene (häufig als männliche Hormone bezeichnet) die Wirkung von Östrogen ausgleichen. Das im Mittelpunkt dieser Arbeit stehende Enzym, 3α-HSD3, hilft dabei, ein starkes Androgen in schwächere Formen umzuwandeln. Wenn 3α-HSD3 überaktiv ist, nimmt es diesen schützenden androgenen Einfluss weg und hinterlässt eine östrogengeprägte Umgebung, die Tumorzellen dazu anregt, sich zu vermehren und Behandlungen zu widerstehen. Die Blockade dieses Enzyms könnte daher das Hormonverhältnis wieder zugunsten einer Hemmung des Krebswachstums verschieben.
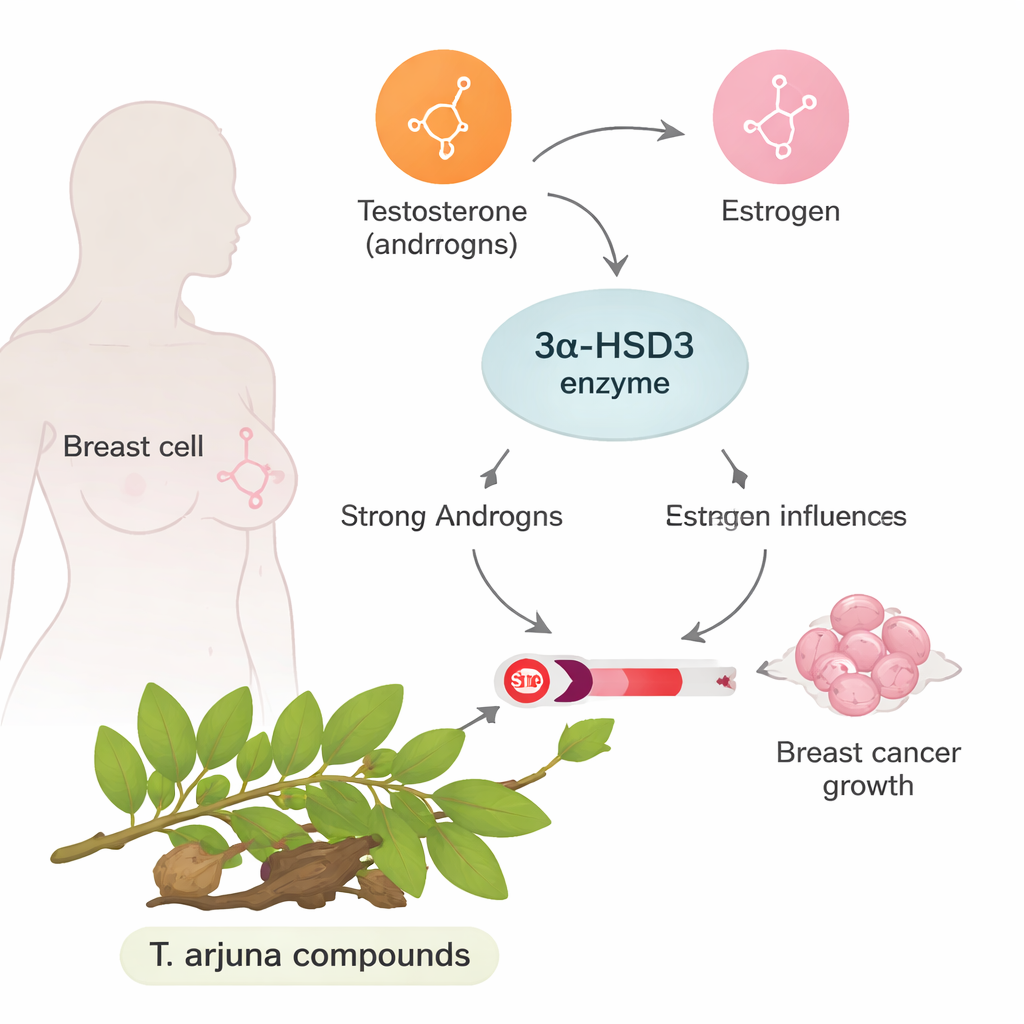
Das Potenzial eines traditionellen Heilbaums
Terminalia arjuna ist ein Baum, der in der südasiatischen traditionellen Medizin lange vor allem für die Herzgesundheit verwendet wird. Rinde und andere Pflanzenteile enthalten viele Pflanzenstoffe mit berichteten antioxidativen und antikarzinogenen Eigenschaften. Gegen 3α-HSD3 wurden diese Verbindungen jedoch bislang nicht systematisch untersucht. Die Autoren wählten neun bekannte Moleküle aus diesem Baum aus, darunter Flavonoide und Tannine, gestützt auf frühere Berichte zu anticancer und schützenden Effekten. Statt sofort Tierversuche oder klinische Studien durchzuführen, nutzten sie zunächst eine Reihe computerunterstützter Werkzeuge des Wirkstoffdesigns, um zu klären: Welche dieser natürlichen Moleküle passen wahrscheinlich in das Enzym, blockieren es, verhalten sich wie echte Medikamente im Körper und vermeiden offensichtliche Toxizität?
Simulation, wie Pflanzenmoleküle auf ihr Ziel treffen
Das Team begann mit der dreidimensionalen Struktur des humanen 3α-HSD3, die zuvor durch Röntgenkristallographie gelöst wurde, und überprüfte deren Qualität mit üblichen Strukturtests. Anschließend bauten sie die Formen der einzelnen Pflanzenmoleküle digital auf und „entspannten“ sie, sodass realistische Konformationen entstehen, wie sie im Körper vorkommen würden. Es folgte das virtuelle Docking: Der Computer testete viele Anordnungen, wie jedes Molekül in die aktive Tasche des Enzyms passen könnte, und bewertete, wie eng und vorteilhaft die Bindung ist. Mehrere Terminalia-Verbindungen zeigten starke vorhergesagte Bindung, oft besser als ein bekannter synthetischer Referenzinhibitor. Vier stachen besonders hervor: Luteolin, Leucocyanidin, Gallussäure und Ellagsäure. Diese wurden nicht nur als enge Binder vorhergesagt, sondern sollten auch mehrere Wasserstoffbrücken und andere stabilisierende Kontakte mit Schlüsselaminosäuren eingehen, die die Enzymaktivität steuern.
Stabilität, Verhalten und Sicherheit in silico testen
Docking liefert einen Momentaufnahme-Eindruck; die Forschenden prüften anschließend, ob diese Komplexe über die Zeit in einer wässrigen, körperähnlichen Umgebung stabil bleiben. Sie führten 100-Nanosekunden-Molekulardynamik-Simulationen durch — im Grunde physikbasierte Filme von Atomen, die bei Körpertemperatur umherschwanken. Messungen zur Bewegung von Protein und Liganden zeigten, dass die vier Pflanzenmoleküle fest in der Enzymtasche verankert blieben und diese häufig stabiler machten als das Kontrollmedikament. Zusätzliche Berechnungen schätzten Bindungsenergien und bestätigten, dass insbesondere Luteolin, Leucocyanidin und Gallussäure starke, günstige Wechselwirkungen bilden. Parallelrechnungen sagten voraus, dass alle vier Kandidaten gut über den Darm aufgenommen werden könnten, sich günstig im Gewebe verteilen, keine gravierenden Wechselwirkungen mit Leberenzymen zeigen und bei therapeutischen Dosen geringes Risiko für genetische oder Organ-Toxizität aufweisen.
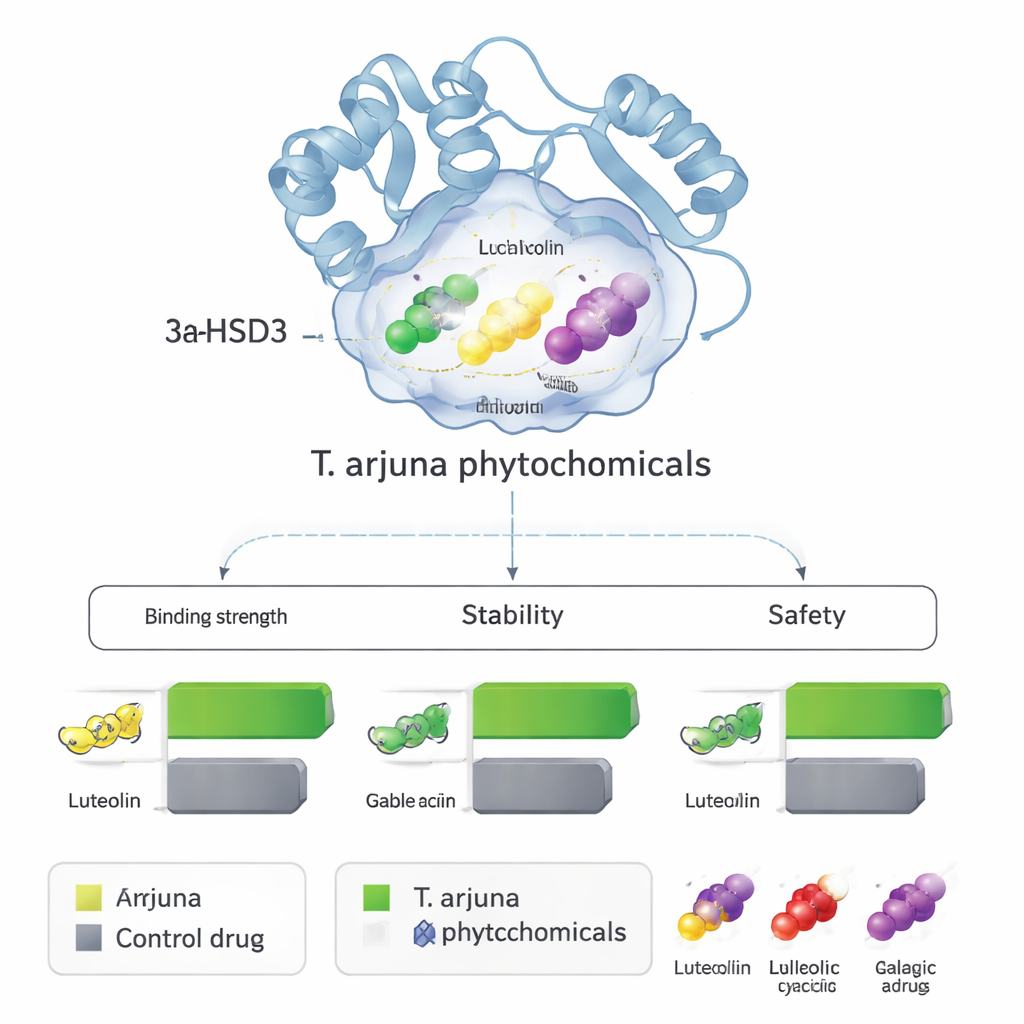
Von Computerprognosen zu zukünftigen Therapien
Für Nichtfachleute ist die zentrale Botschaft: Diese Arbeit erhebt nicht den Anspruch, ein neues Heilmittel entdeckt zu haben, sondern liefert eine fokussierte Shortlist vielversprechender Naturstoffe. Luteolin, Leucocyanidin, Gallussäure und Ellagsäure aus Terminalia arjuna scheinen nach mehreren unabhängigen Computertests an 3α-HSD3 zu binden und es potenziell zu blockieren — ein Enzym, das zur Entstehung einer östrogenreichen Umgebung in hormonempfindlichen Brustkrebszellen beiträgt. Auf dem Papier wirken sie außerdem arzneimittelähnlich und relativ sicher. Die nächsten unverzichtbaren Schritte sind Laborversuche, um zu prüfen, ob diese Vorhersagen zutreffen: Hemmen diese Verbindungen das Enzym tatsächlich in Reagenzgläsern, und drosseln sie das Wachstum von Brustkrebszellen, ohne gesundes Gewebe zu schädigen? Gelingt das, könnten sie die Entwicklung verbesserter Derivate anleiten oder neue Kombinationstherapien inspirieren, die traditionelle Pflanzenkunde und moderne Molekularwissenschaft verbinden.
Zitation: Al Mashud, M.A., Rahman, M.A., Kumer, A. et al. Computational identification of Terminalia arjuna phytochemicals as potential 3α-HSD3 inhibitors. Sci Rep 16, 8045 (2026). https://doi.org/10.1038/s41598-026-37558-z
Schlüsselwörter: Brustkrebs Hormone, Terminalia arjuna, natürliche Enzyminhibitoren, computerunterstütztes Wirkstoffdesign, Luteolin Gallussäure