Clear Sky Science · de
Ein Ansatz mit geteilter Biotin‑Ligase enthüllt Proteine, die mit oligomerem Alpha‑Synuclein während der Aggregation assoziiert sind
Warum verklumpte Gehirnproteine wichtig sind
Bei Morbus Parkinson und verwandten Erkrankungen kann ein normalerweise nützliches Gehirnprotein namens Alpha‑Synuclein in klebrige Ablagerungen verklumpen, die als Lewy‑Körper bekannt sind. Diese Ablagerungen treten Jahrzehnte vor den Symptomen auf und sind ein charakteristisches Merkmal bei der Obduktion, doch wir wissen noch nicht, welche anderen Proteine Alpha‑Synuclein dabei helfen, vom harmlosen Zustand in gefährliche Aggregate überzugehen. Diese Studie verwendet ein ausgeklügeltes molekulares „Proximity‑Tag“, um zu kartieren, welche Proteine in der Nähe von Alpha‑Synuclein sitzen, während es sich von Einzelmolekülen zu kleinen Klumpen verändert. Das liefert neue Hinweise darauf, wie die Krankheit beginnt und welche Signalwege man anpeilen könnte, um sie zu verlangsamen oder zu verhindern.
Ein molekulares „Tag“, das Nachbarn sichtbar macht
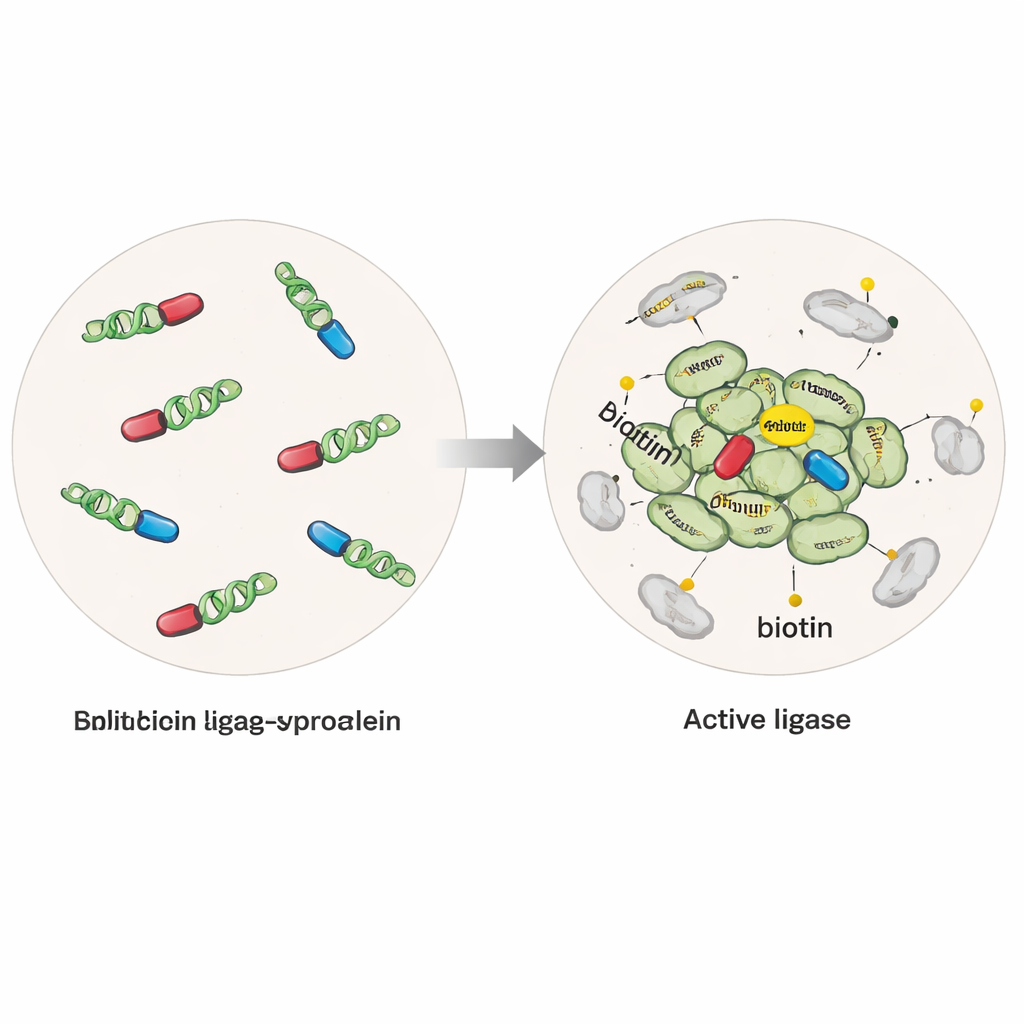
Die Forschenden konstruierten menschliche Zellen so, dass sie Alpha‑Synuclein mit einer modifizierten Enzymkomponente exprimieren, die ein kleines Biotin‑Tag an jedes Protein in einem Abstand von wenigen Nanometern anfügen kann. In einer Variante war das Enzym intakt und aktiv, wann immer Alpha‑Synuclein vorhanden war, und erfasste Proteine in der Nähe sowohl einzelner Moleküle als auch von Klumpen. In einer zweiten, selektiveren „geteilten“ Version wurde das Enzym in zwei inaktive Hälften geschnitten, von denen jede an ein separates Alpha‑Synuclein‑Molekül gekoppelt war. Nur wenn Alpha‑Synuclein‑Moleküle zu Multimeren oder Oligomeren zusammenkamen, vereinten sich die Hälften zu einem aktiven Enzym und schalteten das Tagging gezielt rund um diese frühen Aggregate ein. Durch Zugabe gereinigter Alpha‑Synuclein‑Fibrillen zu den Zellen konnte das Team außerdem krankheitsähnliche Aggregation antreiben und normale gegen pathologische Zustände vergleichen.
Eine Karte der umliegenden Proteine erstellen
Nach ausreichender Zeit für das Tagging isolierte das Team alle biotinmarkierten Proteine und identifizierte sie mittels Massenspektrometrie, einer Technik, die Proteine hochpräzise wägt und zählt. Über alle Versuchsbedingungen hinweg fanden sie 1.277 verschiedene Proteine; nach sorgfältiger Filterung reduzierte sich die Zahl auf 581 Proteine, die wahrscheinlich tatsächlich in der Nähe von Alpha‑Synuclein lagen. Durch den Vergleich des intakten und des geteilten Enzymsystems konnten sie Proteine unterscheiden, die hauptsächlich mit Einzelmolekülen assoziieren, von solchen, die Multimere bevorzugen. Ebenso verglichen sie Zellen mit und ohne zugefügte Fibrillen, um zu sehen, wie sich die lokale Proteinumgebung von Alpha‑Synuclein verändert, sobald die Aggregation ausgelöst ist.
Wichtige zelluläre Wege in den Klumpen
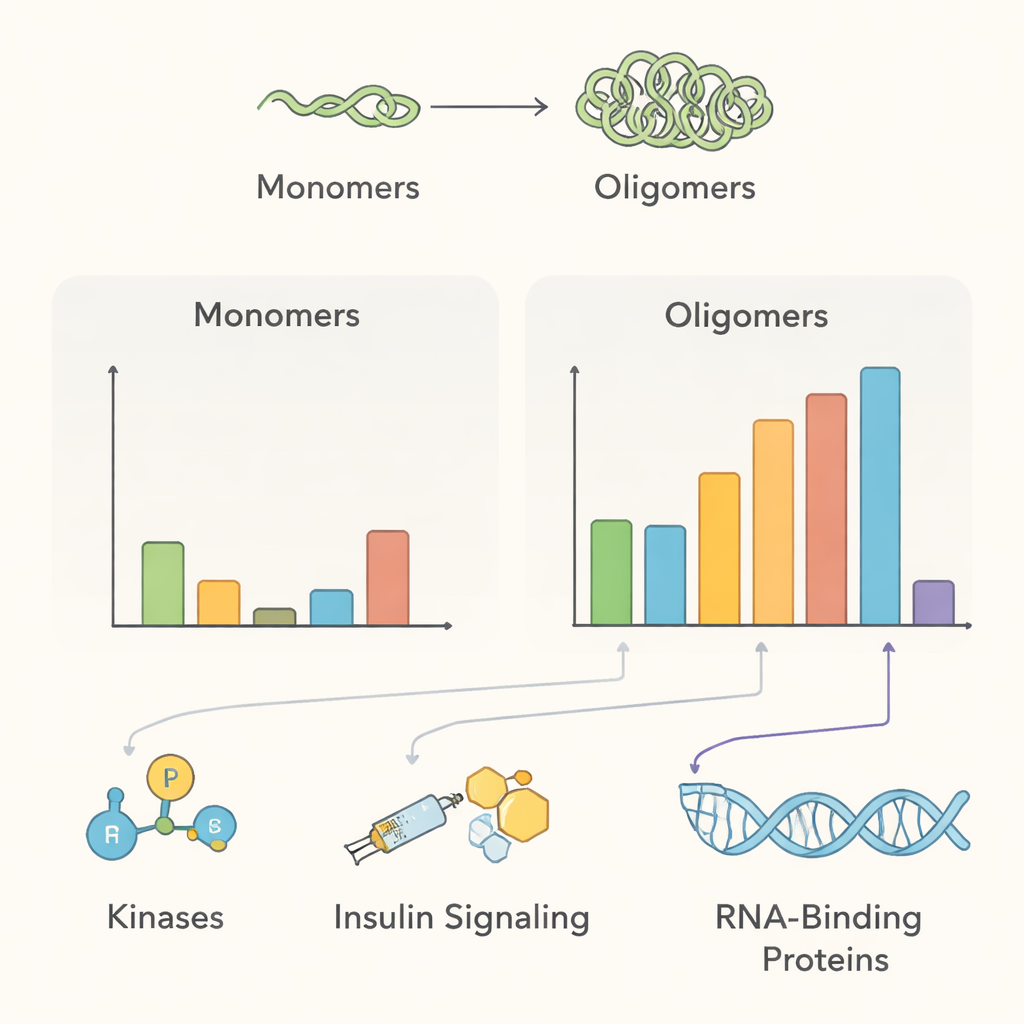
Die resultierende Interaktom‑Skizze weist auf mehrere zentrale biologische Themen hin. Unter normalen Bedingungen lagen multimeres Alpha‑Synuclein in der Nähe zahlreicher Membran‑Trafficking‑Proteine und Protein‑modifizierender Enzyme—im Einklang mit seiner vorgeschlagenen Rolle bei der Regulation synaptischer Vesikel und der Aufrechterhaltung der Proteinqualitätskontrolle in Nervenzellen. Mehrere Enzyme, die Phosphatgruppen hinzufügen, darunter die Kinasen PAK4, RIPK2 und MAP4K4, waren bei gesunden Multimeren angereichert, schienen aber den Kontakt zu verlieren, sobald Aggregate entstanden—ein Hinweis darauf, dass die Störung dieser Beziehungen krankheitsfördernde Formen des Proteins begünstigen könnte. Das Team entdeckte zudem Proteine, die mit dem Insulin‑ähnlichen Wachstumsfaktor‑Signalweg verknüpft sind, was klinische Zusammenhänge zwischen Insulinresistenz und Parkinson‑Erkrankung stützt, und fand, dass die Aggregation Proteine rekrutiert, die an der Entsorgung beschädigter Proteine beteiligt sind, wie die Chaperon‑Familie 14‑3‑3 und spezifische Komponenten zellulärer Abbauwege.
Unerwartete Brücken zu anderen Hirnerkrankungen
Über Morbus Parkinson hinaus heben die Daten eine überraschende Verbindung zu amyotropher Lateralsklerose (ALS) und frontotemporaler Demenz (FTD) hervor. Ein RNA‑bindendes Protein namens FUS, das sich bei diesen Erkrankungen fehllokalisiert und aggregiert, tauchte sowohl unter normalen als auch unter aggregationsfördernden Bedingungen in der Nähe von multimerem Alpha‑Synuclein auf. Auch andere RNA‑bezogene Proteine veränderten ihre Nähe, als Alpha‑Synuclein aggregierte. Diese Befunde legen die Möglichkeit nahe, dass kleine Alpha‑Synuclein‑Assemblies RNA‑verarbeitende Proteine an falsche Orte in der Zelle binden und damit die Biologie der Lewy‑Körper‑Erkrankungen mit der von ALS und FTD verknüpfen könnten, auch wenn direkte physische Wechselwirkungen noch bestätigt werden müssen.
Was das für das Verständnis der Krankheit bedeutet
Für Nicht‑Spezialisten ist die wichtigste Schlussfolgerung, dass diese Arbeit eine frühe „Kontaktliste“ von Proteinen liefert, die mit Alpha‑Synuclein reisen, während es sich vom normalen Helfer zum schädlichen Klumpen wandelt. Die Studie legt nahe, dass der Verlust bestimmter schützender Beziehungen—etwa zu spezifischen Kinasen oder Qualitätskontroll‑Enzymen—ebenso wichtig sein kann wie das Hinzukommen neuer toxischer Partner. Zwar wurden die Experimente in einem vereinfachten Zellmodell durchgeführt und liefern noch keinen Beweis für Ursache und Wirkung, doch sie heben konkrete Kandidaten und Signalwege hervor, die in Neuronen und Hirngewebe weiter untersucht werden sollten. Langfristig könnte das Kartieren dieser wechselnden Protein‑Nachbarschaften Strategien leiten, schützende Interaktionen wiederherzustellen, insulinbezogene Signalwege zu unterstützen oder das Einfangen von RNA‑bindenden Proteinen zu verhindern—und so möglicherweise den Übergang von subtilen molekularen Veränderungen zu voll ausgeprägten Lewy‑Körper‑Erkrankungen zu verlangsamen.
Zitation: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Schlüsselwörter: alpha‑Synuclein, Lewy‑Körper‑Erkrankung, Proteinaggregation, Proximity‑Proteomik, Morbus Parkinson