Clear Sky Science · de
Einblicke in die strukturellen Unterschiede zwischen Homo- und Heterodimeren, angereichert aus einem Cocktail monoklonaler Antikörper gegen SARS-CoV-2
Warum das Mischen von Antikörpern Überraschungen erzeugen kann
Während der COVID-19-Pandemie wurden Antikörper-Arzneimittel wie der REGEN-COV-Cocktail eingesetzt, um das die Krankheit verursachende Virus SARS-CoV-2 zu blockieren. Diese Medikamente sind sorgfältig entworfen, doch sobald sie zusammen in einem Fläschchen vorliegen, können sie seltene Paarbildungen eingehen, sogenannte Heterodimere — zwei unterschiedliche Antikörper, die ein Paar bilden. Die vorliegende Studie stellt eine praxisnahe Frage mit großen Sicherheits- und Wirkungsfolgen: Verhalten sich diese ungewöhnlichen Paare anders als die bekannteren Paare identischer Antikörper, und könnte das die Wirksamkeit des Medikaments verändern?
Ungewöhnliche Paare in einem wirksamen COVID-19-Medikament
REGEN-COV kombiniert zwei monoklonale Antikörper, Casirivimab und Imdevimab, die jeweils so konzipiert sind, dass sie auf unterschiedliche Weise am Spike-Protein von SARS-CoV-2 ansetzen. Wenn beide zusammen formuliert werden, verbinden sich ein sehr kleiner Teil der Antikörper zu Paaren. Einige Paare sind Homodimere (zwei Kopien desselben Antikörpers); andere sind Heterodimere (ein Casirivimab plus ein Imdevimab). Heterodimere gelten als Verunreinigung, weil sie nicht Teil des ursprünglichen Arzneimitteldesigns sind, und ihr Verhalten im Körper war weitgehend unbekannt. Die Autorinnen und Autoren verwendeten zunächst einen mehrstufigen Reinigungsprozess, um mehrere unterschiedliche Homodimerarten sowie das Heterodimer aus derselben REGEN-COV-Charge zu isolieren, wodurch sie eine seltene Gelegenheit erhielten, all diese Assemblierungen Seite an Seite zu vergleichen.
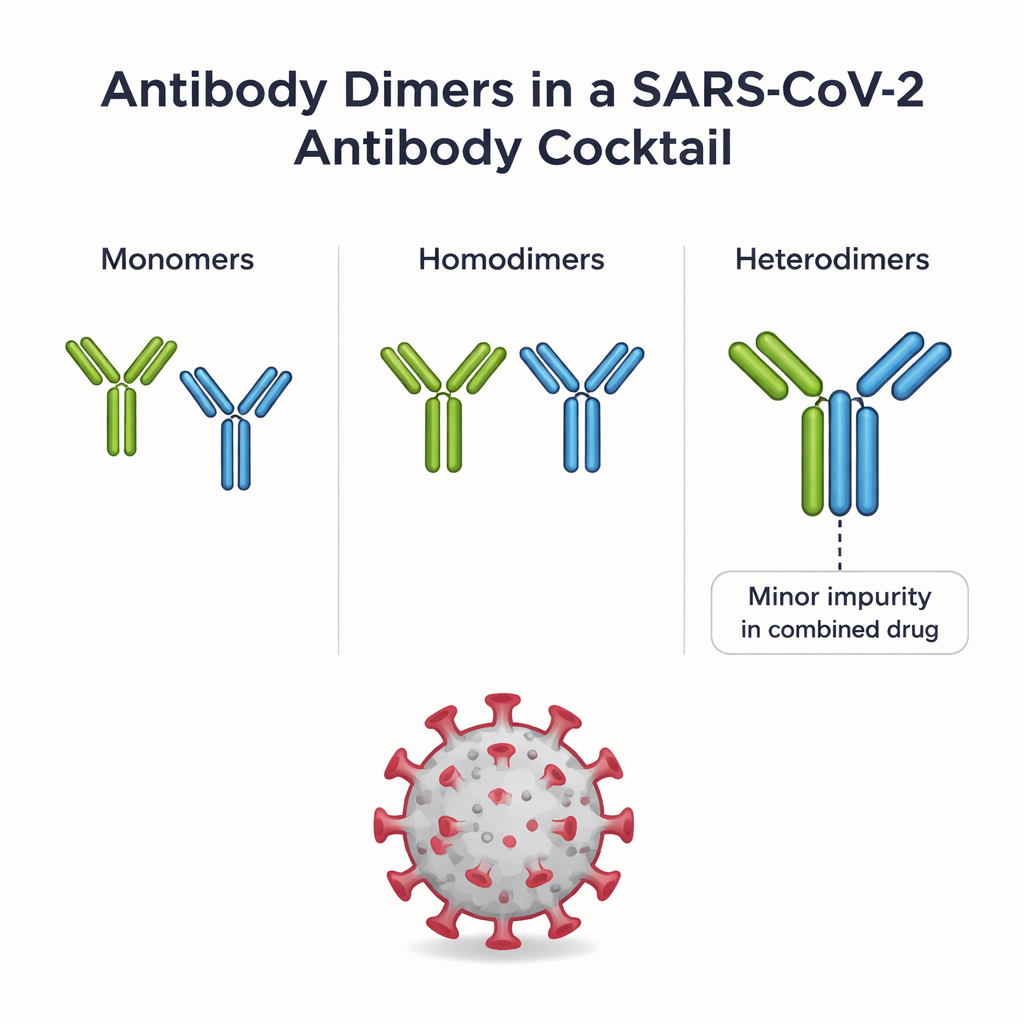
Form, Klebrigkeit und chemische Bindungen erforschen
Um zu verstehen, was jeden Dimertyp einzigartig macht, kombinierte das Team mehrere hochauflösende Analytikmethoden. Chromatographie-Experimente zeigten, wie sich die Dimere in ihrer Oberflächen‑„Klebrigkeit“ (Hydrophobizität) unterscheiden, während Kapillarelektrophorese und eine spezialisierte Form der Massenspektrometrie Aufschluss darüber gaben, ob die beiden Antikörper in einem Dimer durch schwache Anziehungskräfte oder durch stärkere kovalente Bindungen zusammengehalten werden. Elektronenmikroskopie und analytische Ultrazentrifugation lieferten anschließend Einblicke in die Gesamtgestalt — ob ein Dimer gestreckt und flexibel oder kompakt und dicht gepackt ist. Zusammengenommen zeigten diese Methoden, dass Casirivimab und Imdevimab mehrere unterschiedliche Homodimere mit verschiedenen Formen und Bindungsmustern bilden und dass das Heterodimer besonders kompakt ist und reich an kovalenten Verknüpfungen in unterschiedlichen Bereichen der Antikörperarme und -stämme.
Wie Struktur mit Virusblockade und Zelltötung zusammenhängt
Die Forschenden fragten anschließend, wie sich diese strukturellen Unterschiede auf das auswirken, was wirklich zählt: das Virus zu stoppen und das Immunsystem einzubinden. Sie testeten jedes Dimer in einem Pseudovirus-Neutralisationsassay, der misst, wie gut die Antikörper das Eindringen eines virusähnlichen Partikels verhindern, und in einem Antikörper-abhängigen zellulären Zytotoxizitätsassay (ADCC), der beurteilt, wie effektiv Antikörper Immunzellen rekrutieren, um infizierte Zielzellen zu zerstören. Überraschenderweise waren die meisten Dimere mindestens so wirksam wie — und teils besser als — ihre einzelnen Monomer‑Gegenstücke bei der Neutralisation des Virus. Insbesondere zeigten Imdevimab-Homodimere eine „hyperpotente“ Neutralisation, vermutlich weil ihre Geometrie ihnen erlaubt, mehrere Spike‑Proteine auf der Virushülle zu überbrücken. Einige Casirivimab-Homodimere erzeugten besonders starke ADCC‑Signale, offenbar weil ihre Orientierung die Schwanzregionen (die Fc‑Teile) gut für Rezeptoren von Immunzellen freilegt.
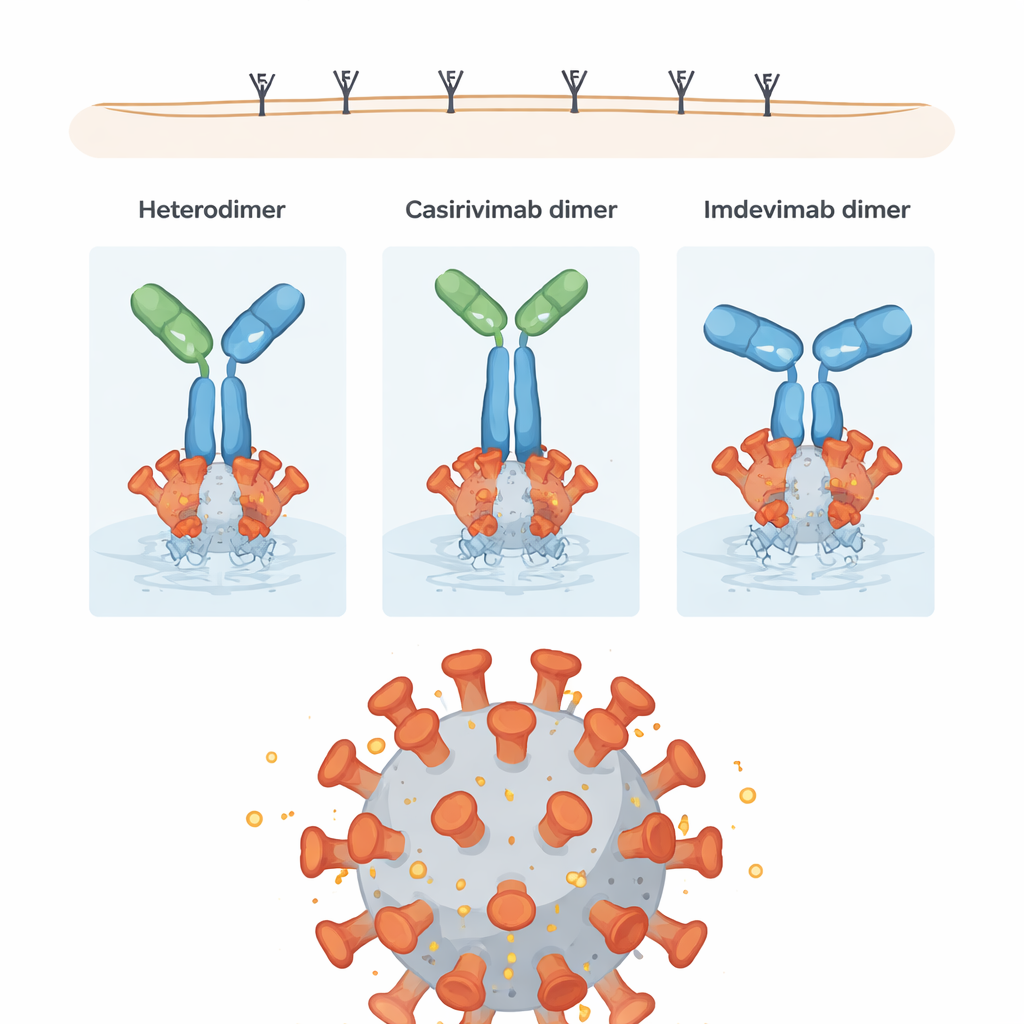
Eine kompakte Verunreinigung mit gemischter Leistung
Das Heterodimer, obwohl reich an starken, kompakten Verbindungen zwischen seinen zwei unterschiedlichen Antikörpern, zeigte eine etwas reduzierte Leistung: etwa 70 % der Neutralisations‑ und ADCC‑Aktivität der vorgesehenen koformulierten Mischung. Die umfangreiche Vernetzung zwischen seinen Armen und Stämmen scheint die freie Rotation und Neuorientierung des Moleküls beim Binden an den Virus‑Spike einzuschränken, was wiederum sowohl die Blockade des Virus als auch die Signalübermittlung an Immunzellen begrenzen kann. Viele seiner Bindungen sind jedoch vom Typ, der sich unter physiologischen Bedingungen langsam lösen kann, wodurch das Heterodimer über die Zeit relativ instabil ist und dazu neigt, wieder in Einzelantikörper zurückzufallen.
Was das für Antikörpermedikamente bedeutet
Für Patientinnen und Patienten sowie Arzneimittelentwickler ist die Kernaussage beruhigend, aber nuanciert. Dieser tiefgehende Blick auf REGEN‑COV‑Dimere legt nahe, dass die meisten dimerischen Formen, einschließlich der ungewöhnlichen Heterodimer‑Verunreinigung, erhebliche antivirale Aktivität behalten, und es gibt kein eindeutiges Anzeichen für ein zusätzliches Sicherheitsrisiko durch höhergradige Aggregate in diesem System. Gleichzeitig zeigt die Arbeit, dass feine Details — wo Antikörper sich berühren, wie eng sie quervernetzt sind und ob sie kompakt oder langgestreckt sind — die Potenz merklich verschieben können. Die Autorinnen und Autoren argumentieren, dass ähnliche strukturelle und funktionelle Profile von Dimeren in anderen Antikörperwirkstoffen zu einem leistungsfähigen nicht‑klinischen Instrument werden könnten, um Verunreinigungen zu verstehen und zu steuern, und dass dies möglicherweise sogar zur gezielten Entwicklung multimerer Antikörper inspirieren könnte, die Geometrie nutzen, um Viren besser anzugreifen und zu neutralisieren.
Zitation: Nguyen, J.B., Liu, S., Yan, Y. et al. Insights into the structural differences between homo- and heterodimers enriched from a cocktail of monoclonal antibodies against SARS-CoV-2. Sci Rep 16, 7024 (2026). https://doi.org/10.1038/s41598-026-37545-4
Schlüsselwörter: Antikörper-Dimere, REGEN-COV, SARS-CoV-2-Spike, Cocktails monoklonaler Antikörper, Proteinaggregate