Clear Sky Science · de
Kovalente Immobilisierung von Lepidium draba‑Peroxidase auf chitosanbeschichteten magnetischen Nanopartikeln und ihre Anwendung in der Glukosebiosensorik
Warum winzige Magnete für den Blutzucker wichtig sind
Die Kontrolle des Blutzuckers ist entscheidend für das Management von Diabetes und die Vermeidung langfristiger Schäden am Herz, an den Nieren, den Augen und Nerven. Heutige Glukosetests funktionieren gut, doch die darin verwendeten Enzyme können empfindlich, kurzlebig und schwer wiederverwendbar sein, was Kosten und Abfall erhöht. Diese Studie untersucht einen eleganten Ansatz, ein Pflanzenenzym robuster und langlebiger zu machen, indem man es an mikroskopisch kleine magnetische Kügelchen befestigt — ein Weg zu schnelleren, zuverlässigeren und potenziell günstigeren Glukosetests.
Eine pflanzliche Hilfe, inspiriert von Meerrettich
Viele medizinische Tests beruhen auf Enzymen — Proteinen, die chemische Reaktionen beschleunigen. Ein Arbeitstier in diagnostischen Laboren ist die Meerrettichperoxidase, die unsichtbare chemische Veränderungen in deutlich sichtbare Farbwechsel umwandelt. Die Forschenden arbeiteten mit einem nahen pflanzlichen Verwandten dieses Enzyms, der Lepidium draba‑Peroxidase, die in Bakterien produziert wurde, sodass sie in großen Mengen hergestellt werden kann. Allein ist dieses freie Enzym zwar wirksam, aber empfindlich: Es verliert Aktivität durch Wärme, Lagerung und wiederholte Nutzung, was seinen Wert für industrielle Sensoren und klinische Kits einschränkt.
Enzyme in magnetische Werkzeuge verwandeln
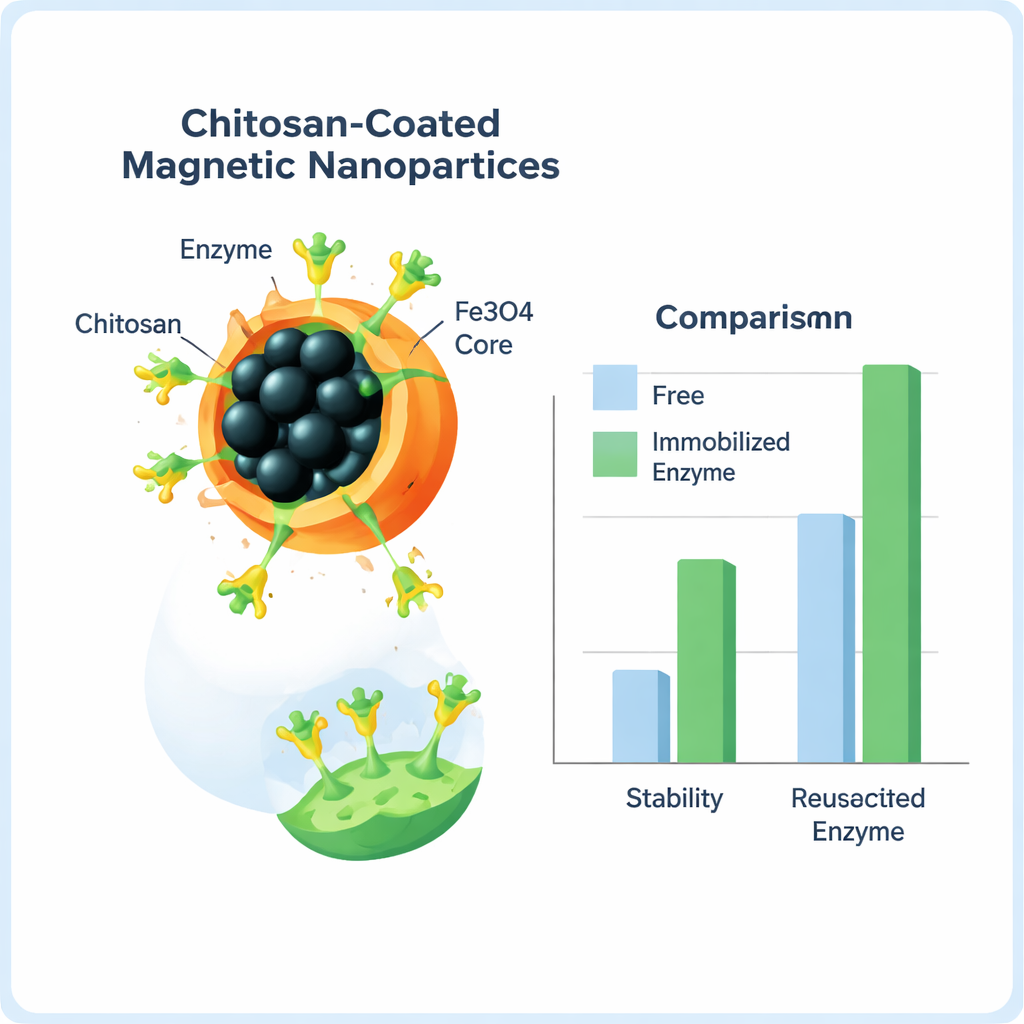
Um das Enzym zu schützen und wiederzuverwenden, befestigte das Team es an Eisenoxid‑Nanopartikeln — winzigen Körnchen magnetischen Materials —, die mit einem natürlichen Polymer namens Chitosan beschichtet sind, das aus Schalentierabfällen gewonnen wird. Chitosan bietet eine weiche, biokompatible Schicht mit vielen chemischen „Handgriffen“, an denen Enzyme anhaften können. Mithilfe eines kleinen Vernetzungsmoleküls, Glutaraldehyd, bildeten sie starke kovalente Bindungen zwischen dem Enzym und den beschichteten Partikeln. Die Forschenden optimierten dann die Menge des Vernetzers, die Reaktionsdauer und die Menge des Trägermaterials und fanden Bedingungen, die das beste Gleichgewicht zwischen gebundener Enzymmenge und verbleibender Aktivität lieferten.
Struktur, Stabilität und Haltbarkeit prüfen
Nach der Immobilisierung bestätigte das Team mit mehreren strukturellen Methoden, dass das Enzym tatsächlich an den Partikeln sitzt, indem sie Bindungsschwingungen, Kristallmuster und Oberflächenformen analysierten. Wichtiger für den praktischen Einsatz war, dass sich das immobilisierte Enzym besser verhielt als seine freie Form. Es zeigte eine höhere Affinität zu seinem Farbstoffsubstrat und wandelte dieses deutlich effizienter in das gefärbte Produkt um — in einigen Tests bis zu elffach höhere katalytische Effizienz. Das gebundene Enzym tolerierte außerdem ein breiteres pH‑Spektrum, behielt bei nützlichen Temperaturen eine höhere Aktivität und widerstand längerer Erwärmung bei 50 °C. Seine Halbwertszeit bei dieser Temperatur verdoppelte sich mehr als, und nach zwei Monaten im Kühlschrank behielt es etwa doppelt so viel Aktivität wie das freie Enzym. Da die Partikel magnetisch sind, ließen sie sich mit einem Magneten aus der Lösung herausziehen und wiederverwenden; selbst nach 11 Reaktionszyklen blieb noch etwa 40 % der ursprünglichen Aktivität erhalten.
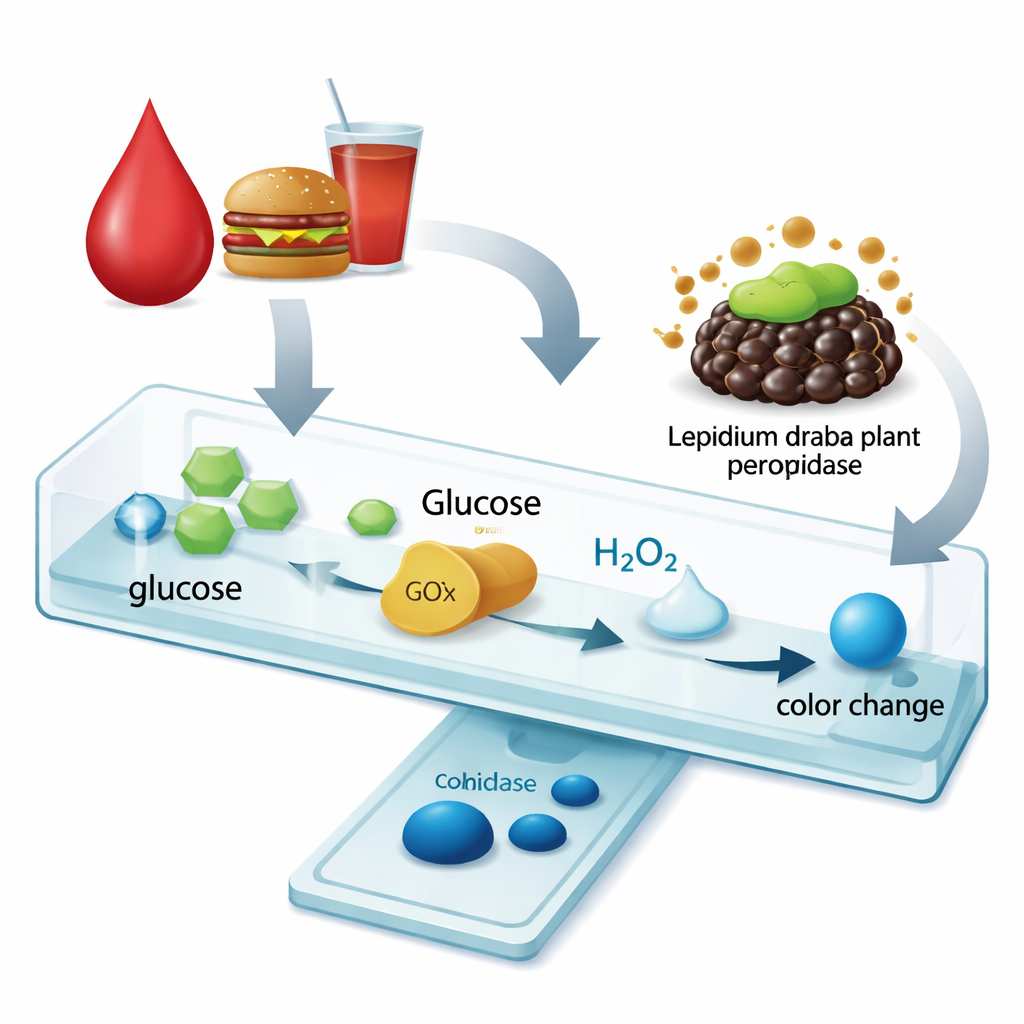
Deutlichere Farbänderung für Glukosetests
Um zu prüfen, ob dieses stabilere Enzym einen praktischen Test tatsächlich verbessert, bauten die Forschenden einen einfachen colorimetrischen Glukosetest. Zuerst wandelt ein übliches Glukoseoxidase‑Enzym Glukose in Wasserstoffperoxid um. Dann nutzt die Lepidium draba‑Peroxidase, entweder frei oder immobilisiert auf den magnetischen Chitosan‑Beads, dieses Wasserstoffperoxid, um einen farblosen Farbstoff tiefblau zu färben. Bei der immobilisierten Form erweiterte sich der nutzbare Messbereich für Glukose dramatisch — von 0,1–1 Millimol pro Liter mit dem freien Enzym auf 0,1–10 Millimol pro Liter beim immobilisierten Enzym. Gleichzeitig verringerte sich die für den Test benötigte Reaktionszeit auf etwa ein Drittel, während die minimal nachweisbare Glukosekonzentration sehr niedrig und weiterhin klinisch relevant blieb.
Was das für die tägliche Gesundheit bedeutet
Indem sie ein Pflanzenenzym an chitosanbeschichtete magnetische Nanopartikel ankerten, schufen die Autorinnen und Autoren eine robuste, wiederverwendbare und hochempfindliche Komponente für colorimetrische Glukosesensoren. Für Laien bedeutet das, dass zukünftige Teststreifen, Laborkits oder sogar clevere Verpackungen für Lebensmittel stabiler, über einen größeren Zuckerspektrum genauer und potenziell günstiger werden könnten, weil das aktive Enzym zurückgewonnen und erneut verwendet werden kann. Zwar sind weitere Arbeiten nötig, um die Enzymbeladung der Partikel zu erhöhen und den Ansatz auf andere Blutmarker wie Cholesterin oder Harnstoff auszuweiten, doch die Studie zeigt, wie Nanomaterialien und natürliche Polymere zusammenarbeiten können, um vertraute biochemische Werkzeuge robuster, sauberer und vielseitiger zu machen.
Zitation: Sepahi-Baghan, M., Asoodeh, A. & Riahi-Madvar, A. Covalent immobilization of Lepidium draba peroxidase on chitosan-coated magnetic nanoparticles and its application in glucose biosensing. Sci Rep 16, 7035 (2026). https://doi.org/10.1038/s41598-026-37542-7
Schlüsselwörter: Glukosebiosensor, Enzymimmobilisierung, magnetische Nanopartikel, colorimetrische Detektion, Peroxidase