Clear Sky Science · de
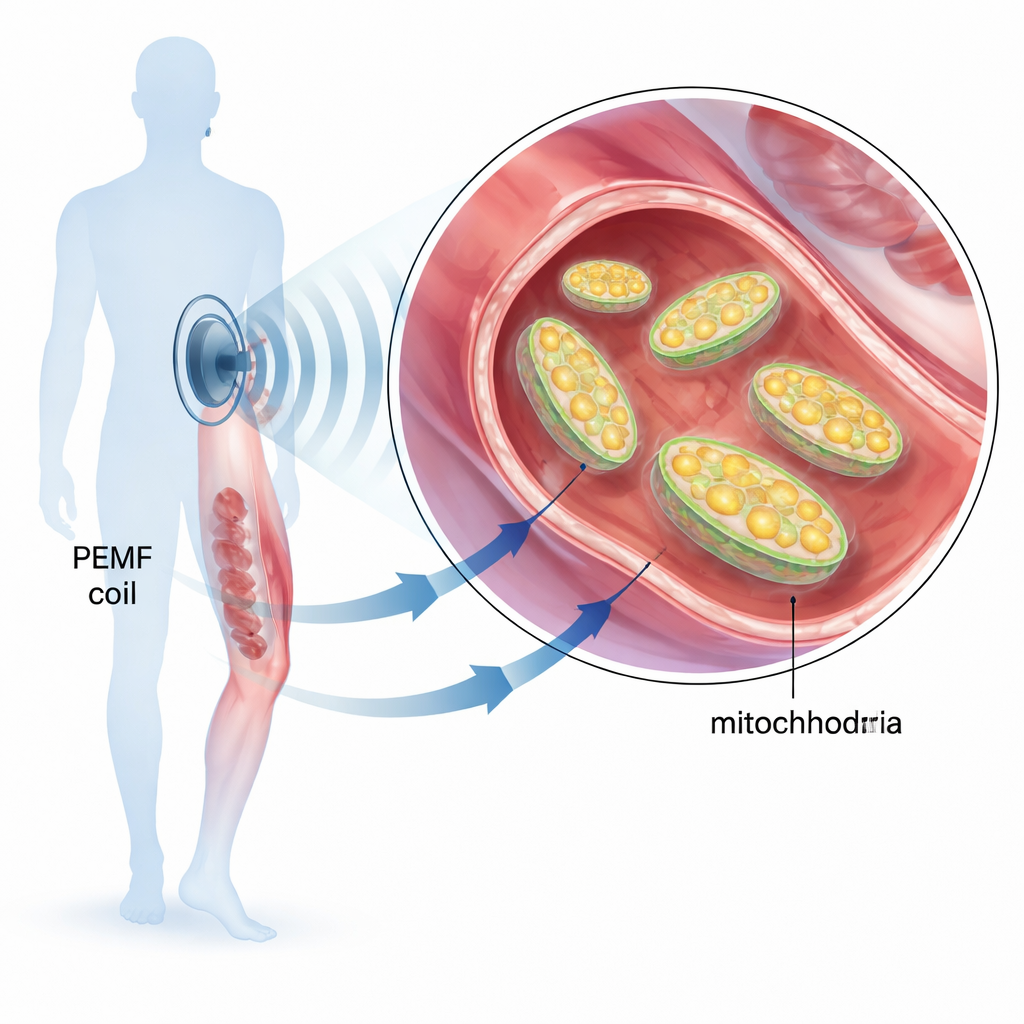
Wechselwirkung gepulster niederfrequenter elektromagnetischer Felder (PEMF) mit Mitochondrien
Sanfte Felder und die Kraftwerke der Zelle
Die gepulste elektromagnetfeldtherapie (PEMF) wird bereits klinisch eingesetzt, um gebrochene Knochen zu unterstützen, Gelenkschmerzen zu lindern und die Erholung nach Operationen zu beschleunigen. Dennoch verstehen wir noch nicht vollständig, wie diese sanften, niederfrequenten Felder im Körper wirken. Diese Studie stellt eine grundlegende, aber wichtige Frage: Beeinflussen PEMF‑Signale direkt die Mitochondrien, die winzigen Kraftwerke in unseren Zellen, die den Großteil unserer Energie erzeugen — und wenn ja, wie?
Warum Mitochondrien für die alltägliche Gesundheit wichtig sind
Mitochondrien wandeln Nahrung und Sauerstoff in das Molekül ATP um, die universelle „Energieeinheit“ der Zellen. Wenn Mitochondrien versagen, heilen Gewebe langsamer, Muskeln ermüden schneller und Krankheiten, die mit gestörtem Stoffwechsel verbunden sind, können sich verschlechtern. Da frühere Untersuchungen darauf hingedeutet haben, dass PEMF‑Behandlungen den Energiestoffwechsel verbessern und die Gewebereparatur unterstützen, konzentrierten sich die Autoren darauf, ob ein spezifisches PEMF‑Gerät die mitochondriale Aktivität feinjustieren kann. Sie verwendeten ein gut definiertes Magnetsignal: kurze, millisekundenlange Pulse einer 30‑kHz‑Sinuswelle mit geringer Eingangsenergie, angewendet auf Muskelzellen in Kultur, auf Rattengewebe und auf gereinigte Mitochondrien.
Ein genauerer Blick in lebende Zellen
In im Labor gezüchteten menschlichen Muskelzellen maßen die Forscher drei zentrale Indikatoren nach PEMF‑Exposition: das elektrische Potenzial über der inneren mitochondrialen Membran (eine Art winzige Batterie), die Mengen reaktiver Sauerstoffspezies (hohe Werte können schädlich sein) und Nitricoxid, ein Gas, das die mitochondriale Atmung vorübergehend blockieren kann. Etwa 90 Minuten nach der Behandlung war das mitochondriale Membranpotenzial leicht erniedrigt, während die Nitricoxidwerte reduziert waren; reaktive Sauerstoffspezies nahmen nicht zu. Ein kleiner Abfall des Membranpotenzials kann entweder auf Schäden oder auf eine gesteigerte ATP‑Produktion hinweisen. Da die Zellen keine Stressanzeichen zeigten, vermuteten die Autoren, dass die Mitochondrien schlichtweg etwas schneller arbeiteten und die über die innere Membran gespeicherte Spannung verbrauchten.
Prüfung, wie Mitochondrien „atmen“
Um diese Idee direkter zu testen, perforierten die Forscher die äußere Zellmembran vorsichtig, sodass sie den Mitochondrien gezielt unterschiedliche Brennstoffe zugeben und den Sauerstoffverbrauch genau messen konnten. Sie beobachteten konsistent einen Trend zu höherer Atmung, die mit ATP‑Produktion verbunden ist, nach PEMF‑Behandlung, insbesondere wenn Glutamat, ein häufiger mitochondrialer Brennstoff, vorhanden war. Statistische Analysen über viele Proben hinweg deuteten darauf hin, dass die Kombination aus PEMF‑Exposition und der Wahl des Brennstoffs signifikant beeinflusste, wie schnell Mitochondrien Sauerstoff verbrauchten. Wichtig ist, dass es keinen Hinweis darauf gab, dass PEMF die Zellen oder ihre Mitochondrien schädigte. Stattdessen schienen die Felder selektiv den „gekoppelten“ Atmungsmodus zu stimulieren, bei dem der Sauerstoffverbrauch eng mit der ATP‑Bildung verknüpft ist, ohne die verschwendete, entkoppelte Verbrennung von Brennstoff zu steigern.
Entzündung, Nitricoxid und eine Überraschung durch blaues Licht
Weil Nitricoxid sich bei Entzündungen ansammeln und einen wichtigen Schritt der mitochondrialen Atmung blockieren kann, prüfte das Team, ob PEMF Mitochondrien helfen könnte, sich von einer solchen Hemmung zu erholen. Sie fügten einen chemischen Nitricoxidspender zu Muskel‑ und Lebergewebehomogenaten sowie zu isolierten Lebermitochondrien hinzu, was die Atmung stark verlangsamte. Unter diesen Bedingungen stellte PEMF die mitochondriale Funktion nicht wieder her, selbst wenn die Mitochondrien hochkonzentriert waren. Um zu testen, ob die Blockade überhaupt reversibel war, bestrahlten sie die nitrosyl‑hemmten Mitochondrien mit blauem Licht, mittels einer Methode, die bekanntlich Nitricoxid von seiner Bindungsstelle lösen kann. Blaues Licht rettete die Atmung teilweise, was bestätigte, dass das System sich erholen kann — aber PEMF brachte keinen zusätzlichen Vorteil. Das zeigte, dass die positiven Effekte von PEMF nicht darauf beruhen, Nitricoxid unter entzündungsähnlichen Bedingungen zu entfernen.
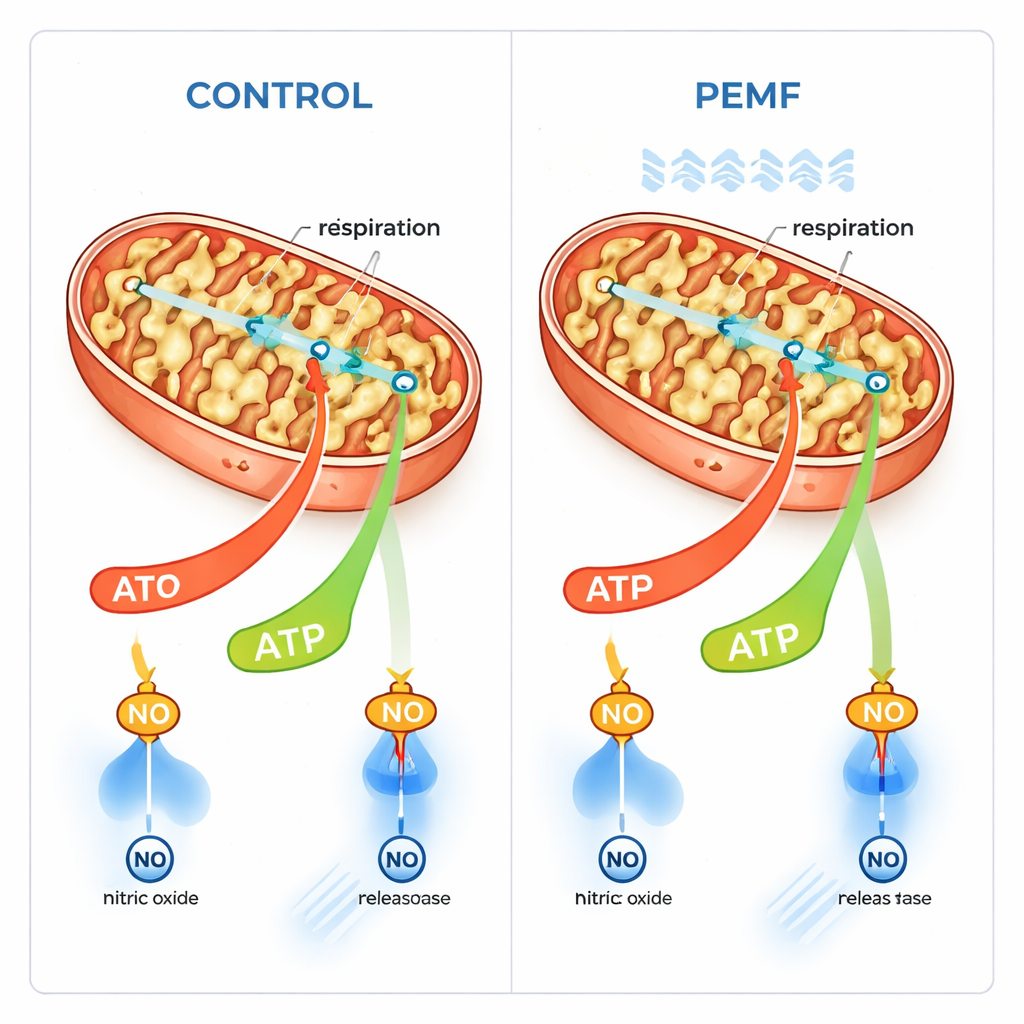
Membranpforten und Energiefluss
Mit einer Analogie zwischen Zellen und elektrischen Schaltkreisen schlagen die Autoren vor, dass PEMF vor allem auf biologische Membranen wirken könnte. Mitochondrien sind von einer äußeren Membran umgeben, die ein wichtiges Torprotein namens VDAC enthält, das energiebezogene Moleküle hinein und heraus passieren lässt. Im Gegensatz zur inneren Membran mit sehr hohem Spannungspotenzial weist die äußere Membran eine kleinere, leichter beeinflussbare Spannung auf. Die Autoren vermuten, dass PEMF dieses äußere Membranpotenzial subtil verändert, wodurch sich die Öffnungsfrequenz der VDAC‑Tore verschiebt und damit der Fluss von Brennstoff und verbrauchtem ATP über die Membran erleichtert wird. Das würde natürlicherweise den gekoppelten, ATP‑produzierenden Atmungsmodus fördern, ohne die maximale Kapazität der Elektronentransportmaschinerie selbst zu verändern.
Was das für zukünftige Therapien bedeutet
Insgesamt liefert die Studie keine Hinweise darauf, dass diese Art von PEMF Mitochondrien schädigt. Im Gegenteil: PEMF verbessert behutsam den Teil der mitochondrialen Atmung, der ATP erzeugt, während die maximale respiratorische Kapazität und der oxidative Stress unverändert bleiben. Allerdings stellt PEMF Mitochondrien, die durch hohes Nitricoxid blockiert sind, nicht wieder her, was darauf hindeutet, dass seine Vorteile in entzündetem Gewebe über andere Wege zustande kommen müssen. Für Patientinnen und Patienten sowie Klinikpersonal stützen diese Ergebnisse die Idee, dass sorgfältig abgestimmte elektromagnetische Felder die Kraftwerke der Zellen in einen effizienteren, energieproduzierenden Zustand lenken können — und liefern eine plausible, mechanistische Erklärung für einige der berichteten Heilungswirkungen bei Knochenreparatur, Wundversorgung und postoperativer Erholung.
Zitation: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
Schlüsselwörter: gepulste elektromagnetfeldtherapie, Mitochondrien, zelluläre Energie, Nitricoxid, ATP-Produktion