Clear Sky Science · de
Cafestol-Derivate als potenzielle FXR-Agonisten und CYP7A1-Inhibitoren und ihre Auswirkungen auf Hypercholesterinämie: eine In-silico-Studie
Warum Ihr Morgenkaffee Ihrem Cholesterin einen Schubs geben könnte
Kaffeeliebhaber hören oft, dass ungefilterte Zubereitungen wie French Press oder gekochter Kaffee das Cholesterin erhöhen können, doch die Gründe bleiben meist im technischen Jargon verborgen. Diese Studie geht der Chemie hinter dieser Warnung nach. Sie untersucht nicht nur Cafestol – einen natürlichen Stoff im Kaffee, der bereits dafür bekannt ist, Cholesterin zu erhöhen – sondern auch, was mit Cafestol passiert, wenn Kaffeebohnen geröstet werden und wenn der Körper es zu metabolisieren beginnt. Mithilfe leistungsfähiger Computersimulationen stellen die Forschenden eine einfache, praxisnahe Frage: Könnten diese verwandten Verbindungen ebenfalls stillschweigend den Cholesterinspiegel anheben?
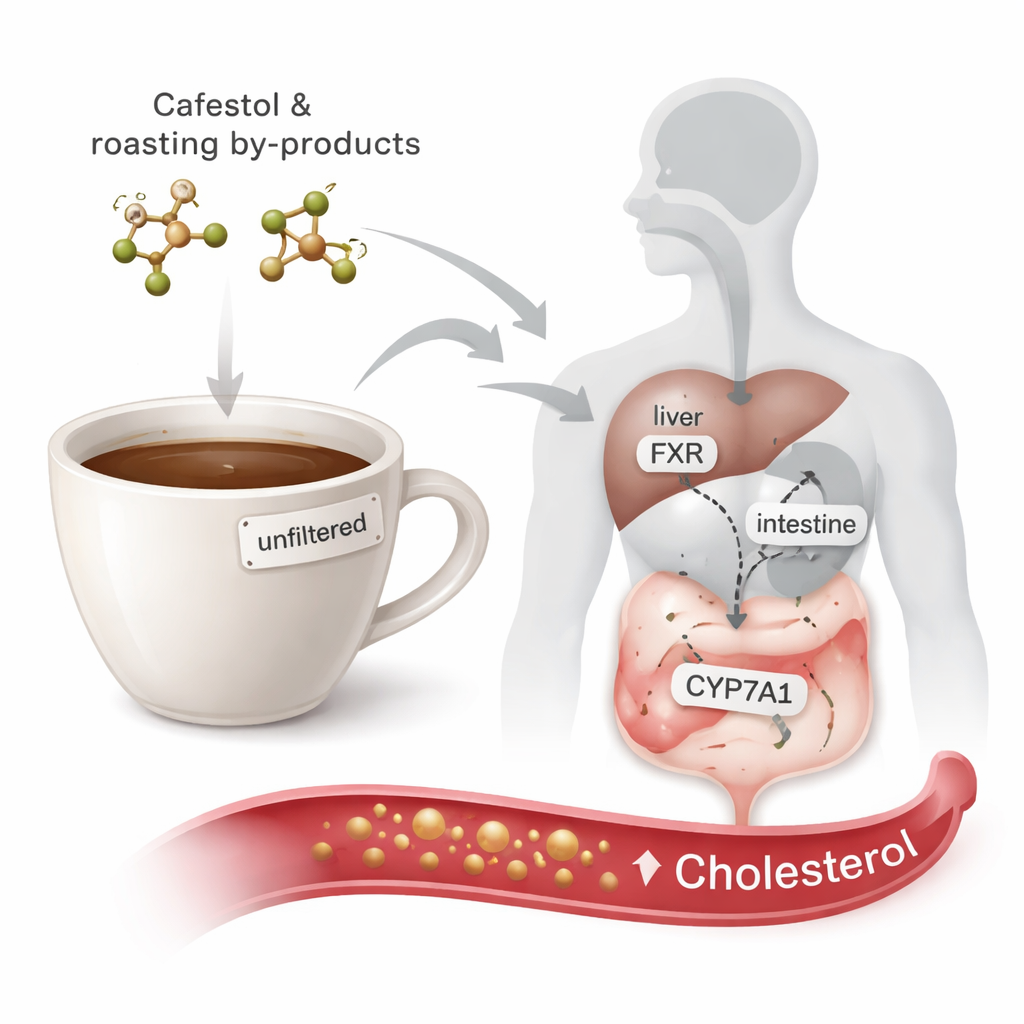
Kaffeeöle und die Cholesterinfrage
Cafestol ist ein fettsubstanzähnliches Molekül, das im öligeren Anteil der Kaffeebohne vorkommt, besonders in ungefilterten Kaffeegetränken. Während Cafestol in Laborstudien mit einigen potenziellen gesundheitlichen Vorteilen in Verbindung gebracht wurde, etwa anti-krebs- und anti-diabetischen Effekten, haben Humanstudien konstant gezeigt, dass es das Blutcholesterin erhöhen kann. Schon 10 Milligramm pro Tag über einige Wochen reichen aus, um bei Versuchspersonen messbar das Cholesterin anzuheben. Röst- und Brühmethoden spielen eine Rolle: Espresso, Mokka, French Press und gekochter Kaffee behalten mehr dieser öligen Verbindungen als papiergefilterter Kaffee. Bislang war jedoch kaum bekannt, ob die Röstprodukte und frühen Metaboliten von Cafestol ebenfalls das Potenzial haben, das Cholesterin anzuheben.
Zwei molekulare Schalter, die das Cholesterin steuern
Die Arbeit konzentriert sich auf zwei Schlüsselproteine, die steuern, wie der Körper mit Cholesterin umgeht: den Farnesoid-X-Rezeptor (FXR) und ein Enzym namens CYP7A1. FXR fungiert als Sensor für Gallensäuren – Verbindungen, die in der Leber aus Cholesterin gebildet werden – und hilft, sowohl die Gallensäureproduktion als auch das Fettgleichgewicht zu regulieren. Wenn FXR aktiviert wird, sendet es Signale, die letztlich die Aktivität von CYP7A1 verringern können. CYP7A1 wiederum führt den ersten und geschwindigkeitsbestimmenden Schritt bei der Umwandlung von Cholesterin in Gallensäuren zur Ausscheidung aus. Wird FXR überaktiviert oder CYP7A1 direkt gehemmt, kann der Körper weniger Cholesterin in Gallensäuren umwandeln, was potenziell zu höheren zirkulierenden Cholesterinwerten führt. Von Cafestol ist bereits bekannt, dass es auf diese Schalter wirkt, doch das Verhalten seiner Röstprodukte und frühen Metaboliten war bislang nicht kartiert.
Testen von Kaffeeverbindungen im virtuellen Labor
Da viele dieser Cafestol-ähnlichen Moleküle schwer zu isolieren und experimentell zu testen sind, wandte sich das Team In-silico-Methoden zu – computerbasierten Experimenten. Sie bauten dreidimensionale Modelle des menschlichen FXR und CYP7A1 und simulierten dann, wie Cafestol, seine Röstderivate und seine Phase-I-Metaboliten in diese Proteine passen könnten, ähnlich wie verschiedene Schlüssel in ein Schloss ausprobiert werden. Dazu gehörten molekulares Docking, das vorhersagt, wie fest und in welcher Orientierung jedes Molekül binden kann, sowie molekulardynamische Simulationen, die beobachten, wie diese Komplexe in einer virtuellen wässrigen Umgebung „wackeln“ und sich über die Zeit stabilisieren. Außerdem erstellten sie Pharmakophor-Modelle, abstrakte Muster, die hervorheben, welche Merkmale – etwa ölige Regionen und Wasserstoffbrückenbindungsgruppen – für die Bindung am wichtigsten sind, und führten Absorptions- und Metabolismusvorhersagen durch, um abzuschätzen, wie sich die Röstprodukte im Körper verhalten könnten.
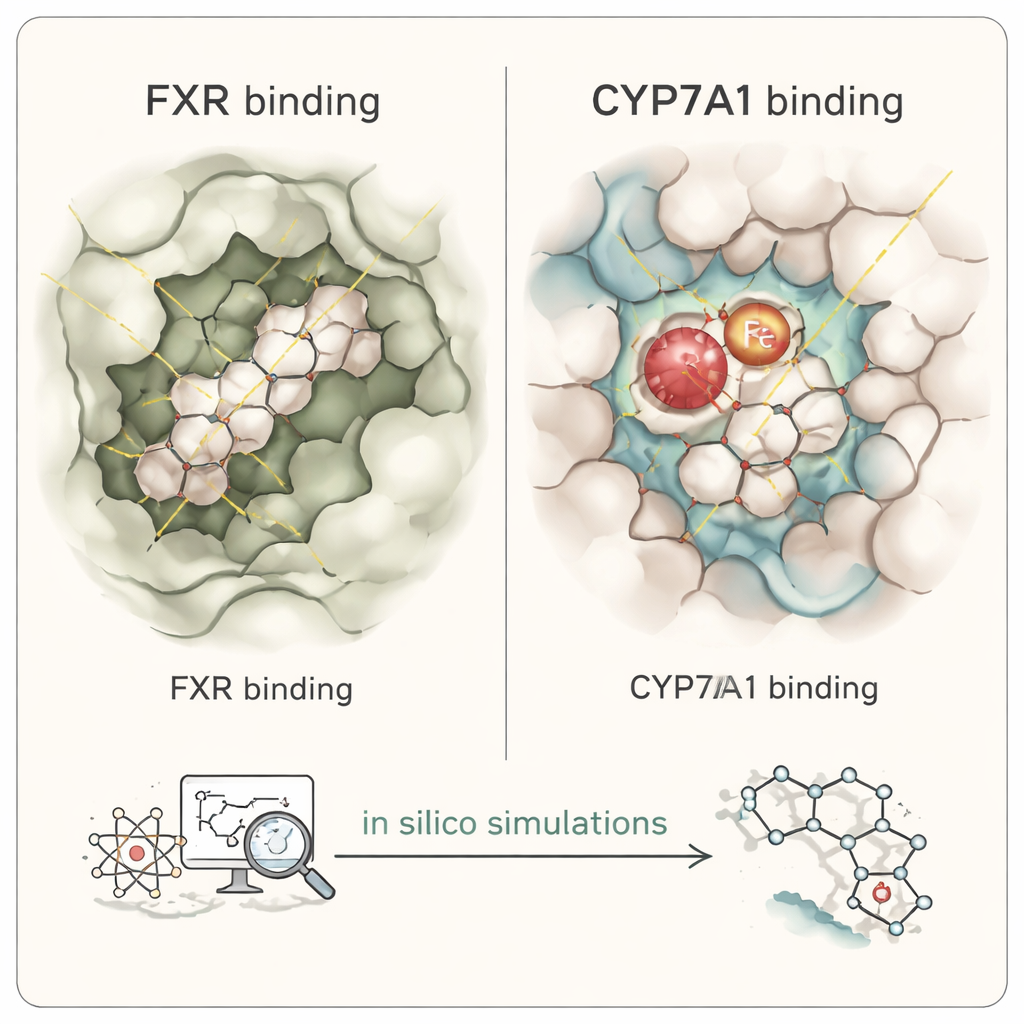
Röstprodukte, die weiterhin problematisch erscheinen
Die Simulationen deuten darauf hin, dass mehrere während des Röstens gebildete Cafestol-Derivate sowie einige frühe Abbauprodukte, die in einem Zebrafischmodell gefunden wurden, sich an FXR und CYP7A1 anlagern können, und zwar in einer Weise, die bekannten steroidbasierten Wirkstoffen und Inhibitoren ähnelt. Das zentrale Ringsystem dieser Kaffee-Moleküle ahmt das starre Steroidgerüst natürlicher Gallensäuren und Oxysterole nach und erlaubt ihnen, sich in dieselben Taschen zu setzen wie körpereigene Signalmoleküle. Im FXR zeigten Cafestol und seine nahen Verwandten stabile, überwiegend ölige (hydrophobe) Kontakte in der Hauptbindungsstelle, mit vorhergesagten Bindungsstärken, die sich gegenseitig ähnelten, wenn auch schwächer als ein potenter pharmazeutischer FXR-Agonist. In CYP7A1 platzierten viele der Röstderivate ihren Furanring in der Nähe des Häm-Zentrums des Enzyms – des metallhaltigen Kerns, der die Chemie ausführt – und spiegelten damit wider, wie ein bekannter cholesterinabgeleiteter Inhibitor bindet. Einige Metaboliten verloren diesen kritischen Kontakt, was darauf hindeutet, dass sie weniger in der Lage sein könnten, das Enzym direkt zu blockieren.
Was das für Kaffeetrinker bedeutet
Für Laien bedeutet die Botschaft nicht, dass Kaffee unsicher ist, sondern dass bestimmte Zubereitungsarten und Mengen Respekt verdienen. Diese Arbeit stützt die Idee, dass Cafestol nicht allein wirkt: eng verwandte Moleküle, die beim Rösten und in frühen Stoffwechselstufen entstehen, könnten ebenfalls die gleichen Proteinschalter beeinflussen, die steuern, wie schnell der Körper Cholesterin entsorgt. Da diese Schlussfolgerungen auf Computermodellen und nicht auf Humanstudien beruhen, sollten sie eher als frühe Warnung denn als endgültiges Urteil betrachtet werden. Sie unterstreichen jedoch, warum ungefilterter, ölreicher Kaffee – French Press, gekochter Kaffee oder sehr starker Espresso – bei manchen Menschen zu höherem Cholesterin beitragen kann und warum Mäßigung sowie die Wahl der Brühmethode wichtig sind, wenn man die Freuden des Kaffees mit der langfristigen Herzgesundheit in Einklang bringen möchte.
Zitation: da Silva, M.A.E., Camargo, P.G., da Silva Lima, C.H. et al. Cafestol-derivatives as potential FXR agonists and CYP7A1 inhibitors and their impact on hypercholesterolemia: an in silico study. Sci Rep 16, 7102 (2026). https://doi.org/10.1038/s41598-026-37519-6
Schlüsselwörter: Kaffee-Diterpene, Cafestol, ungefilterter Kaffee, Cholesterinstoffwechsel, FXR und CYP7A1