Clear Sky Science · de
Validierung eines neuartigen genomischen Biomarkers für die Skalierbarkeit mesenchymaler Stammzellen und die Auswirkungen des Genotyps auf zelluläre Seneszenzphänotypen
Warum das Wachstum von Stammzellen mit der Zeit schwieriger wird
Stammzellen aus dem Knochenmark Erwachsener sind eine Grundlage vieler experimenteller Therapien, vom Reparieren beschädigter Knochen bis zur Abschwächung von Entzündungen. Es gibt jedoch einen Haken: Für die Behandlung eines Patienten müssen diese Zellen außerhalb des Körpers vermehrt werden, und je länger die Expansion dauert, desto mehr verlangsamen sie sich und verhalten sich wie „gealterte“ Zellen. Diese Studie untersucht, warum die Stammzellen mancher Menschen im Kulturgefäß langsamer altern und ob ein winziges fehlendes DNA‑Stück Wissenschaftlern helfen kann, die robustesten Zellen für künftige Therapien auszuwählen.
Ein fehlendes Gen, das die Spielregeln ändert
Die Forschenden konzentrierten sich auf ein Gen namens GSTT1, das Zellen dabei hilft, schädliche Moleküle zu entgiften, die während des normalen Stoffwechsels und unter Stress entstehen. Überraschenderweise fehlt ein beträchtlicher Teil der Bevölkerung dieses Gen vollständig – sie sind „GSTT1‑null“. Frühere Arbeiten deuteten an, dass Knochenmarkstammzellen von diesen Personen schneller wachsen und ihre schützenden Chromosomenenden, die Telomere, länger erhalten könnten. In diesem Projekt untersuchte das Team Stammzellen von sechs gesunden Spendern, teilte sie in GSTT1‑positiv und GSTT1‑null ein und verfolgte dann, wie sich die Zellen über viele Vermehrungszyklen hinweg und nach Bestrahlung mit Röntgenstrahlen, einem starken Auslöser zellulären Alterns, verhielten.
Schnell wachsende Zellen, die Alterungssignalen widerstehen
Als die Forschenden die Zellzahlen über mehrere Tage verfolgten, vermehrten sich GSTT1‑null Stammzellen in frühen Passagen schneller als Zellen mit vorhandenem Gen. Bei sehr langer Expansion näherten sich die Wachstumsraten zwischen den Gruppen an, doch der frühe Vorteil war deutlich. Um Altern direkt zu untersuchen, nutzte das Team einen klassischen Farbstoff, der seneszente, also „gealterte“, Zellen blau färbt. Nach vielen Teilungen und erneut nach Bestrahlung enthielten GSTT1‑null‑Kulturen durchweg weniger blaue, seneszente Zellen als GSTT1‑positive Kulturen. Wichtig ist, dass dieser Unterschied nicht auf langsameres Telomerverkürzen oder auf höhere Aktivität des Enzyms, das Telomere erhält (hTERT), zurückzuführen war; beide Messgrößen sahen unabhängig vom GSTT1‑Status ähnlich aus, was auf einen anderen zugrundeliegenden Mechanismus hindeutet.
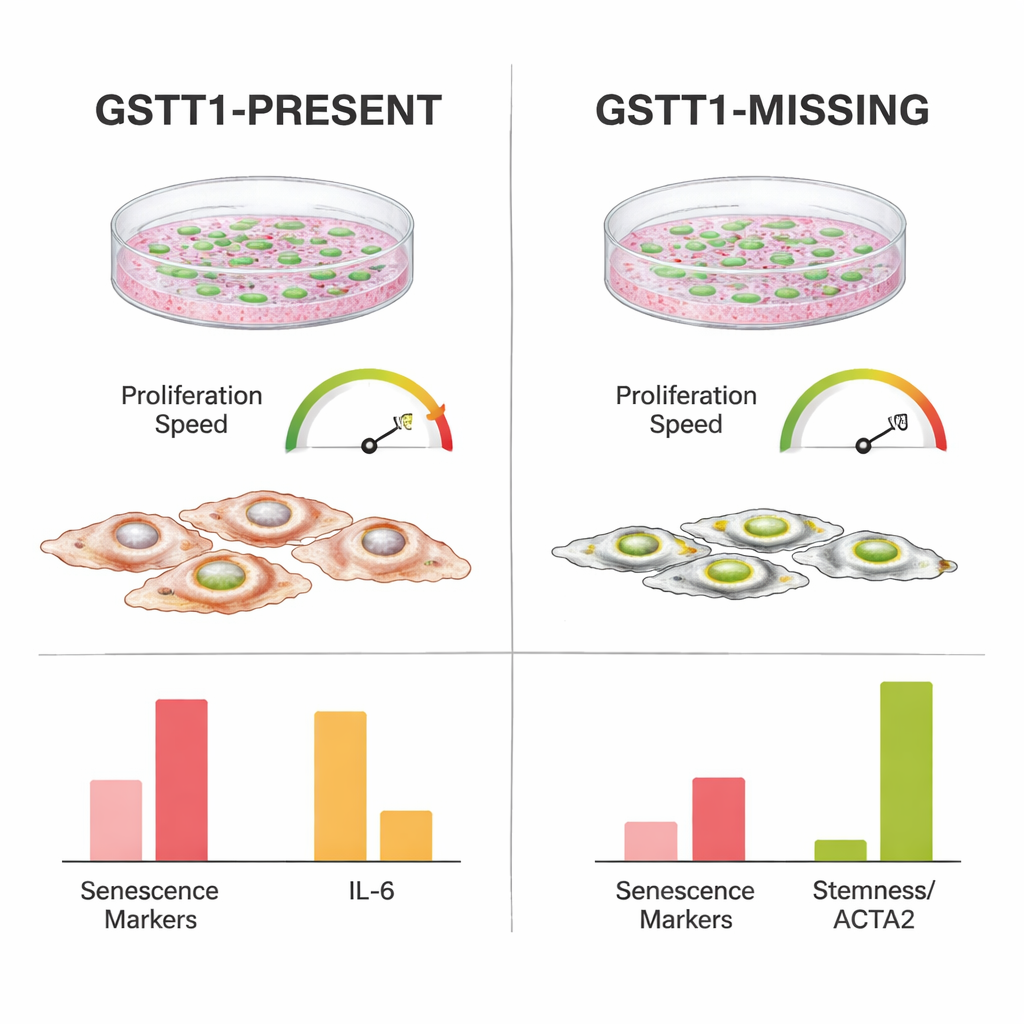
Geringerer Stress und weniger Entzündung in der Kultur
Um zu verstehen, was GSTT1‑null Zellen widerstandsfähiger machte, maßen die Forschenden die Aktivität von Genen, die mit Zellzyklusarrest, DNA‑Schäden und dem sogenannten seneszenzassoziierten sekretorischen Phänotyp verbunden sind – einem Cocktail aus entzündlichen und Stresssignalen, den alternde Zellen abgeben. Zellen mit vorhandenem GSTT1 zeigten höhere Werte wichtiger „Stopp“-Signale wie p21 und p14, besonders in späteren Passagen und nach Bestrahlung. Sie schalteten außerdem IL‑6, ein starkes entzündliches Molekül, und weitere stressbezogene Gene stärker hoch als GSTT1‑null Zellen. Im Gegensatz dazu hielten GSTT1‑null Stammzellen niedrigere Werte dieser Alters‑ und Entzündungsmarker bei, während sie höhere Werte von ACTA2 und TWIST1 aufrechterhielten, Genen, die mit struktureller Integrität und stammzellähnlichem Verhalten assoziiert sind. Bemerkenswerterweise behielten beide Genotypen eine ähnliche Fähigkeit zur Differenzierung in Knochen‑ und Fettzellen bei, was bedeutet, dass der schützende Effekt nicht einfach auf den Verlust normaler Stammzellfunktionen zurückzuführen war.
Was das für künftige Zelltherapien bedeuten könnte
Insgesamt deuten die Ergebnisse darauf hin, dass Knochenmarkstammzellen ohne GSTT1 teilweise vor dem üblichen Verschleiß durch Labor‑Expansion und Bestrahlung geschützt sind. Sie wachsen früh schneller, akkumulieren weniger offensichtlich gealterte Zellen und behalten ein weniger entzündliches Profil, obwohl sich ihre Chromosomen in ähnlichem Maße verkürzen. Für Unternehmen und Kliniken, die große Mengen an Stammzellen herstellen, könnte GSTT1‑Nullstatus als praktischer genetischer Marker dienen, um Spender zu identifizieren, deren Zellen Expansion besser tolerieren und somit potenziell konsistentere und wirksamere Therapien liefern. Natürlich wurde die Studie an einer kleinen Spendergruppe und unter nicht‑klinischen Kulturbedingungen durchgeführt, sodass größere, sorgfältig kontrollierte Studien nötig sind. Dennoch zeigt die Arbeit, wie ein einzelner vererbter Unterschied das Gleichgewicht zwischen jugendlichem und altersbedingtem Verhalten von in der Regenerativen Medizin gezüchteten Stammzellen verschieben kann.
Zitation: Ardana, I.K.K.G., Maldonado, V.V., Barnes, C.L. et al. Validation of a novel genomic biomarker of mesenchymal stem cell scalability and implications of genotype status on cellular senescence phenotypes. Sci Rep 16, 6219 (2026). https://doi.org/10.1038/s41598-026-37517-8
Schlüsselwörter: mesenchymale Stammzellen, zelluläre Seneszenz, Biomarker, Herstellung von Zelltherapien, GSTT1-Polymorphismus