Clear Sky Science · de
Neue Einblicke in die molekulare Grundlage der Gametogenese beim hybridogenetischen Wasserfrosch Pelophylax esculentus
Warum merkwürdige Frösche wichtig sind
Die meisten Tiere, einschließlich der Menschen, mischen ihre Gene jede Generation neu, wenn Samen- und Eizelle aufeinandertreffen. Einige ungewöhnliche Lebewesen umgehen diese Regel jedoch und vererben ganze Genome als fertige Klone. Europäische Wasserfrösche gehören zu dieser kleinen Gruppe. Sie sind lebende Experimente dafür, wie Sex, Asexualität und Hybridisierung sich gegenseitig beeinflussen können. Zu verstehen, wie diese Frösche ihre Eier und Spermien erzeugen, befriedigt nicht nur die Neugier an einem eigenartigen Amphibium – es wirft auch Licht darauf, wie Genome bei Wirbeltieren gesteuert, repariert und gelegentlich radikal umgeschrieben werden.
Frösche, die die Regeln der Vererbung brechen
In vielen europäischen Teichen kommen drei eng verwandte Wasserfroschtypen vor. Zwei sind gewöhnliche, sexuelle Arten, hier einfach L und R genannt. Wenn sie sich paaren, können sie ein Hybridelement LR hervorbringen, bekannt als Pelophylax esculentus. Dieser Hybrid vollbringt etwas Besonderes: In seiner Keimbahn – den Zellen, die zu Eiern oder Spermien werden – wirft er ein elterliches Genom aus und kopiert das andere unvermischt. Das Ergebnis sind klonale Keimzellen, die entweder ein intaktes L‑ oder ein intaktes R‑Genom tragen, das dann von einer normalen Keimzelle einer Elternart befruchtet wird. Je nach lokalem „Populationssystem“ schließen Hybriden routinemäßig das R‑Genom aus, das L‑Genom oder in einigen Regionen variieren die Individuen. Die Studie stellt die Frage: Welche Gene helfen dabei, diesen gezielten Genom‑Ausschluss und die klonale Vererbung zu steuern?
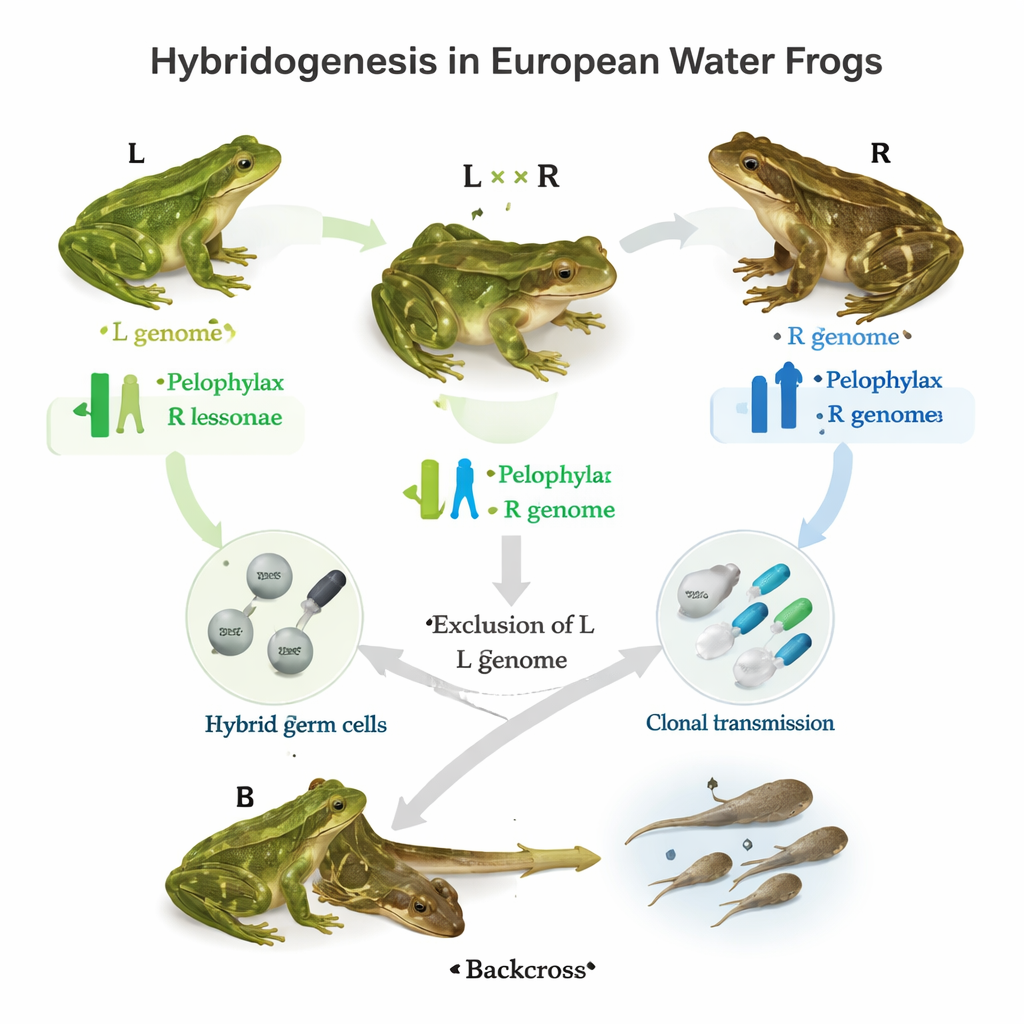
Auf der Suche nach Genen hinter dem klonalen Sex
Die Autoren stellten zunächst ein Verzeichnis von 160 Genen zusammen, die aus anderen Tieren bekannt dafür sind, an der Gametogenese beteiligt zu sein – dem Prozess der Bildung von Eiern und Spermien. Sie sequenzierten diese Gene aus Hoden von L‑ und R‑Fröschen und verglichen Grundmerkmale wie Länge, Struktur und Basenzusammensetzung der DNA. Die meisten dieser Gene erwiesen sich als hoch konserviert zwischen den beiden Arten, was darauf hindeutet, dass sie wichtige, wenig veränderliche Funktionen erfüllen. Danach konzentrierte sich das Team auf 52 dieser Gene und durchsuchte sie in mehr als 650 in ganz Europa gesammelten Fröschen nach einzelbasigen DNA‑Unterschieden, sogenannten SNPs. Diese Individuen stammten aus verschiedenen Populationssystemen: solchen, in denen nur L und Hybriden zusammen vorkommen, solchen mit nur R und Hybriden, all‑hybriden Systemen, die reich an triploiden Fröschen sind, und rein R‑Populationen.
Signale von Genfluss und verborgener Struktur
Durch die Analyse der SNP‑Muster fanden die Forschenden Hinweise auf Introgression – Genfluss – zwischen den L‑ und R‑Genpools. In mehreren Genen waren R‑Versionen kaum von ihren L‑Gegenstücken zu unterscheiden, am besten erklärbar durch frühere Hybridisierung und Rückkreuzung. Obwohl die Gesamtgrade des Genflusses gering waren, waren sie stärker in Richtung R als in Richtung L, was frühere genetische Untersuchungen bestätigt. Verglich das Team SNP‑Häufigkeiten zwischen Populationssystemen, zeigten sich bestimmte genetische Varianten, die stark mit bestimmten Systemen assoziiert waren. So waren LR‑Hybriden aus all‑hybriden Populationen genetisch ähnlicher zu LR‑Fröschen aus R–Hybrid‑Systemen als zu LR‑Fröschen aus rein diploiden L–Hybrid‑Systemen und enthüllten damit eine verborgene Struktur, die mit der lokalen Organisation der Fortpflanzung verknüpft ist.
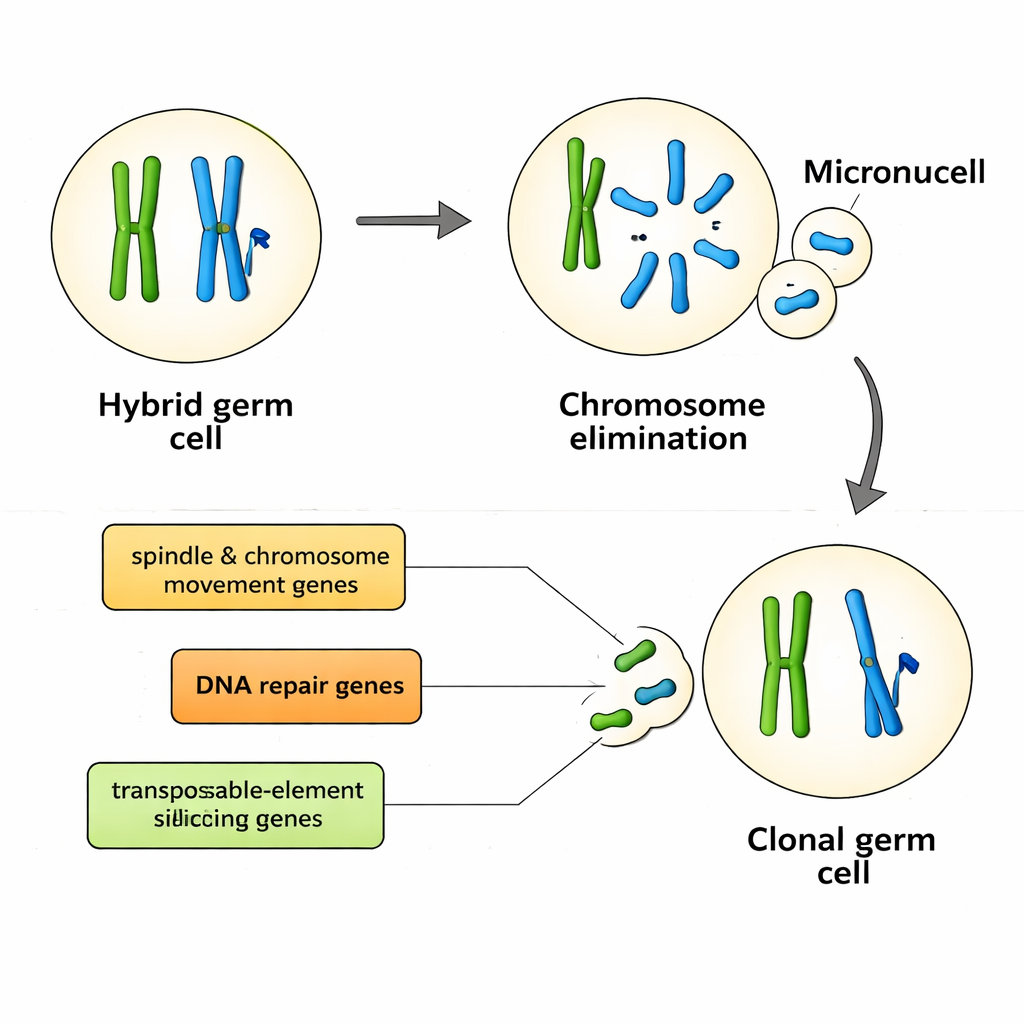
Zentrale Akteure in Chromosomenkontrolle und Genomverteidigung
Zehn Gene zeigten besonders starke Assoziationen mit dem Populationssystem und damit mit der Art und Weise, wie Genome ausgeschlossen und klonal weitergegeben werden. Sie gehören zu mehreren funktionellen Gruppen. Einige, wie kif22 und nusap1, helfen beim Aufbau und der Kontrolle des Spindelapparats – der zellulären Maschine, die Chromosomen während der Zellteilung bewegt. Andere, darunter hormad1, rad50, rad51ap1 und sfr1, sind zentral für die Entstehung und Reparatur von DNA‑Doppelstrangbrüchen – kontrollierte Schnitte, die normalerweise Rekombination fördern, aber auch die gezielte Eliminierung von Chromosomen auslösen könnten. Ein weiteres Gen, henmt1, stabilisiert kleine RNAs, die transponierbare Elemente stilllegen – mobile DNA‑Sequenzen, die Genome schädigen oder Zentromere, die für korrekte Chromosomenbewegung nötig sind, umgestalten können. Zusammen zeichnen diese Gene das Bild, dass Genom‑Ausschluss aus dem Zusammenspiel von Chromosomen‑Transport, DNA‑Reparatur und Genom‑Verteidigungswegen entsteht und nicht von einem einzigen Master‑Schalter gesteuert wird.
Evolution am Rande der Stabilität
Die Studie legt nahe, dass seltene Rekombination und bidirektionaler Genfluss zwischen L und R geholfen haben, unterschiedliche Genomvarianten zu erzeugen, die verschiedene nicht‑mendel’sche Vererbungsmodi begünstigen. Einige Hybridlinien könnten schädliche Mutationen akkumulieren, während ihre klonalen Genome voranschreiten, während sporadische Rekombination und Introgression sie gelegentlich auffrischen – zum Preis von Entwicklungsproblemen bei einigen Nachkommen. Anstatt einer einfachen Regel zu folgen, die auf dem Grad der Divergenz zweier Arten beruht, scheint das Pelophylax‑System von einem komplexen Netzwerk interagierender Faktoren bestimmt zu werden, das fein einstellt, ob ein Hybrid zu einer stabilen klonalen Linie oder zu einer Sackgasse wird.
Was das über Frösche hinaus bedeutet
Für allgemeine Leser lautet die Kernbotschaft: Vererbung kann weit flexibler sein, als es die Mendelschen Schaubilder vermuten lassen. Diese Wasserfrösche zeigen, dass Wirbeltier‑Genome selektiv gelöscht, kopiert und wiederverwendet werden können wie modulare Bausteine, je nach Kontext. Indem die Studie echte Gene identifiziert, die mit diesem Prozess verknüpft sind, macht sie aus einem seltsamen Fortpflanzungstrick ein bearbeitbares molekulares Problem. Künftige Experimente, geleitet von diesem neuen Genkatalog, werden testen, wie Änderungen in Chromosomen‑Handhabungs‑ und Genom‑Verteidigungswegen eine Population zwischen gewöhnlichem Sex und klonaler Hybridfortpflanzung umschalten können – Erkenntnisse, die letztlich Fruchtbarkeit, Genomstabilität und die Evolution des Sex bei vielen anderen Tieren erhellen könnten.
Zitation: Plötner, M., Meixner, M., Poustka, A.J. et al. New insights into the molecular basis of gametogenesis in the hybridogenetic water frog Pelophylax esculentus. Sci Rep 16, 5012 (2026). https://doi.org/10.1038/s41598-026-37515-w
Schlüsselwörter: Hybridogenese, Wasserfrösche, klonale Vererbung, Genom‑Ausschluss, Gametogenese