Clear Sky Science · de
Liquid-Biopsie von Plasma- und Harn-cfDNA unterscheidet Gliomrezidiv von strahlenbedingter Gehirnnekrose in präklinischen Modellen
Warum ein einfacher Blut- und Urintest Hirntumorpatienten helfen könnte
Für Menschen, die wegen eines Hirntumors behandelt wurden, ist eine der beängstigendsten Fragen nach einer Bestrahlung, ob ein neuer Fleck im Bild einen Tumorrückfall anzeigt oder ob das Gehirn lediglich Narbengewebe als Folge der Behandlung aufweist. Diese beiden Möglichkeiten sehen in konventionellen MRT-Aufnahmen fast identisch aus, verlangen aber sehr unterschiedliche Entscheidungen: aggressivere Therapie versus behutsame Beobachtung. Diese Studie an Ratten untersucht, ob Fragmente von DNA, die im Blut und Urin zirkulieren, auf einfachem, nichtinvasivem Weg zwischen beiden unterscheiden könnten — womit Patienten riskante Hirnbiopsien erspart und Ärztinnen und Ärzten die Wahl des richtigen nächsten Schritts erleichtert werden könnte.
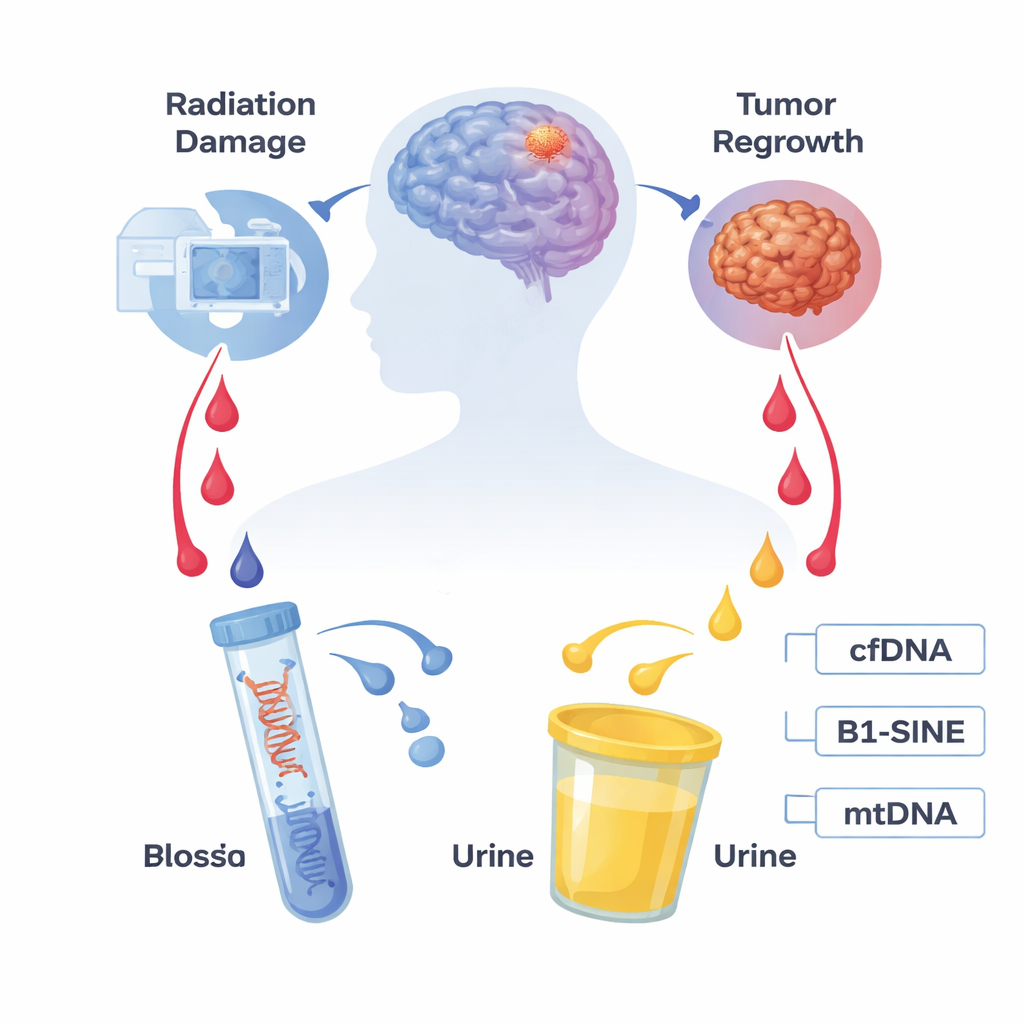
Die Herausforderung, Nachbehandlungsaufnahmen zu interpretieren
Gliome gehören zu den tödlichsten Hirntumoren, mit hohen Rückfallraten selbst nach Operation, Strahlentherapie und Chemotherapie. Wenn ein zuvor behandeltes Areal im MRT wieder auffällig wird, kann das entweder Tumorwachstum oder eine strahlenbedingte Gehirnnekrose bedeuten — eine verzögerte Form des Gewebeuntergangs durch hoch dosierte Strahlung. Beide Zustände können Schwellungen, neurologische Symptome und ähnliche Bildmuster verursachen. Derzeit verlassen sich Ärztinnen und Ärzte oft auf langfristige Bildverläufe oder invasive chirurgische Biopsien, um zu klären, welcher Prozess vorliegt. Diese Vorgehensweisen sind langsam, riskant und mitunter nicht eindeutig, weshalb ein sicherer, frühzeitiger und verlässlicherer Test dringend benötigt wird.
Auf der Spur frei treibender DNA
Unsere Zellen setzen ständig winzige Fragmente genetischen Materials, so genannte zellfreie DNA, in Körperflüssigkeiten wie Blut und Urin frei. Tumoren und geschädigtes Gewebe geben noch mehr dieser Bruchstücke ab. Die Forschenden konzentrierten sich auf zwei spezifische Signale: B1-SINE, eine häufige repetitive DNA-Sequenz, die das allgemeine Niveau zellfreier DNA im Blut von Nagetieren widerspiegelt, und mitochondriale DNA (mtDNA), die aus den Kraftwerken der Zelle stammt und bei Zellstress oder -untergang freigesetzt werden kann. Da Blutentnahmen und Urinsammlungen deutlich einfacher und sicherer sind als Hirnbiopsien, sind diese Marker vielversprechende Kandidaten für eine "Liquid Biopsy" — einen Test, der molekulare Informationen aus Körperflüssigkeiten statt aus Gewebe liest.
Rattenmodelle, die die menschliche Erkrankung nachahmen
Um die Idee unter kontrollierten Bedingungen zu prüfen, erzeugte das Team zwei separate Rattenmodelle. In einer Gruppe setzten sie Gliomzellen ins Gehirn, ließen einen Tumor heranwachsen, entfernten ihn chirurgisch und verfolgten die Tiere weiter, bis der Tumor wieder zunahm — was ein menschliches Gliomrezidiv nachahmt. In einer anderen Gruppe setzten sie gezielt hoch dosierte Strahlung auf eine Gehirnhälfte an, um eine verzögerte strahlenbedingte Nekrose auszulösen, die eine ernsthafte Komplikation beim Menschen widerspiegelt. Im Verlauf der folgenden Wochen sammelten sie Blut und Urin, bestimmten B1-SINE- und mtDNA-Werte mittels empfindlicher DNA-Amplifikationstechniken und bestätigten die Veränderungen im Gehirn durch MRT-Aufnahmen und histologische Analysen.
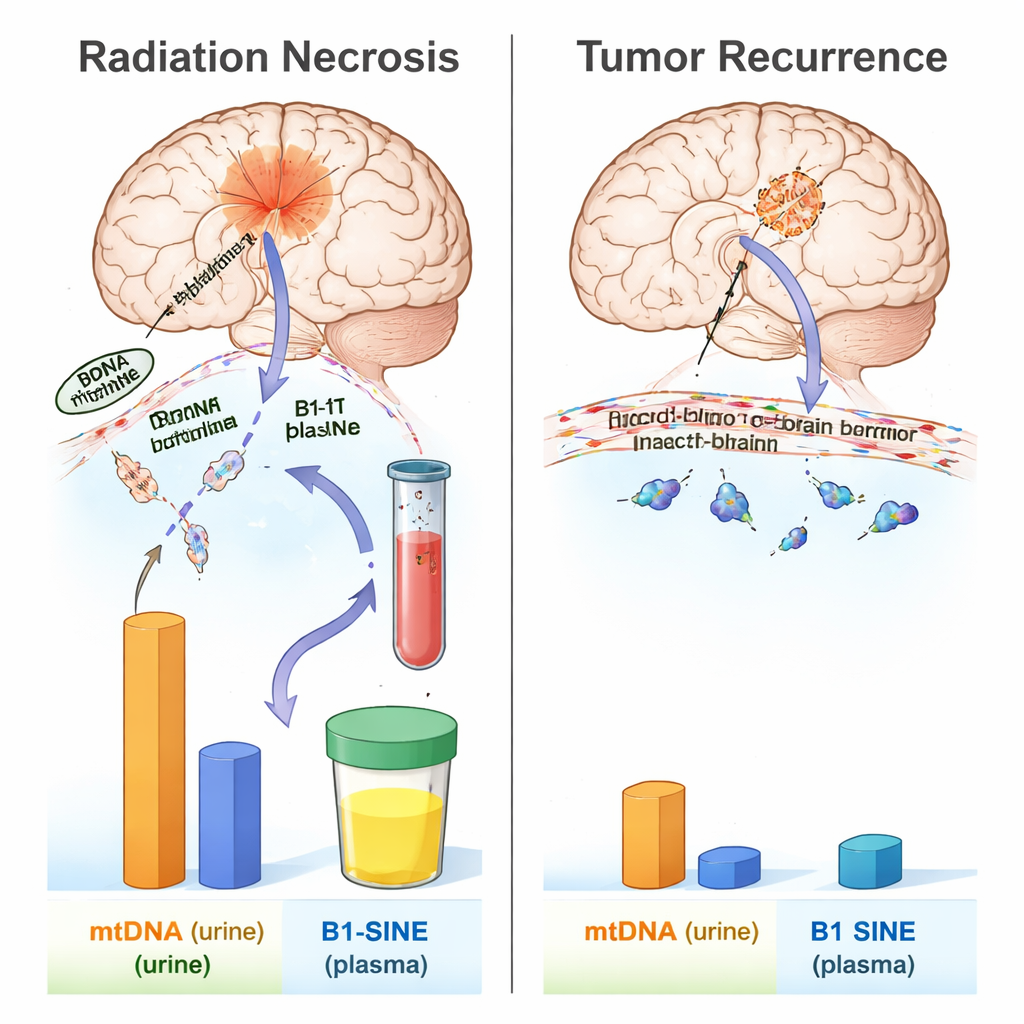
Unterschiedliche DNA-Signaturen bei Strahlenschäden
Die Muster der DNA-Fragmente in den Flüssigkeiten unterschieden sich deutlich zwischen den beiden Zuständen. Nach der Strahlung stieg die mitochondriale DNA im Urin innerhalb von 24 Stunden an, sank kurzzeitig wieder ab und stieg dann um Woche sechs herum erneut an, mit einem Peak in Woche acht und anhaltender Erhöhung, während sich die Strahlennekrose entwickelte. Auch die plasmatischen B1-SINE-Werte schossen nach der Bestrahlung nach oben, zeigten einen klaren Gipfel in Woche acht und blieben von Woche acht bis sechzehn erhöht — dem Zeitraum, in dem Gewebeuntergang in Bildgebung und Pathologie zu sehen war. Im Gegensatz dazu zeigten Ratten mit wiederkehrendem Gliom über denselben Zeitraum keine signifikanten Veränderungen in weder der urinären mtDNA noch der plasmatischen B1-SINE im Vergleich zu gesunden bzw. Placebo-operierten Kontrollen. Das deutet darauf hin, dass strahlenbeschädigtes Hirngewebe in diesem Modell eine charakteristische Welle von DNA-Fragmente in die Zirkulation freisetzt, die beim Tumorwachstum nicht beobachtet wurde.
Was das für zukünftige Patienten bedeuten könnte
Für Laien lautet die Kernbotschaft, dass einfache Blut- und Urintests eines Tages Ärztinnen und Ärzten helfen könnten, strahlenbedingte Hirnschäden von zurückkehrendem Krebs zu unterscheiden, ohne den Schädel zu öffnen. In diesen Rattenversuchen stiegen zwei Signale — mtDNA im Urin und B1-SINE im Blut — deutlich nur bei Vorliegen einer Strahlennekrose, nicht bei Tumorrezidiv. Zwar sind größere Studien und Untersuchungen am Menschen nötig und müssen die genauen Grenzwerte sowie human-spezifische Marker noch definiert werden, doch weist diese Forschung in Richtung einer Zukunft, in der ein "flüssiges Abbild" zirkulierender DNA die Nachsorge von Hirntumoren lenken, Unsicherheit verringern und eine persönlichere, weniger invasive Versorgung unterstützen kann.
Zitation: Sun, J., Jin, C., Chen, Y. et al. Liquid biopsy of plasma and urinary CfDNA differentiates glioma recurrence from radiation brain necrosis in preclinical models. Sci Rep 16, 7123 (2026). https://doi.org/10.1038/s41598-026-37493-z
Schlüsselwörter: Gliom, Strahlennekrose, Liquid Biopsy, zellfreie DNA, Überwachung von Hirntumoren