Clear Sky Science · de
Außerordentlich selektive Blockade des Spannungssensors von NaV1.5-Kanälen durch Mg‑Protoporphyrin hemmt die Migration von Krebszellen
Pigment aus Pflanzen weist auf neue Krebsstrategie
Unsere Herzen und unsere Tumoren könnten eine unerwartete Verwundbarkeit teilen: ein spezielles elektrisches Tor in der Zellmembran namens NaV1.5. Diese Studie zeigt, dass ein natürlicher Verwandter der chlorophyll‑Bausteine in Pflanzen, Magnesium‑Protoporphyrin IX (MgPpIX), dieses Tor mit außergewöhnlicher Präzision schließen kann. Dadurch verlangsamt es stark die Bewegung bestimmter Krebszellen – ein Hinweis darauf, dass ein von der Photosynthese inspirierter Wirkstoff die Metastasenbildung dämpfen könnte, ohne Gehirn oder Muskulatur stark zu stören.
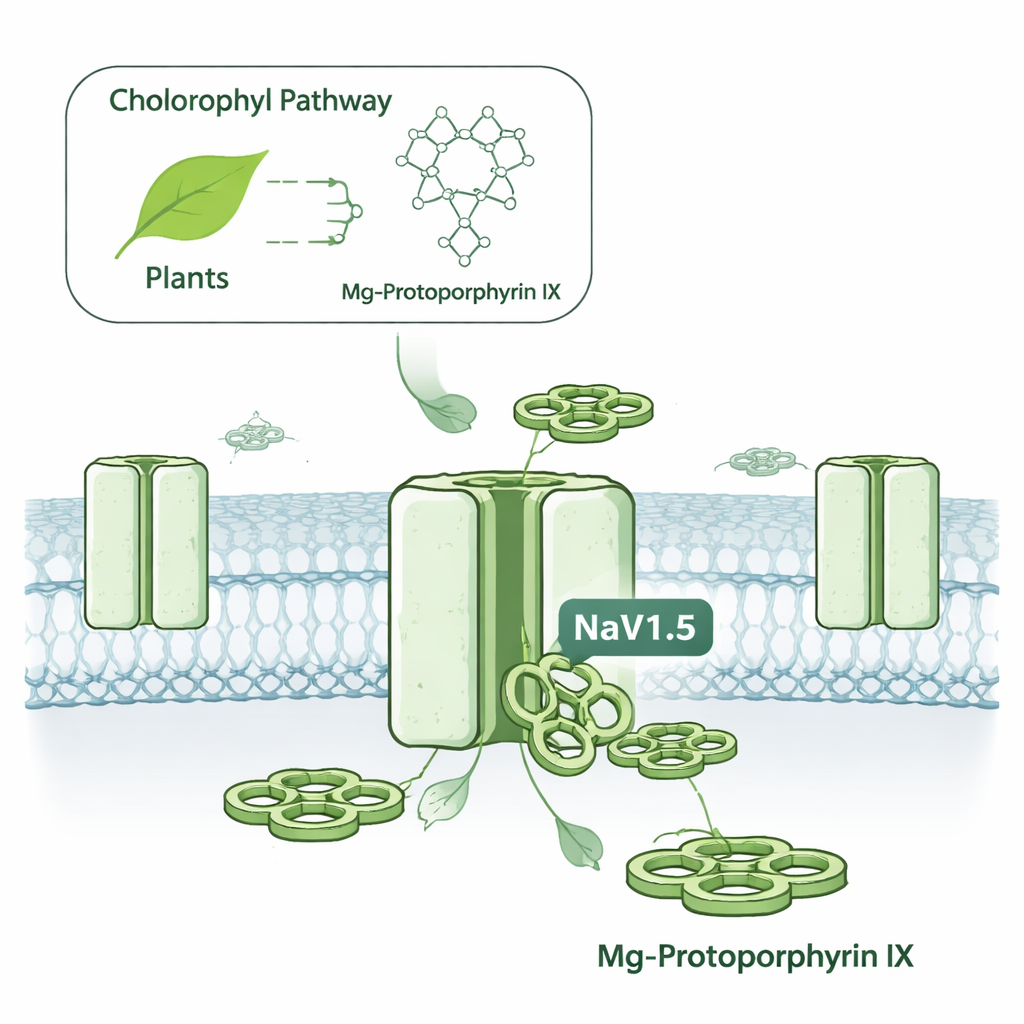
Ein verborgenes elektrisches Schaltglied in Krebszellen
Zellen nutzen spannungsabhängige Natriumkanäle als winzige Türen, die sich öffnen und schließen, um geladene Teilchen passieren zu lassen und elektrische Signale zu erzeugen. NaV1.5 ist vor allem für seine Rolle bei Herzschlägen bekannt, wo es hilft, jede Kontraktion auszulösen. Derselbe Kanal findet sich aber auch in mehreren Krebsarten, einschließlich Brust‑ und Darmtumoren, wo seine Aktivität mit erhöhter Zellbewegung und Invasivität in Verbindung gebracht wurde. NaV1.5 ins Visier zu nehmen war schwierig, weil die meisten Natriumkanal‑Medikamente auch verwandte Kanäle in Nerven und Skelettmuskulatur treffen und Nebenwirkungen wie Krampfanfälle, Taubheit oder Muskelschwäche riskieren. Die Autoren wollten herausfinden, ob es kleine Moleküle gibt, die NaV1.5 mit deutlich höherer Selektivität von seinen Verwandten unterscheiden können.
Pflanzeninspiriertes Hemmstoff mit Rekordpräzision
Das Team untersuchte eine Familie ringförmiger Moleküle, so genannter Metall‑Protoporphyrine, die den Kernen von Häm im Blut und Chlorophyll in Pflanzen ähneln, aber unterschiedliche zentrale Metallatome enthalten. Bei Tests an humanen NaV1.5‑Kanälen, die in kultivierten Zellen produziert wurden, stach ein Stoff besonders hervor: MgPpIX. Er verringerte den elektrischen Strom durch NaV1.5 bei nanomolaren Konzentrationen um etwa 99 %, also ungefähr 100‑mal wirksamer als ein eisenhaltiges Gegenstück (Hemin). Andere Metallvarianten, etwa mit Nickel oder Kupfer, waren praktisch inaktiv. Bemerkenswerterweise ließ MgPpIX mehrere andere menschliche Natriumkanaltypen (in Gehirn, peripheren Nerven und Skelettmuskulatur) bei denselben Dosen völlig unberührt und erreicht damit eine der schärfsten Selektivitäten, die je für diese Kanal‑Familie berichtet wurden.
Wie das Molekül einen winzigen Spannungshebel blockiert
Um diese ungewöhnliche Präzision zu verstehen, kombinierten die Forschenden genetische Modifikationen mit Computersimulationen. Natriumkanäle bestehen aus vier sich wiederholenden Bereichen, von denen jeder einen „Spannungssensor“ enthält, der seine Position ändert, wenn sich das Membranpotenzial verändert. Durch den Austausch einzelner Aminosäuren zwischen NaV1.5 und seinen unempfindlichen Verwandten führte das Team die Wirkung von MgPpIX auf den Spannungssensor der zweiten Domäne zurück, insbesondere auf zwei Residuen, die nach außen exponiert sind. Molekulardynamische Simulationen in einer realistischen Membranumgebung legen nahe, dass sich MgPpIX gegen diesen Sensor legt, wenn er sich in seiner ruhenden, „abwärts“ gerichteten Stellung befindet. Das positiv geladene Metallzentrum von MgPpIX wird von einer negativ geladenen Seitenkette am Kanal angezogen, während der flache Ring mit umgebenden Lipiden interagiert. Diese Bindung scheint den Spannungssensor zu verriegeln, verhindert dessen Bewegung in den aktiven „aufwärts“ Zustand und hält so den Kanal geschlossen. Interessanterweise können starke Depolarisationen – etwa während eines Herzschlags – das Molekül vorübergehend lösen, ein Verhalten, das die Autoren als „reverse use‑dependence“ beschreiben.
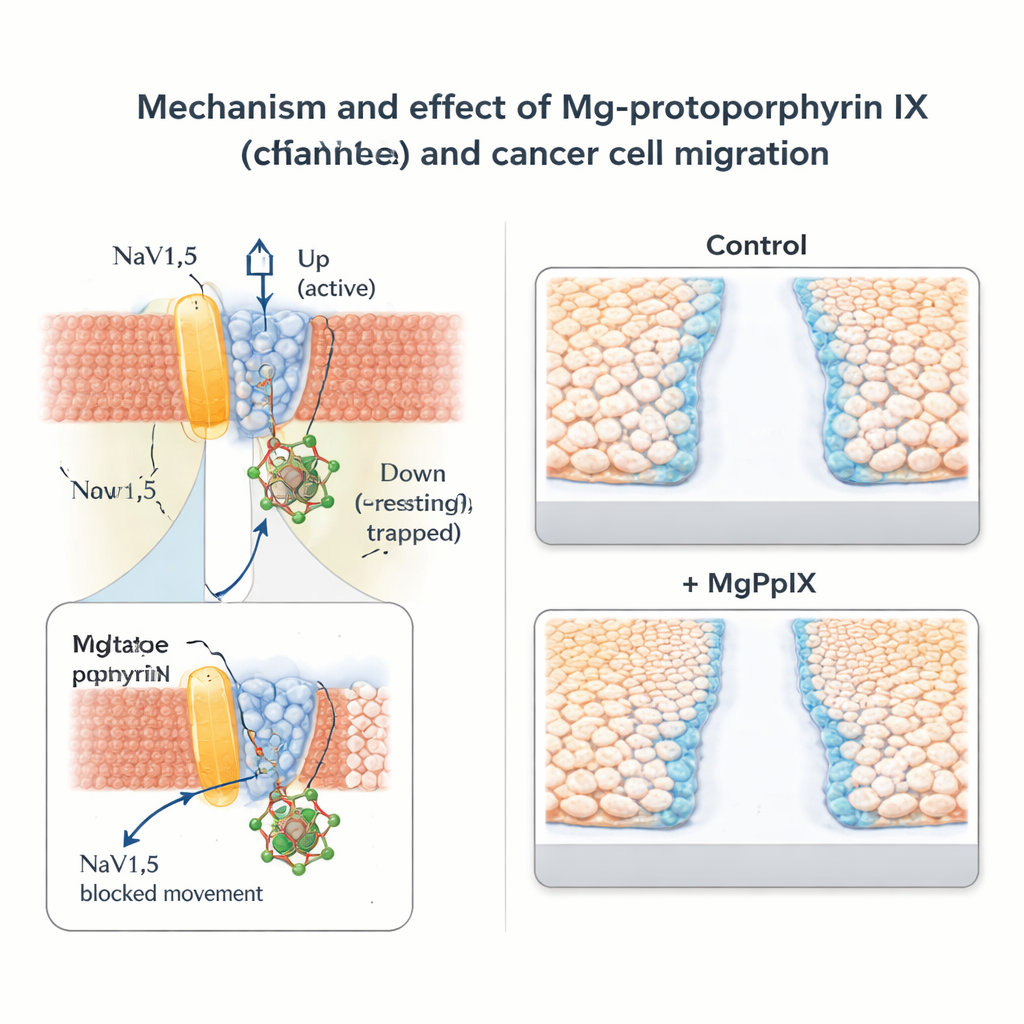
Verlangsamte Krebszellbewegung ohne breitflächige Nervenblockade
Das Team untersuchte anschließend, welche Folgen diese molekulare Bremse für das Krebsverhalten hat. In Brustkrebs‑(MDA‑MB‑231) und Darmkrebs‑(SW‑480)‑Zelllinien, die natürlicherweise NaV1.5 exprimieren, reduzierte MgPpIX die Natriumströme drastisch und verlangsamte die Zellmigration in standardisierten „Scratch“‑ und Transwell‑Assays. Je stärker ein bestimmtes Metall‑Protoporphyrin NaV1.5 blockierte, desto stärker behinderte es die Zellbewegung, was die Verbindung zwischen Kanalaktivität und Mobilität untermauert. Im Gegensatz dazu zeigten Krebszelllinien ohne NaV1.5 weder elektrisch noch in Migrationsversuchen eine Reaktion auf MgPpIX, was die Idee stützt, dass der Effekt hochspezifisch und nicht allgemein toxisch ist. Im Vergleich zum klassischen Natriumkanal‑Toxin Tetrodotoxin erreichte MgPpIX eine stärkere Unterdrückung der Migration bei deutlich niedrigeren Konzentrationen.
Verheißung und Vorsicht für künftige anti‑metastatische Medikamente
Für Nicht‑Spezialisten ist die zentrale Aussage: Die Forschenden haben ein pflanzenverwandtes Molekül gefunden, das wie eine präzise Klammer an einem herztypischen elektrischen Tor wirkt, das von einigen Krebsarten missbraucht wird. Indem es den winzigen Spannungshebel des Tors in seiner ruhenden Position einfängt, kann MgPpIX die Mobilität von Krebszellen im Labor stark einschränken und gleichzeitig andere für Sinneswahrnehmung und Bewegung wichtige Natriumkanäle verschonen. Da die schnelle elektrische Aktivität des Herzens diese Blockade teilweise aufheben kann, könnte es sogar ein Sicherheitsfenster geben, in dem Tumorzellen stärker gehemmt werden als Herzmuskelzellen. Während MgPpIX selbst möglicherweise nicht unmittelbar als Arzneimittel bereitsteht, liefern sein einzigartiger Bindungsort und Mechanismus eine kraftvolle Blaupause für die Entwicklung künftiger Wirkstoffe, die die Ausbreitung von Krebs durch gezielte Hemmung von NaV1.5 mit beispielloser Selektivität stoppen sollen.
Zitation: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
Schlüsselwörter: Natriumkanäle, NaV1.5, Migration von Krebszellen, chlorophyll‑abgeleitete Moleküle, zielgerichtete Ionenkanal‑Medikamente