Clear Sky Science · de
MiniPromoters Ple384 (TH) und Ple388 (PITX3) zur gezielten Ansprache von dopaminergen Neuronen im Mittelhirn bei Mäusen und Affen
Warum diese Forschung für die Gehirngesundheit wichtig ist
Die dopaminproduzierenden Zellen des Gehirns helfen uns, uns zu bewegen, aus Belohnungen zu lernen und motiviert zu bleiben. Es sind auch genau diese Zellen, die bei der Parkinson-Krankheit absterben. Wissenschaftler und Ärztinnen möchten hilfreiche Gene oder molekulare Werkzeuge gezielt in diese anfälligen Neurone bringen — sowohl in Versuchstieren als auch eines Tages beim Menschen. Ein zentrales Hindernis war jedoch, Gentherapie so zu steuern, dass sie nur in den richtigen Zellen aktiv wird und nicht überall im Gehirn. Diese Studie beschreibt zwei neue, kompakte DNA-„Schalter“, die Gene verlässlich nahezu ausschließlich in Mittelhirn-Dopaminneuronen von Mäusen und Affen einschalten können. Das eröffnet Wege für präzisere und potenziell sicherere Behandlungen.
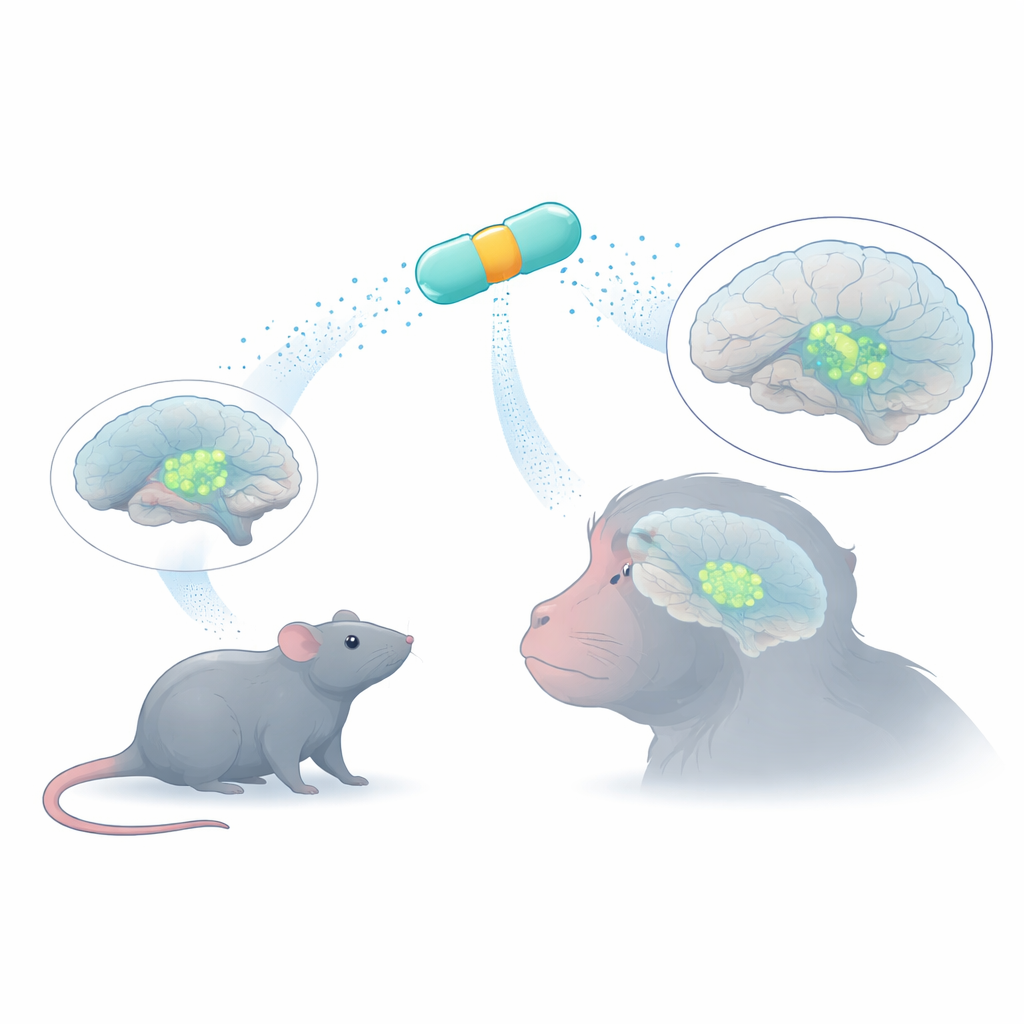
Kleine genetische Schalter mit großer Aufgabe
Um ein therapeutisches Gen in Gehirnzellen zu bringen, verwenden Forschende oft Adeno-assoziierte Viren (AAVs), harmlose Transporter, die nur eine begrenzte Menge DNA fassen können. Innerhalb jedes Virus fungiert eine kurze Promotorsequenz wie ein An-/Ausschalter, der bestimmt, in welchen Zellen dieses Gen aktiv ist. Viele natürliche Promotoren sind zu groß oder zu unspezifisch und schalten Gene in zu vielen Zelltypen ein. Das Team nutzte Bioinformatik, um acht sehr kompakte „MiniPromoters“ aus menschlicher DNA zu entwerfen — kurze Kombinationen von Kontrollelementen aus Genen, die dafür bekannt sind, dopaminproduzierende Neurone zu markieren. Das Ziel war eine Reihe von Schaltern, die in AAVs passen und dennoch starke, zelltypspezifische Expression antreiben.
Die richtigen Ziele im Mausgehirn finden
Die acht Kandidaten-MiniPromoter wurden zuerst an Mäusen getestet. Jeder Promotor wurde in einen AAV eingebaut, der ein grünes fluoreszierendes Protein trug, so dass die Forschenden sehen konnten, wo der Schalter aktiv war. Die Viren wurden entweder in den Blutkreislauf oder direkt in die mit Flüssigkeit gefüllten Bereiche des Gehirns verabreicht. Die meisten MiniPromoter erwiesen sich als wenig selektiv: Einige leuchteten in vielen Nicht-Dopamin-Zellen, andere zeigten kaum Aktivität. Zwei stachen heraus. Ple384 basierte auf Kontrollregionen des Gens für Tyrosinhydroxylase, dem Schlüsselenzym aller Katecholamin-produzierenden Neurone. Ple388 stammte aus PITX3, einem Gen, das für eine Untergruppe von Mittelhirn-Dopaminneuronen wichtig ist. Beide, Ple384 und Ple388, erzeugten starke, eng begrenzte Signale in der Substantia nigra compacta und dem ventralen tegmentalen Areal — den Mittelhirnzentren der Dopaminneurone — wobei über 90 % der markierten Zellen auch das charakteristische Dopamin-Molekül aufwiesen.
Von Mäusen zu Affen, ohne tief ins Gehirn bohren zu müssen
Jegliche Gentherapie für menschliche Erkrankungen muss letztlich in Primaten funktionieren, deren Gehirne größer und komplexer sind. Die direkte Injektion in die Substantia nigra ist technisch anspruchsvoll und kann diese kleine, tief liegende Struktur schädigen. Stattdessen prüften die Forschenden, ob dieselben MiniPromoter über das Rückenmarkswasser (Zerebrospinalflüssigkeit) von Rhesusmakaken mittels einer einzigen Injektion in einen Seitenventrikel verteilt werden können. Mit einer AAV-Kapsidvariante, die dafür bekannt ist, sich gut von den Flüssigkeitsräumen aus zu verbreiten, stellten sie fest, dass sowohl Ple384 als auch Ple388 eine robuste Expression in Mittelhirn-Dopaminneuronen der Substantia nigra und des ventralen tegmentalen Areals antrieben, während andere dopaminreiche Regionen wie der Hypothalamus und der Locus coeruleus weitgehend verschont blieben. Die meisten markierten Zellen in der Zielregion waren Dopaminneurone, was bestätigt, dass die Schalter ihre Selektivität über die Speziesgrenze hinweg beibehielten.
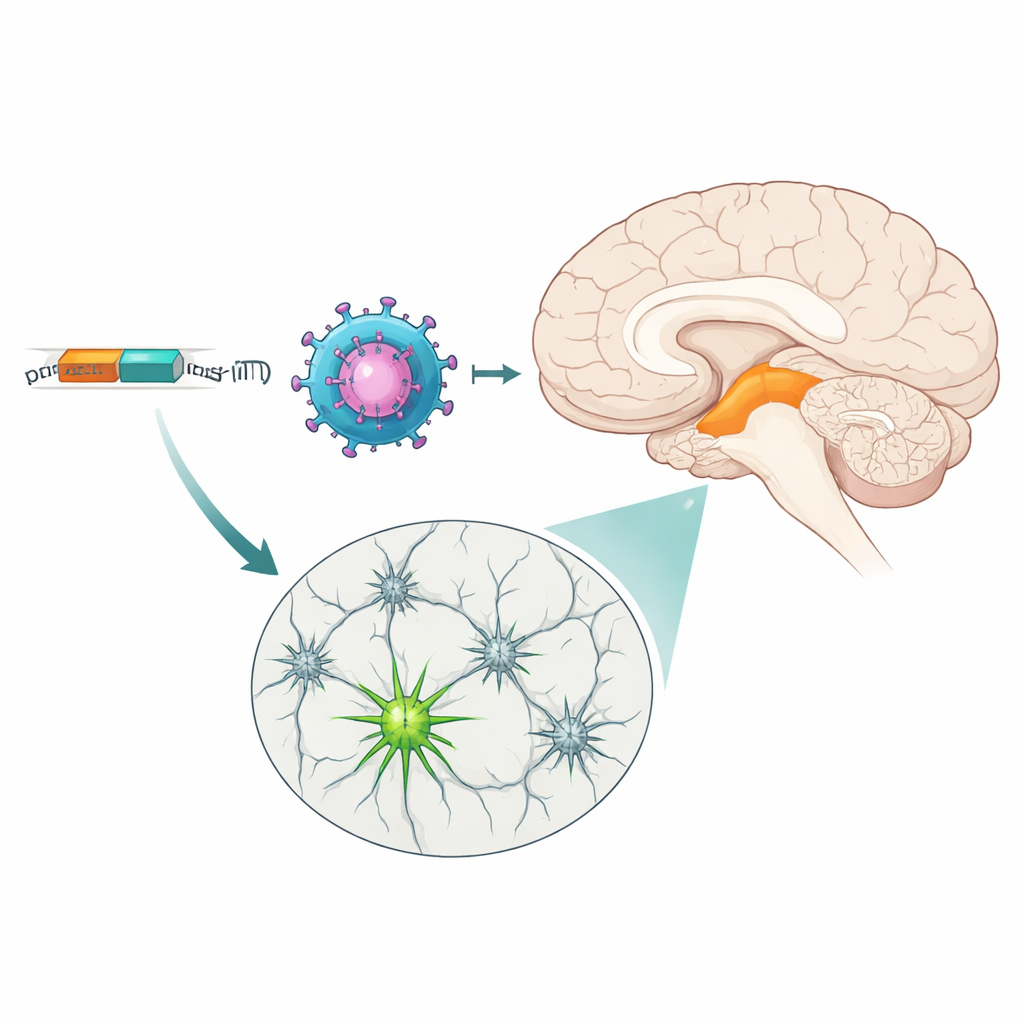
Zwei Werkzeuge mit unterschiedlichen Stärken
Obwohl beide MiniPromoter ihre Ziele trafen, taten sie dies mit unterschiedlichen Mustern. Ple384, basierend auf dem weiter gefassten Tyrosinhydroxylase-Gen, markierte insgesamt mehr Neurone und deckte sowohl ventrale als auch dorsale Schichten der Substantia nigra sowie einen größeren Teil des ventralen tegmentalen Areals ab. Ple388, entsprechend dem engeren PITX3-Gen, kennzeichnete vor allem eine Untergruppe ventraler Schicht-Neurone und zeigte schwächere Fluoreszenz. Off-Target-Expression trat hauptsächlich in der Nähe der Injektionsstellen und in einigen peripheren Organen nach intravenöser Verabreichung auf, doch Kontrollversuche zeigten, dass die viralen Vektoren viele Hirnregionen erreichen konnten; es waren die MiniPromoter selbst, die die Expression überwiegend auf Mittelhirn-Dopaminneurone beschränkten. Diese einstellbare Stärke — ein Schalter kraftvoller und breiter, der andere selektiver und moderater — erlaubt Forschenden, den für ihren Zweck passenden Schalter zu wählen, von sanfter Modulation bis hin zu breit angelegten Interventionen.
Was das für künftige Therapien bedeutet
Für Nicht-Spezialisten ist die Kernaussage, dass die Autoren zwei kompakte genetische Schalter entwickelt haben, die wie präzise, programmierbare Lichtschalter für Dopaminneurone bei Mäusen und Affen wirken. Ple384 bietet starken, weitreichenden Zugang zu diesen Zellen, während Ple388 sich auf eine schmalere, besonders verletzliche Untergruppe konzentriert. Da die Schalter klein genug sind, um bequem in gängige virale Vektoren zu passen, bleibt Platz für therapeutische Gene, und Nebenwirkungen durch ungewollte Aktivität in anderen Hirnregionen könnten reduziert werden. Während die Gentherapie bei Parkinson und verwandten Erkrankungen voranschreitet, werden solche gezielten Kontrollelemente zu wesentlichen Bestandteilen von Behandlungen, die sowohl kraftvoll als auch präzise sind.
Zitation: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
Schlüsselwörter: Dopaminneurone, Gentherapie, Morbus Parkinson, AAV-Vektoren, zell-spezifische Promotoren