Clear Sky Science · de
Therapeutische Wirkungen von IGF-2 bei NMOSD durch Hemmung der Astrozytenapoptose über Modulation des IGF-1R/PI3K/AKT-Signalwegs
Gehirnschutz bei einer wenig bekannten Autoimmunerkrankung
Neuromyelitis-optica-Spektrumstörung (NMOSD) ist eine seltene, aber verheerende Autoimmunerkrankung, die die Sehnerven und das Rückenmark angreift und Patientinnen und Patienten häufig blind, gelähmt oder mit schweren kognitiven Beeinträchtigungen zurücklässt. Die derzeit verfügbaren Medikamente dämpfen vor allem das Immunsystem, sind teuer und schützen Gehirnzellen nicht direkt vor Schäden. Diese Studie untersucht, ob ein natürliches, wachstumsbezogenes Molekül im Blut, namens IGF‑2, Gehirnzellen bei NMOSD vor Verletzungen schützen und so einen neuen Therapieansatz bieten könnte.
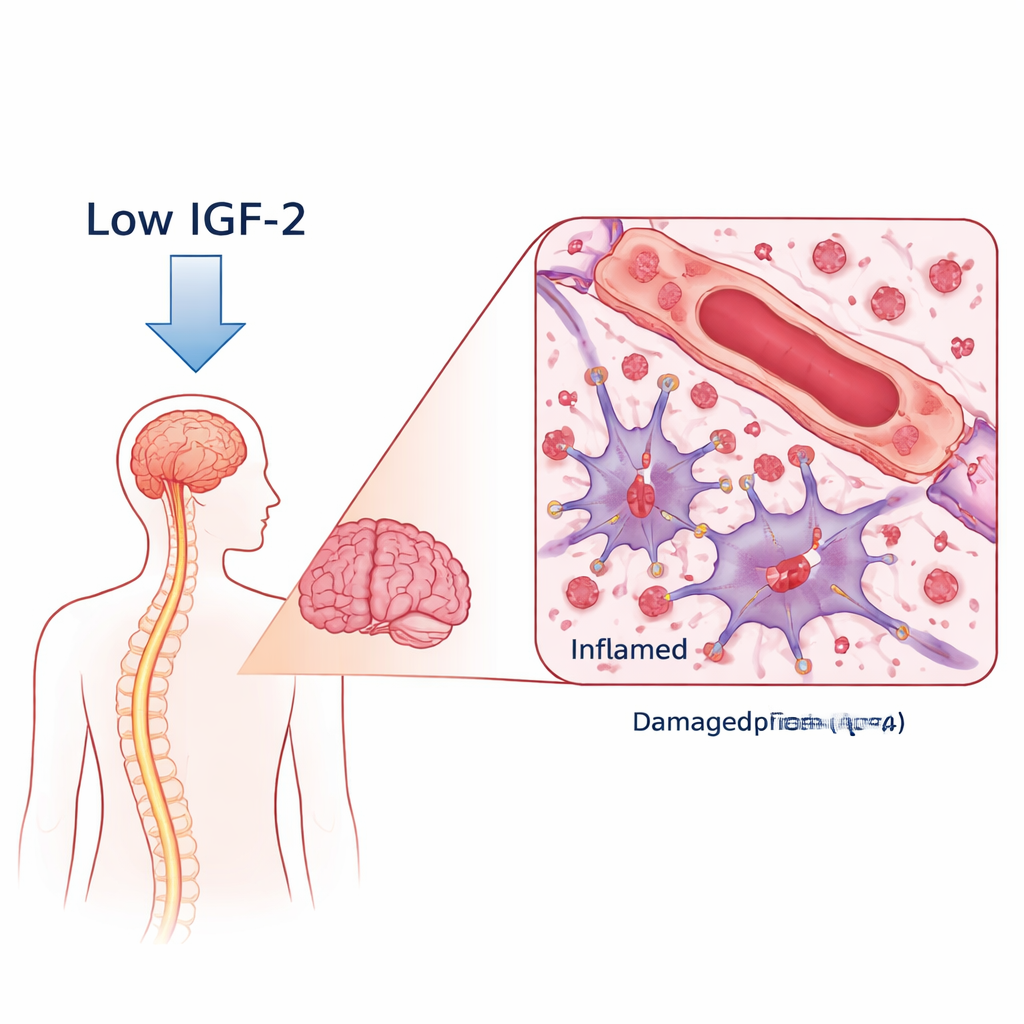
Ein schädlicher Antikörper und ein fehlender Schutzfaktor
Bei NMOSD bildet der Körper Antikörper gegen ein Wasserkanalprotein namens AQP4, das auf den sternförmigen Stützzellen des Gehirns, den Astrozyten, sitzt. Wenn diese Antikörper binden, lösen sie Immunangriffe aus, die Astrozyten schädigen, Myelin (die Isolationsschicht der Nerven) entfernen und Neurone beschädigen können. Die Forschenden verglichen Blutproben von Frauen mit AQP4‑Antikörper-positivem NMOSD mit denen gesunder Freiwilliger. In einer breit angelegten Proteinanalyse fanden sie deutlich niedrigere IGF‑2-Spiegel bei NMOSD-Patientinnen, während zwei IGF-bindende Proteine, die IGF‑2 binden können, erhöht waren. Wichtig: Patientinnen mit den niedrigsten IGF‑2-Werten zeigten tendenziell stärkere Behinderungen und schlechtere Leistungen bei Denk- und Gedächtnistests, was dieses Molekül mit Krankheitsschwere und kognitiver Gesundheit verbindet.
Standardbehandlung fördert die Erholung von IGF-2
Viele NMOSD-Patientinnen erhalten Rituximab, ein Medikament, das die Antikörper-produzierenden B-Zellen entfernt. Das Team bestimmte Blutproteine vor und nach der Rituximab-Behandlung. Nach der Therapie stiegen die IGF‑2-Spiegel und die bindenden Proteine fielen, sodass sich ein Muster einstellte, das dem bei gesunden Personen näherkam. Das legt nahe, dass das Beruhigen des Immunsystems dem Körper erlaubt, einige seiner schützenden Faktoren wiederherzustellen. Obwohl Rituximab nicht gezielt auf IGF‑2 wirkt, deutet die Verschiebung dieses Moleküls darauf hin, dass es Teil der Erholungsreaktion des Körpers sein könnte und dass die Messung von IGF‑2 helfen könnte, den Verlauf der Patientinnen im Zeitverlauf zu verfolgen.
Prüfung von IGF-2 in einem Mausmodell der Erkrankung
Um zu prüfen, ob IGF‑2 mehr tun kann als nur den Schweregrad anzuzeigen, liefen die Forschenden Experimente in einem Mausmodell. Sie injizierten menschliche AQP4-Antikörper und menschliches Komplement in die Gehirne von Mäusen, was wichtige Merkmale von NMOSD nachbildete: Verlust von AQP4 auf Astrozyten, Entzündung, Myelinverlust und Gliederschwäche. Einer anderen Mäusegruppe wurde vorab ein harmloses Virus verabreicht, das ihre Gehirnzellen dazu brachte, zusätzliches IGF‑2 zu produzieren. Diese Mäuse mit erhöhtem IGF‑2 verloren weniger Gewicht, zeigten mildere Bewegungsstörungen und wiesen in Gehirn- und Rückenmarkgewebe weniger Myelinverlust und Entzündung auf. Auch die Standardbehandlung mit Rituximab half, aber die Überexpression von IGF‑2 schien das Gewebe direkter zu schützen, was auf eine neuroprotektive Rolle hinweist und nicht nur auf eine immunsuppressive Wirkung.
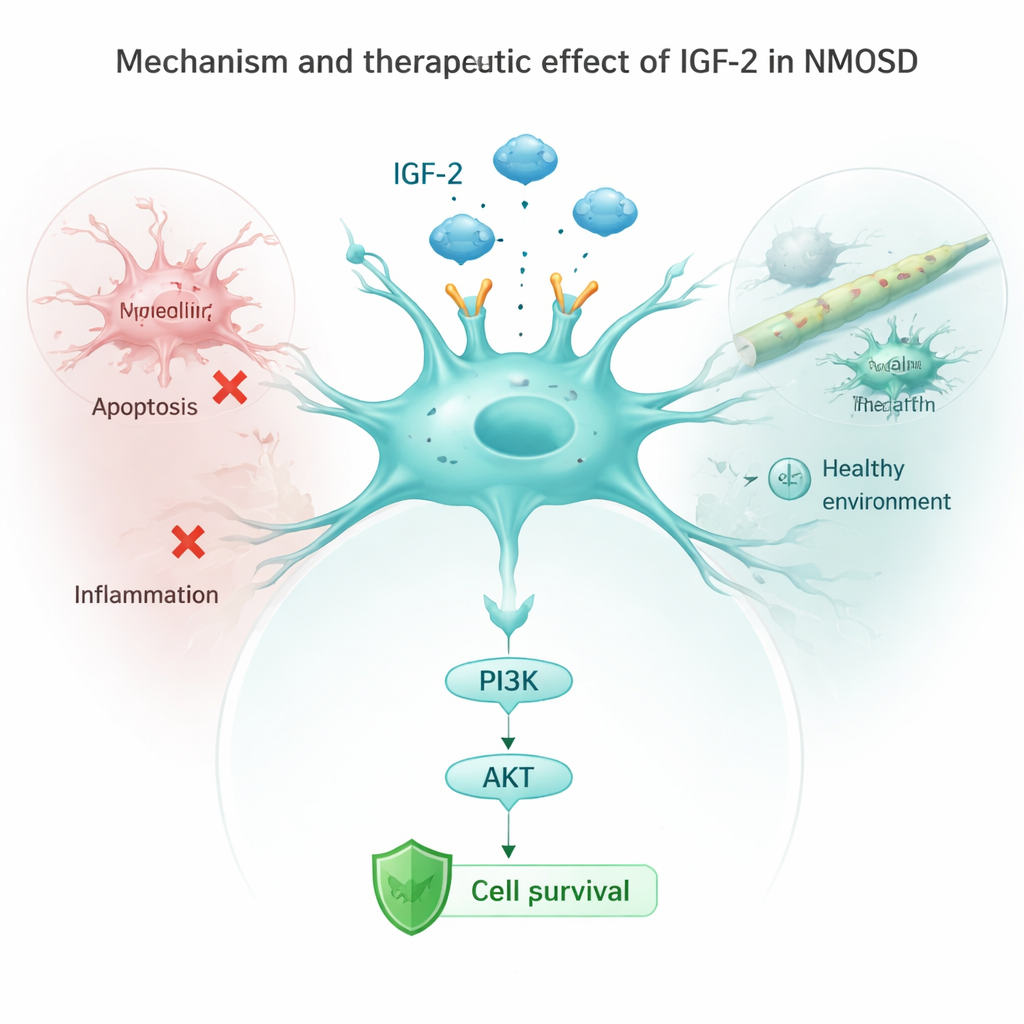
Wie IGF-2 Zelltod und Entzündung dämpft
Das Team untersuchte dann Astrozyten in Zellkulturen, die NMOSD-Antikörpern ausgesetzt wurden. Normalerweise senkten diese Antikörper die Spiegel eines wichtigen Rezeptors, IGF‑1R, und dämpften einen nachgeschalteten Schutzweg, bekannt als PI3K/AKT, während sie „Selbstzerstörungs“-Proteine und entzündliche Signale aktivierten. Wenn die Forschenden Astrozyten zwangen, mehr IGF‑2 zu produzieren, wurde dieser Schutzweg wieder aktiviert, Marker für Zelltod nahmen ab und die Zellen setzten weniger entzündliche Moleküle wie IL‑1β, IL‑6 und TNF‑α frei. Das Blockieren des IGF‑1R-Rezeptors hob diese Vorteile teilweise auf, was zeigt, dass IGF‑2 hauptsächlich durch Aktivierung der IGF‑1R/PI3K/AKT-Kette in Astrozyten wirkt. In lebenden Mäusen verringerte die Erhöhung von IGF‑2 außerdem die Aktivierung von Mikroglia, den Immunwächtern des Gehirns, und senkte entzündliche Signale im Blutkreislauf.
Was das für Patientinnen und Patienten bedeuten könnte
Zusammengefasst deuten diese Ergebnisse darauf hin, dass niedriges IGF‑2 sowohl ein Warnsignal als auch eine verpasste Chance bei NMOSD ist. Patientinnen mit weniger IGF‑2 sind tendenziell stärker beeinträchtigt und zeigen schlechtere kognitive Leistungen, während die Wiederherstellung oder Erhöhung von IGF‑2 in experimentellen Modellen Astrozyten das Überleben erleichtert, Gehirnentzündungen reduziert und Nervenschäden verringert. Obwohl diese Arbeiten vorläufig sind und auf wenigen Patientenproben sowie Tierversuchen basieren, machen sie IGF‑2 zu einem vielversprechenden Ziel für zukünftige Therapien, die nicht nur den Immunangriff abschwächen, sondern auch empfindliche Gehirnzellen direkt schützen würden.
Zitation: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
Schlüsselwörter: Neuromyelitis optica, Astrozyten, IGF-2, Neuroinflammation, Neuroprotektion