Clear Sky Science · de
Integration von Netzwerkgiftigkeitsforschung, maschinellem Lernen und Molekulardynamiksimulationen zur Aufklärung der dualen Wirkmechanismen von Tanshinon IIA bei TNBC und Doxorubicin‑induziertem Kardiotoxizität
Warum diese Forschung für Patientinnen und Patienten wichtig ist
Doxorubicin ist ein Schlüsselmedikament bei Brustkrebs, hat jedoch einen ernsten Nachteil: Es kann das Herz schädigen, teilweise Jahre nach Abschluss der Therapie. Gleichzeitig braucht triple‑negativer Brustkrebs — eine schwer zu behandelnde Form, die gängige Hormon‑ und Wachstumsfaktorziele nicht aufweist — bessere Therapien. Diese Studie untersucht, ob Tanshinon IIA, ein aus der traditionellen chinesischen Heilpflanze Salvia miltiorrhiza gewonnenes Molekül, das Herz vor Doxorubicin‑Toxizität schützen und zugleich aggressive Brusttumoren bekämpfen könnte, wodurch Chemotherapien potenziell sicherer und wirksamer würden.
Ein Stoff, zwei große Probleme
Doxorubicin hat zahllose Leben gerettet, doch sein Nutzen wird durch dosisabhängige Kardiotoxizität begrenzt: Oberhalb einer bestimmten kumulativen Dosis steigt das Risiko für Herzinsuffizienz drastisch. Kliniker stehen oft vor dem schwierigen Abwägungsproblem, Tumorkontrolle und Herzschutz in Einklang zu bringen. Frühere Laborbefunde deuteten darauf hin, dass Tanshinon IIA die antioxidativen Abwehrmechanismen in Herzmuskelzellen stärken und gleichzeitig Krebszellen direkt abtöten kann, doch die molekularen Grundlagen waren unklar. Die Autoren verfolgten systematisch, wie diese einzelne Verbindung Herzschäden abschwächen und gleichzeitig triple‑negativen Brustkrebs angreifen könnte und schlagen damit eine Brücke zwischen traditioneller Medizin und moderner Präzisionsonkologie. 
Große biologische Datensätze für Herzschutz auswerten
Um den Herzschutz zu verstehen, sammelte das Team zunächst tausende Gene, die mit Kardiotoxizität assoziiert sind, aus mehreren großen Datenbanken und kombinierte diese mit bekannten Proteinzielen von Doxorubicin und Tanshinon IIA. Dreizehn Überschneidungsziele traten zutage — Proteine, die mit Herzschäden in Verbindung standen, mit Doxorubicin interagierten und potenziell durch Tanshinon IIA moduliert werden könnten. Mithilfe von Protein‑Protein‑Interaktionsnetzwerken reduzierten die Forscher diese auf sechs Kernspieler, darunter CCND1 (ein Zellzyklusregulator), APAF1 (Auslöser des programmierten Zelltods), AR (Androgenrezeptor), TERT (wichtig für den Schutz von Chromosomenenden), MMP2 (ein Gewebsumbauenzym) und NQO1 (ein antioxidatives Enzym). Rechnersimulationen zum Andocken (Docking) und Molekulardynamik‑Simulationen deuteten darauf hin, dass sowohl Doxorubicin als auch Tanshinon IIA eng an diese Proteine binden können, wobei die Tanshinon IIA–Protein‑Komplexe oft stabiler und energetisch günstiger sind. Das legt nahe, dass die pflanzliche Verbindung Doxorubicins schädliche Signale im Herzen umlenken oder abschwächen könnte.
Aufspüren der Wirkung gegen aggressive Brusttumoren
Auf der Krebsseite konzentrierten sich die Forschenden auf Genexpressionsdatensätze des triple‑negativen Brustkrebses. Sie verglichen Tumorproben mit normalem Brustgewebe, um Hunderte von Genen zu identifizieren, die ungewöhnlich hoch- oder runterreguliert waren. Anschließend nutzten sie eine Methode namens gewichtete Genkoexpressionsnetzwerkanalyse, um Gencluster zu finden, die am engsten mit dem triple‑negativen Phänotyp verknüpft waren. Durch die Schnittmenge dieser Krebsgene mit vorhergesagten Zielen von Tanshinon IIA reduzierten sie die Liste auf wenige Kandidaten und führten drei unabhängige maschinelle‑Lern‑Verfahren durch, um zu ermitteln, welche Gene Tumor und normales Gewebe am besten unterscheiden und klinisch relevant sind. Konvergente Belege hoben ein einzelnes Schlüsselziel hervor: EZH2, ein Gen, das DNA verpackt und in aggressiven Tumoren häufig überaktiv ist.
Verbindung von Tumorbiologie und Immunsystem
Um die Bedeutung von EZH2 bei Patientinnen besser einzuordnen, untersuchten die Forschenden große Krebsdatenbanken. Sie fanden, dass EZH2 in invasiven Brusttumoren deutlich aktiver ist als im normalen Brustgewebe. Zwar zeigte seine Expression nicht durchgängig einen klaren Zusammenhang mit dem Gesamtüberleben bei allen Brustkrebserkrankungen, doch war EZH2 stark mit Eigenschaften des immunologischen Tumormikromilieus verbunden. Höhere EZH2‑Werte korrelierten mit einer stärkeren Infiltration bestimmter Immunzelltypen — etwa B‑Zellen und T‑Zellen — sowie mit einer erhöhten Expression von Molekülen, die sowohl Immunantworten anregen als auch unterdrücken, einschließlich bekannter Checkpoint‑Proteine wie CTLA‑4 und LAG‑3. Diese Muster deuten darauf hin, dass EZH2 an einem Schnittpunkt von Tumorwachstum und Immunregulation steht und dass ein Wirkstoff wie Tanshinon IIA durch Beeinflussung von EZH2 helfen könnte, die Immunerkennung und -abwehr gegen triple‑negativen Brustkrebs neu zu gestalten. 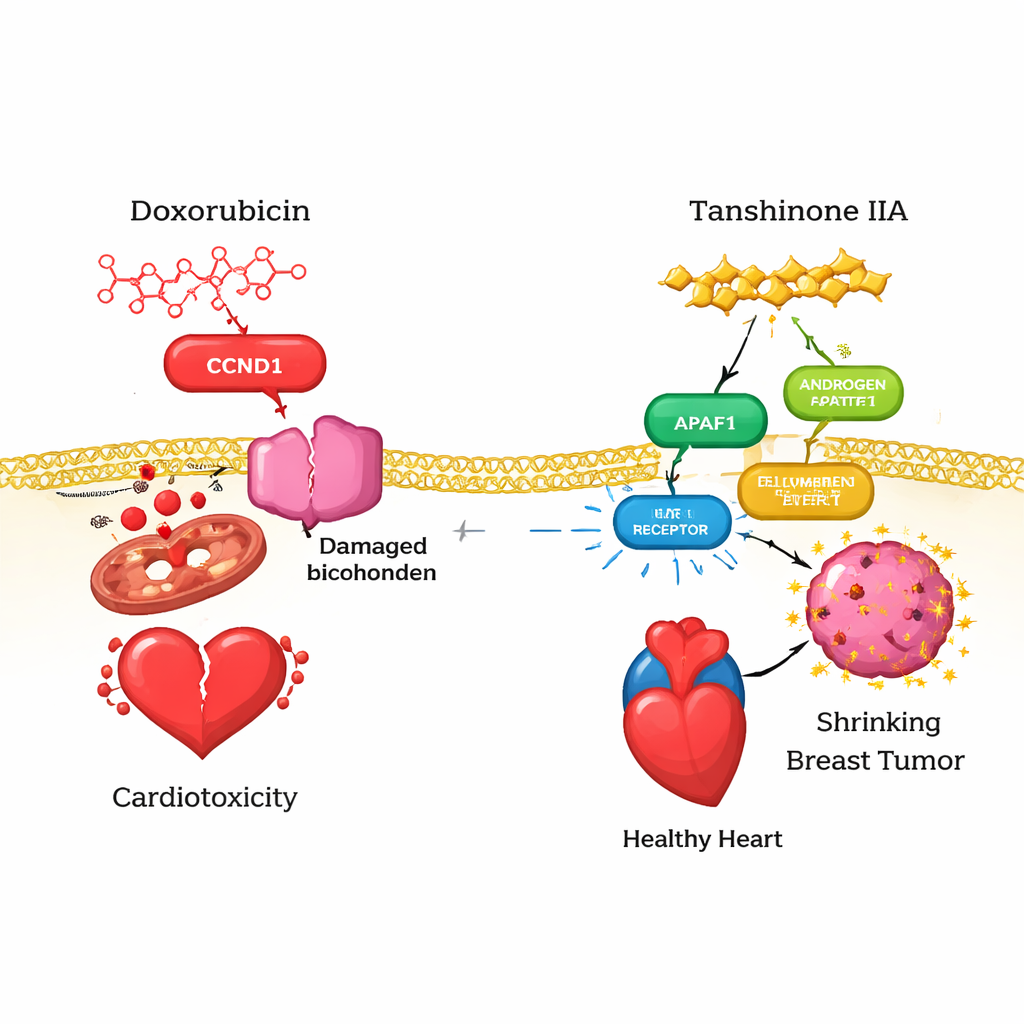
Was das für zukünftige Behandlungen bedeuten könnte
Einfach gesagt schlägt diese Arbeit vor, dass Tanshinon IIA eine doppelte Rolle in der Brustkrebsbehandlung spielen könnte: Zum einen als eine Art „chemischer Schutzschild“, der Doxorubicin‑bedingte Herzschäden verringert, indem er wichtige herzschützende Proteine stabilisiert; zum anderen als gezielte Waffe gegen triple‑negativen Brustkrebs durch seine Wirkung auf EZH2 und zugehörige Immunwege. Die Befunde beruhen auf computergestützten und statistischen Analysen und nicht auf Tier‑ oder Studien am Menschen, daher sind sie ein frühes Konzept und keine sofort einsatzbereite Therapie. Dennoch liefern sie eine detaillierte molekulare Roadmap für die Entwicklung kombinierter Behandlungsansätze, die die lebensrettende Wirkung von Doxorubicin erhalten und gleichzeitig dessen langfristige Risiken mindern — und für die Übersetzung eines traditionellen Pflanzenwirkstoffs in ein modernes, wirkmechanismusgesteuertes Krebsadjunktum.
Zitation: Wu, B., Lan, Xh., Chen, Xq. et al. Integrating network toxicology, machine learning, and molecular dynamics simulations to reveal tanshinone iia’s dual mechanisms in TNBC and doxorubicin-induced cardiotoxicity. Sci Rep 16, 6861 (2026). https://doi.org/10.1038/s41598-026-37428-8
Schlüsselwörter: Tanshinon IIA, Doxorubicin‑Kardiotoxizität, Triple‑negativer Brustkrebs, EZH2, Netzwerkpharmakologie