Clear Sky Science · de
Metabolomische Analyse zeigt Erschöpfung von Aminosäuren und Energiemetaboliten in der Skelettmuskulatur nach ischämischer akuter Nierenschädigung bei Mäusen
Warum verletzte Nieren Ihre Kraft rauben können
Menschen mit plötzlichem Nierenversagen bemerken oft ein Symptom, das scheinbar nichts mit Urin‑ oder Blutwerten zu tun hat: ihre Muskeln fühlen sich schwach an und die Erholung verläuft langsam. Diese Studie stellt eine einfache, aber wichtige Frage – was geschieht bei plötzlicher Nierenschädigung tatsächlich mit den Brennstoffen und Bausteinen in unseren Muskeln? Anhand einer detaillierten chemischen Bestandsaufnahme der Muskeln von Mäusen zeigen die Forschenden, dass akute Nierenschädigung einen körperweiten Abfluss wichtiger Nährstoffe und Energiemoleküle auslöst und die Skelettmuskulatur in einen erschöpften, energiearmen Zustand versetzt.
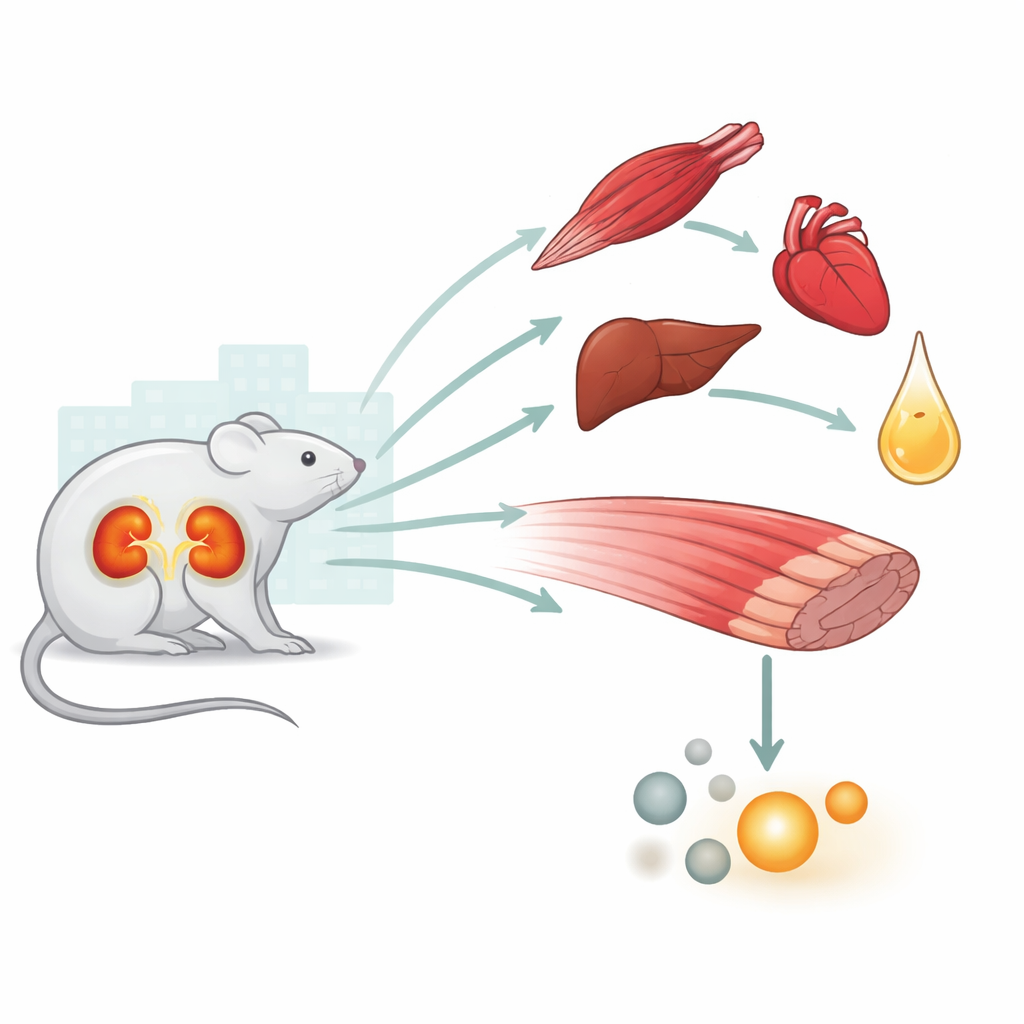
Eine Ganzkörperkrise, nicht nur ein Nierenproblem
Akute Nierenschädigung (AKI) ist bei hospitalisierten und kritisch kranken Patienten weit verbreitet und stark mit einem erhöhten Sterberisiko verknüpft. Ärztinnen und Ärzte beobachten seit langem, dass AKI einem Ganzkörper‑Stresszustand ähnelt und Herz, Lunge, Leber, Gehirn und Muskeln beeinträchtigt. Frühere Arbeiten dieser Gruppe zeigten, dass nach vorübergehendem Verlust der Nierendurchblutung bei Mäusen Herz, Leber, Lunge und die Nieren selbst chemische Zeichen von Energiemangel und oxidativem Stress aufwiesen. Aufbauend darauf konzentriert sich die aktuelle Studie auf die Skelettmuskulatur, ein bedeutendes Reservoir für Kohlenhydrate und Aminosäuren, auf das der Körper in schweren Stresssituationen zurückgreifen kann.
Wie die Studie an Mäusen durchgeführt wurde
Die Forschenden erzeugten ischämische AKI bei jungen erwachsenen männlichen Mäusen, indem sie kurzzeitig beide Nierengefäße abklemmen und anschließend die Durchblutung wiederherstellen ließen. Diese Tiere wurden mit sham‑operierten Mäusen und völlig unbehandelten Kontrollen verglichen. Nach 24 und 72 Stunden entnahmen sie einen wichtigen Beinmuskel (den Gastrocnemius) und nutzten einen untargeted Metabolomik‑Ansatz – einen ultrasensiblen chemischen Scan –, um 175 kleine Moleküle zu messen, darunter Aminosäuren, Antioxidantien und energiebezogene Verbindungen. Statistische und mustererkennende Methoden wurden eingesetzt, um zu bestimmen, welche Moleküle sich am stärksten veränderten und wie sich die Muskelchemie zwischen den Gruppen unterschied.
Muskeltreibstoff und Antioxidantien gehen zur Neige
Die markantesten Veränderungen traten 24 Stunden nach der Nierenschädigung auf. Etwa zwei Fünftel aller nachgewiesenen Metaboliten waren verändert, und das Gesamtbild war deutlich: Viele zentrale Verbindungen im Muskel waren im Vergleich zur Sham‑Operation reduziert. Essentielle und nichtessentielle Aminosäuren wie Alanin, Valin, Lysin, Methionin und Tyrosin fielen, ebenso mehrere Moleküle des Harnstoffzyklus (Arginin, Citrullin, Ornithin, Argininosuccinat), die bei der Stickstoffentsorgung helfen und die Kreatinproduktion unterstützen. Das wichtigste zelluläre Antioxidans Glutathion und dessen Bausteine (darunter Methionin und ein Cystein‑Glycin‑Dipeptid) waren ebenfalls vermindert, was auf erhöhten oxidativen Stress hinweist. Energiebezogene Moleküle, einschließlich Kreatin und Zwischenprodukte zentraler Energiestoffwechselwege, zeigten ebenfalls abwärts gerichtete Tendenzen, was nahelegt, dass der Muskel seine eigenen Reserven opfert, um den Rest des Körpers zu unterstützen.
Verbindung zwischen Muskel und anderen Organen
Um das größere Bild zu erfassen, verglich das Team die Muskeldaten mit zuvor erhobenen metabolomischen Profilen von Niere, Leber, Herz und Blutplasma zum gleichen 24‑Stunden‑Zeitpunkt. In all diesen Proben wiederholten sich bestimmte Muster: eine weitreichende Erschöpfung von Glutathion und seinen Vorstufen, niedrigere Alaninwerte und eine konsistente Störung der Arginin‑ und Harnstoffzyklus‑bezogenen Chemie. Gleichzeitig stiegen in mehreren Organen und im Blutkreislauf einige Abbauprodukte, wie Allantoin (ein Marker für oxidativen Stress). Kreatin und seine energiereiche Form Phosphokreatin waren relativ erhöht in Leber, Niere und Blut, obwohl Arginin und Aminosäuren in Muskel und Plasma sanken, was darauf hindeutet, dass die Skelettmuskulatur möglicherweise Substrate exportiert, damit andere Organe – insbesondere die verletzten Nieren – unter Stress weiter Energie produzieren können.
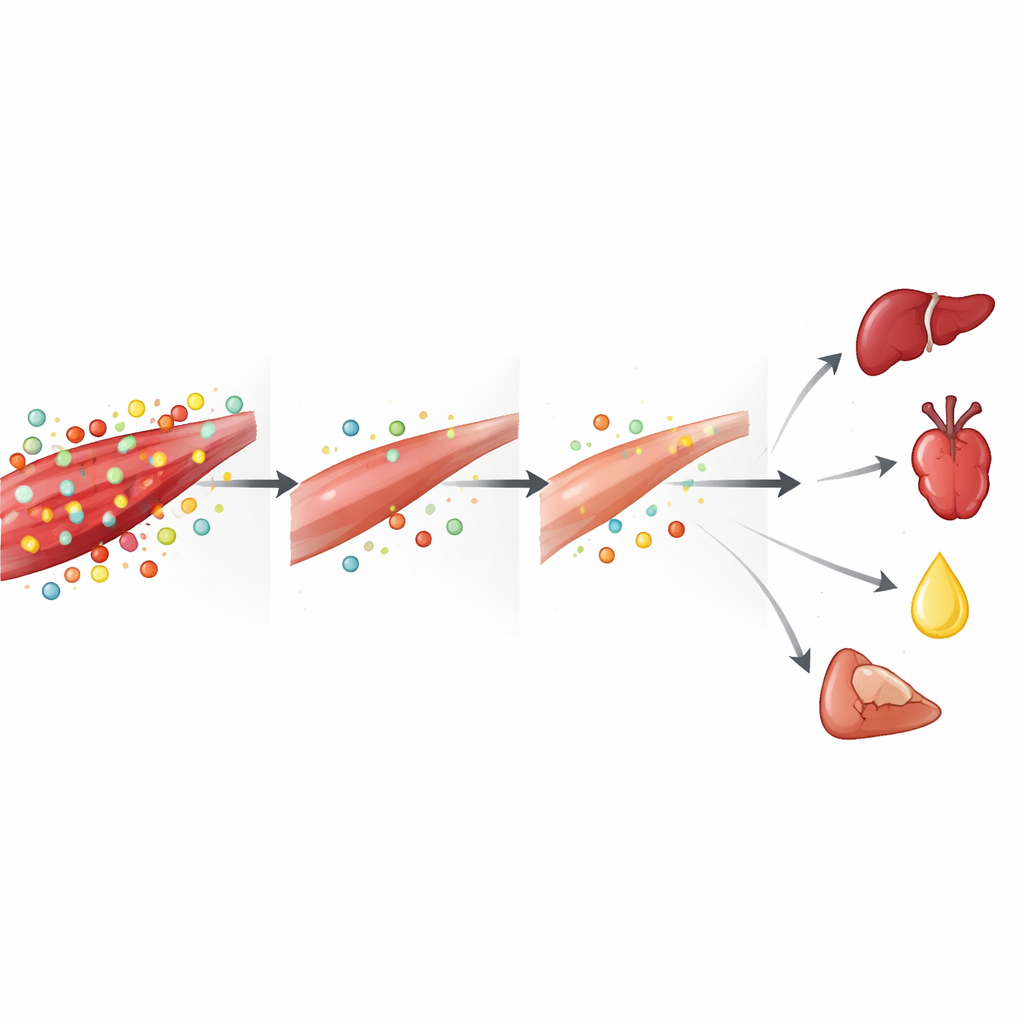
Was das für Patienten und künftige Therapien bedeutet
Alltagsverständlich betrachtet beschreibt die Studie AKI als ein metabolisches „Auskassieren“ des Körpers: Die Skelettmuskulatur baut ihre Protein‑ und Antioxidantienvorräte ab, um lebenswichtige Organe mit Energie und Schutz zu versorgen, wodurch die Muskeln selbst an Treibstoff und Abwehr verlieren. Das erklärt, warum Menschen mit schwerer Nierenschädigung zu Muskelabbau, Schwäche und schlechter funktioneller Erholung neigen. Es eröffnet auch die Möglichkeit, dass gezielte Nährstoffunterstützung – insbesondere Aminosäuren und Verbindungen, die das Glutathion‑ und Kreatin‑Phosphokreatin‑System stärken – eines Tages helfen könnte, sowohl Nieren als auch Muskeln während akuter Erkrankungen zu schützen. Obwohl diese Befunde aus Mäusen stammen und auf chemischen Momentaufnahmen statt auf direkten Flussverfolgungen beruhen, liefern sie eine detaillierte Karte dafür, wie die Muskelchemie durch Nierenschädigung gestört wird, und weisen auf neue Strategien hin, um Kraft zu erhalten und die Prognose bei plötzlichem Nierenversagen zu verbessern.
Zitation: Li, A.S., Baker, P.R., Park, S. et al. Metabolomic assessment reveals depletion of amino acids and energy metabolites in skeletal muscle after ischemic acute kidney injury in mice. Sci Rep 16, 8823 (2026). https://doi.org/10.1038/s41598-026-37424-y
Schlüsselwörter: akute Nierenschädigung, Skelettmuskelstoffwechsel, Aminosäurenmangel, oxidativer Stress, Metabolomik