Clear Sky Science · de
Analyse der systolischen Herzfunktion in PERM1-Knockout-Mäusen anhand großer Tierkohorten
Warum winzige Mausherzen für die menschliche Gesundheit wichtig sind
Herzinsuffizienz wird oft als eine erschöpfte Pumpe beschrieben, doch was ein Herz tatsächlich schwächt, ist überraschend komplex. In dieser Studie nutzten Forschende eine ungewöhnlich große Gruppe von Mäusen, um eine präzise Frage zu stellen: Verändert das Abschalten eines einzelnen Gens namens PERM1, das dafür bekannt ist, Herzmuskelzellen bei der Energieproduktion zu unterstützen, auch die Schlagkraft des Herzens? Durch sorgfältige Untersuchungen der Herzen von mehr als 170 Mäusen zeigen sie, dass dieses Gen das Herz subtil umgestaltet und seine Pumpkraft vermindert, während die Tiere äußerlich weitgehend gesund bleiben. Ihre Ergebnisse helfen, eine Debatte im Feld zu klären, und liefern einen Leitfaden für die Planung besserer Herzexperimente in der Zukunft.
Ein Gen, das Brennstoffnutzung mit Herzkontraktion verbindet
PERM1 wurde zuerst als Schalter identifiziert, der die Energieproduktion in Muskelzellen, einschließlich des Herzens, erhöht. Frühere Arbeiten zeigten, dass die PERM1-Spiegel in versagenden Herzen sowohl bei Mäusen als auch bei Menschen sinken, was die Möglichkeit aufwarf, dass niedriges PERM1 tatsächlich zu schwächeren Herzschlägen beitragen könnte. Studien mit PERM1-Knockout-Mäusen – Tieren, die gezielt ohne dieses Gen erzeugt wurden – hatten jedoch widersprüchliche Ergebnisse geliefert, ob ihre Herzen tatsächlich weniger effektiv pumpen. Da PERM1 als möglicher Zielpunkt für neue Therapien bei Herzversagen angesehen wird, wollten die Autoren seinen Einfluss auf die Herzfunktion mit ausreichend vielen Tieren und strenger Statistik testen, um eine klare Ja-oder-Nein-Antwort zu erhalten.
Ein Blick in kleiner Herzen mit großer Fallzahl
Das Team sammelte Echokardiogramm-Daten – dieselbe Ultraschalltechnik, die in kardiologischen Kliniken verwendet wird – von jeder PERM1-Knockout-Maus und ihrem gesunden Wurfgeschwister, das in ihrem Labor über einen Zeitraum von 18 Monaten eingesetzt wurde. Dieser retrospektive Erfassungszeitraum ergab 84 normale (Wildtyp-) und 88 Knockout-Tiere, eine Stichprobengröße, die deutlich größer ist als üblich in Mausherzstudien. Aus den Ultraschallbildern maßen sie standardisierte Indikatoren für die Funktion des linken Ventrikels, der Hauptpumparterie. Die Schlüsselgröße war die Ejektionsfraktion, der Prozentsatz des mit jedem Schlag ausgeworfenen Bluts, zusammen mit verwandten Messgrößen wie dem Ausmaß der Verkürzung des Ventrikel-Durchmessers bei Kontraktion, der Wanddicke und der insgesamt pro Minute gepumpten Blutmenge.
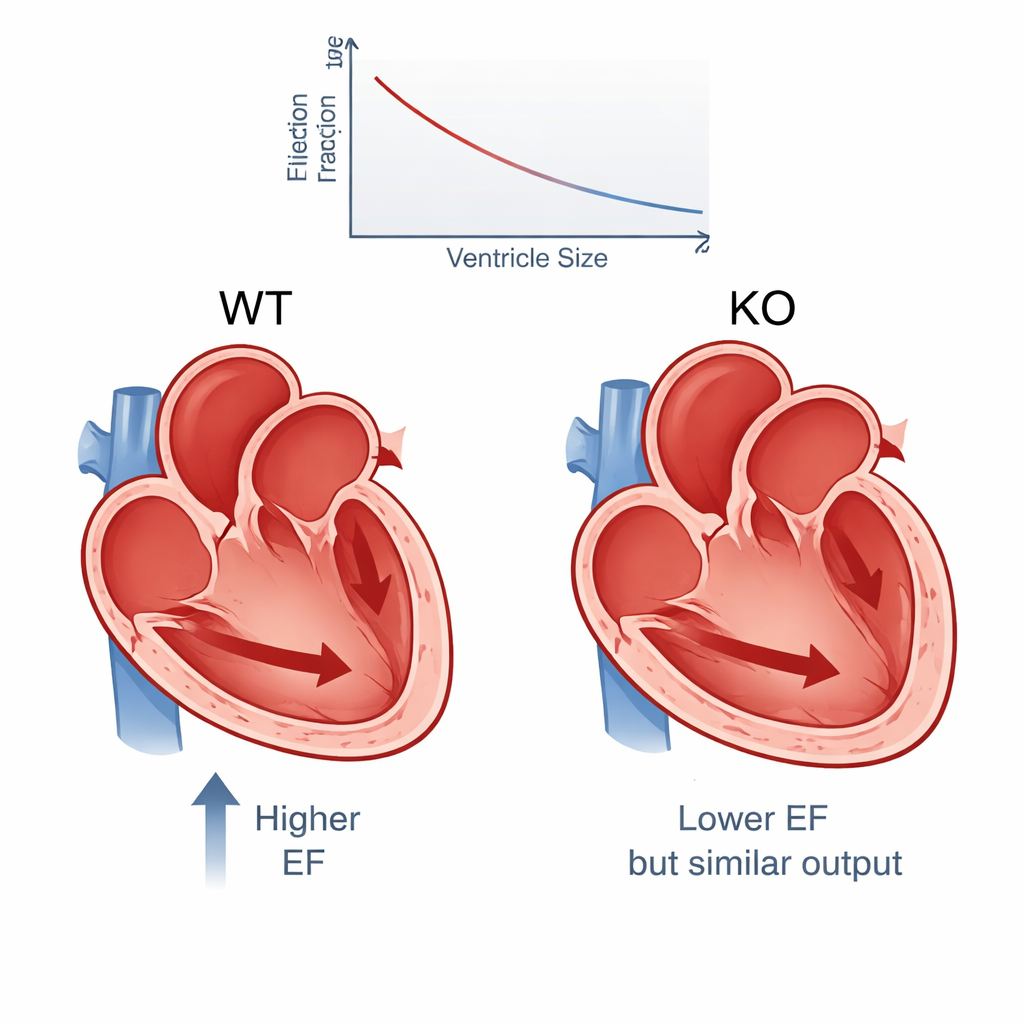
Schwächere Kontraktion, größere Kammer, ähnlicher Auswurf
Die Ergebnisse zeigen ein konsistentes Bild. Im Mittel sank die Ejektionsfraktion von etwa 65 % bei normalen Mäusen auf 54 % bei PERM1-Knockouts – ein Unterschied, der klinisch bei Menschen relevant wäre und statistisch sehr gut abgesichert ist. Andere Kontraktionsmaße, wie die fraktionelle Verkürzung und die Wandverdickung, nahmen ebenfalls ab. Gleichzeitig waren die linken Ventrikel der Knockouts deutlich größer, insbesondere am Ende der Kontraktion, was darauf hindeutet, dass mehr Blut in der Kammer zurückblieb. Trotz dieser schwächeren Kontraktion verringerte sich die insgesamt pro Minute gepumpte Blutmenge nur geringfügig – um etwa 6 % –, weil die vergrößerten Kammern von vornherein mehr Blut fassen konnten. Anders gesagt, das Herz kompensierte die schlechte Kontraktion teilweise durch eine Dehnung seiner Hauptkammer.
Verborgene Vielfalt in „identischen“ Herzen
Da die Studie so viele Tiere einschloss, konnten die Forschenden über Mittelwerte hinaus schauen und untersuchen, wie einzelne Herzen variieren. Sogar unter genetisch identischen, gesunden Mäusen beobachteten sie eine überraschend große Streuung der Ejektionsfraktion. Das Entfernen von PERM1 verschob die gesamte Verteilung nach unten – mehr Herzen mit geringerer Pumpkraft – machte die Streuung selbst jedoch nicht breiter. Etwa 7 % der Knockout-Mäuse hatten eine Ejektionsfraktion unter 40 %, ein Wert, der beim Menschen als Herzinsuffizienz mit reduzierter Ejektionsfraktion gelten würde, doch diese Mäuse hielten dennoch nahezu normale Blutfördermengen aufrecht. Statistische Analysen zeigten, dass Geschlecht, Alter und Körpergewicht nur einen kleinen Teil der Variabilität erklärten; die meisten Unterschiede dürften auf schwerer zu messende biologische Faktoren zurückgehen, wie subtile Umwelteinflüsse oder epigenetische Veränderungen.
Was das für künftige Herzforschung bedeutet
Um anderen Wissenschaftlern bei der Planung besserer Experimente zu helfen, nutzten die Autoren ihren großen Datensatz, um zu berechnen, wie viele Tiere typischerweise benötigt werden, um sinnvolle Änderungen in den einzelnen Herzparametern zu erkennen. Sie fanden heraus, dass die in der Feld üblichen eher kleinen Gruppen reale, aber moderate Effekte leicht übersehen können, besonders bei subtilen Messgrößen wie Schlagvolumen oder Herzzeitvolumen. Insgesamt liefert die Studie starke Hinweise darauf, dass der Verlust von PERM1 ein spezifisches Remodeling des Herzens verursacht – größere Kammern, schwächere Kontraktion – und dass dieses Remodeling teilweise durch strukturelle Veränderungen ausgeglichen wird, die helfen, den Blutfluss zu erhalten. Für Nicht-Spezialisten lautet die Quintessenz, dass ein einzelnes genregulierendes Element der Energieversorgung das Herz in einen neuen Betriebsmodus schieben kann: einen Zustand, der von außen gesund erscheint, aber leisere Veränderungen in Bau und Arbeitsaufwand der Pumpe birgt.
Zitation: Zaitsev, A.V., Sreedevi, K., Goode, B. et al. Analysis of systolic cardiac function in PERM1-knockout mice using large cohorts of animals. Sci Rep 16, 7705 (2026). https://doi.org/10.1038/s41598-026-37420-2
Schlüsselwörter: Herzinsuffizienz, Herzkontraktilität, mitochondriale Energiegewinnung, Mausmodelle, Echokardiographie