Clear Sky Science · de
3D‑heterotypische Modelle des Glioblastoms zeigen den Einfluss von Mikroglia auf die zelluläre Organisation und die Produktion eines charakteristischen Sekretoms
Warum winzige Hirntumore in der Petrischale wichtig sind
Das Glioblastom gehört zu den tödlichsten Hirntumoren, unter anderem weil es nahezu jeder Therapie widersteht, die Ärzte einsetzen. Ein wichtiger Grund für dieses Versagen ist, dass Standard‑Labortests die volle Komplexität eines echten Hirntumors nicht abbilden. In dieser Studie bauen die Forschenden lebensnähere, dreidimensionale „Mini‑Tumore“, die nicht nur Krebszellen, sondern auch Mikroglia – die im Gehirn ansässigen Immunzellen – enthalten. So zeigen sie, wie diese Helfer unauffällig Tumore widerstandsfähiger, invasiver und schwerer zu bekämpfen machen können.
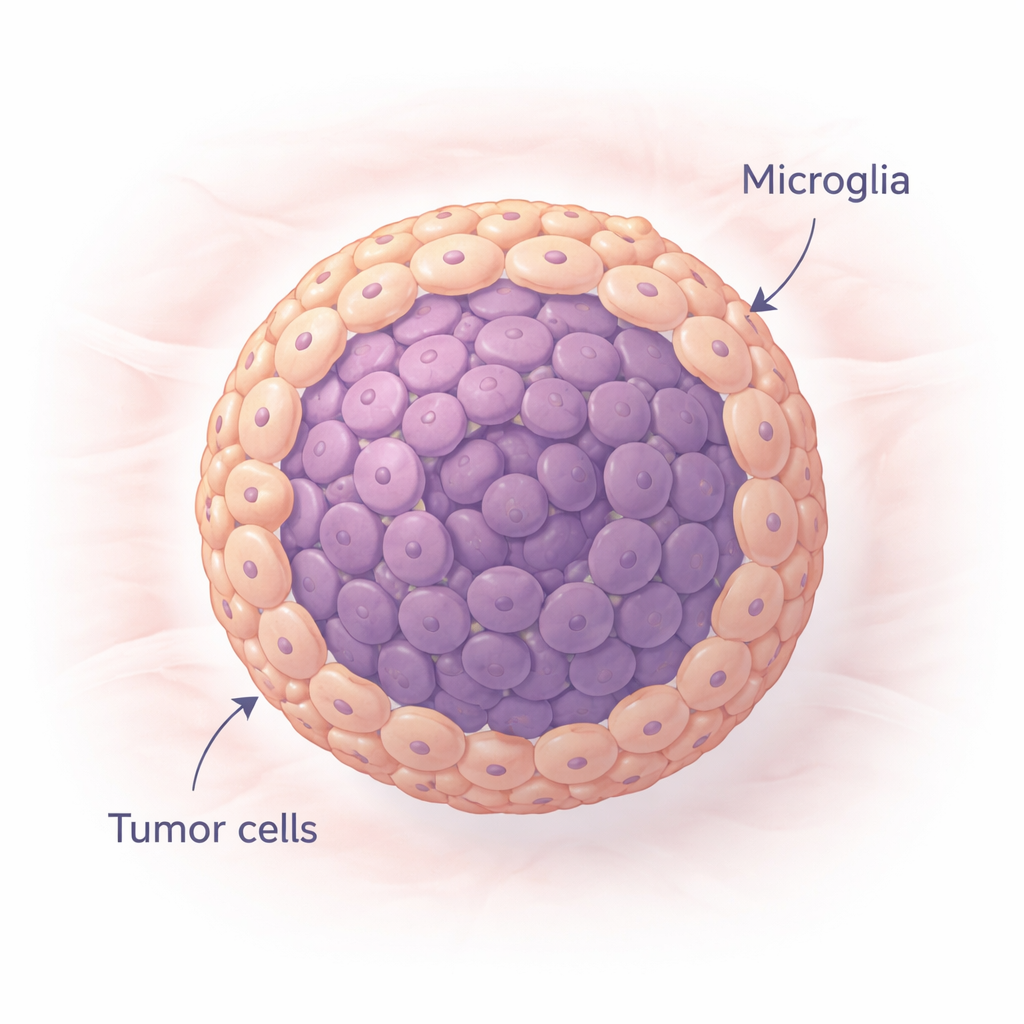
Mini‑Tumore bauen, die sich echter anfühlen
Die Forschenden erzeugten winzige kugelförmige Zellcluster, sogenannte Sphäroide, entweder aus einer gängigen Glioblastom‑Zelllinie oder aus tumorähnlichen Stammzellen, die von einer Patientin oder einem Patienten stammten. Manche Sphäroide enthielten nur Tumorzellen, andere mischten Tumor‑ und Mikrogliazellen in Anteilen, die denen in Patienten ähneln. In speziellen, wenig haftenden Gefäßen klumpten diese Zellen innerhalb einer Woche von selbst zu kompakten Kugeln zusammen und blieben größtenteils lebensfähig. Durch den Vergleich von „nur‑Tumor“ und „Tumor‑plus‑Mikroglia“ Sphäroiden konnte das Team beobachten, wie die zusätzlichen Gehirn‑Immunzellen Wachstum, Struktur und Verhalten veränderten.
Mikroglia als Wachstumsverstärker und Wegbereiter für Invasion
Das Hinzufügen von Mikroglia veränderte das Wesen der Mini‑Tumore. Gemischte Sphäroide wuchsen größer und enthielten mehr Zellen als reine Tumorsphäroide, was zeigt, dass Mikroglia das Gesamtwachstum unterstützten. In Modellen mit patientenabgeleiteten Zellen bildeten diese gemischten Sphäroide sogar mehrere dichte Zentren aus, ein Merkmal, das mit aggressivem Krankheitsverlauf verknüpft ist. Sobald die Sphäroide auf ein weiches Gel gesetzt wurden, das Hirngewebe nachahmt, breiteten sich Zellen aus den gemischten Sphäroiden ausdauernder aus, insbesondere bei einer Tumorzelllinie. Die Verfolgung der wandernden Zellen zeigte, dass Mikroglia oft vorneweg an den Rändern führten – ein Echo dessen, wie sie sich um echte Glioblastom‑Massen sammeln und Wege ins umliegende Gehirngewebe öffnen.
Eine schützende Hülle, die Chemotherapie abschwächt
Als Nächstes testete das Team das Standardmedikament Temozolomid, das in der Glioblastom‑Behandlung weit verbreitet ist. Reine Tumorsphäroide verloren nach der Medikamentenexposition viele Zellen, was auf erhebliche Schäden hindeutete. Im Gegensatz dazu behielten gemischte Sphäroide deutlich mehr Zellen und erholten sich in einigen Fällen innerhalb von 48 Stunden sogar mit höheren Zellzahlen. Hochauflösende Bildgebung erklärte warum: In den gemischten Modellen konzentrierten sich Gliomzellen im Zentrum, während Mikroglia eine umgebende Hülle bildeten. Diese Kern‑und‑Hülle‑Architektur wirkte wie ein lebender Schild und erschwerte es dem Medikament, den Tumorkern zu erreichen und abzutöten. Messungen der Zellzusammensetzung vor und nach der Behandlung zeigten, dass Tumorzellen bevorzugt verloren gingen, während Mikroglia überlebten und relativ häufiger wurden – ein Effekt, der den Schutz verstärkte.
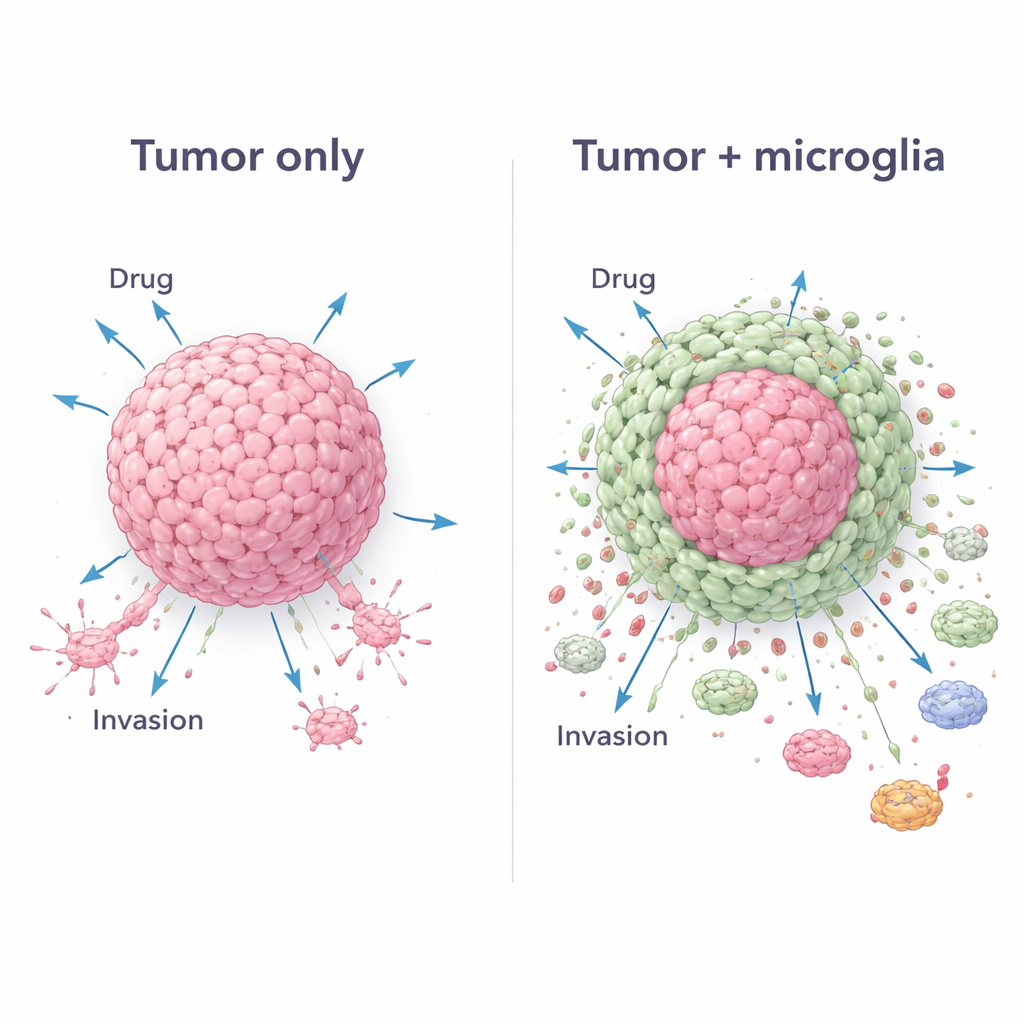
Die Abwehrkräfte des Körpers zugunsten des Tumors umlenken
Glioblastome überleben auch, indem sie das Immunsystem kapern. Um das zu untersuchen, setzten die Forschenden aus dem Blut gewonnene menschliche Immunzellen der Flüssigkeit aus, die aus den Sphäroiden gesammelt wurde. Die Flüssigkeit aus gemischten Tumor‑Mikroglia‑Sphäroiden bewirkte, dass viele dieser Zellen zur Ruhe kamen und einen „M2‑ähnlichen“ Zustand annahmen, einen anti‑entzündlichen Modus, der dafür bekannt ist, Tumorwachstum zu unterstützen statt zu bekämpfen. In Migrationsversuchen wanderten mehr zirkulierende Immunzellen auf die gemischten Sphäroide zu als auf reine Tumorsphäroide, was auf starke chemische Lockstoffe hindeutet. Eine breit angelegte Analyse sekretierter Proteine bestätigte, dass gemischte Sphäroide ein charakteristisches Signalcocktail freisetzten, das mit Invasion, Therapieresistenz und Immunsuppression verknüpft ist – eine Signatur, die fehlt, wenn die Zelltypen allein kultiviert werden.
Was das für künftige Hirntumorbehandlungen bedeutet
Für Nicht‑Spezialisten ist die Kernbotschaft: Glioblastom lässt sich nicht allein durch das Studium isolierter Krebszellen verstehen. Diese Arbeit zeigt, dass Tumorzellen und Mikroglia in 3D zusammengenommen eine Selbstorganisation bilden, bei der ein Tumorkern von einer Mikroglia‑Hülle umgeben ist, die Wachstum fördert, Ausbreitung unterstützt, Chemotherapie abschwächt und einströmende Immunzellen dazu verleitet, eher zu helfen als zu bekämpfen. Diese realistischen Mini‑Tumore erfassen viele Kennzeichen echter Glioblastome, besonders wenn patientenabgeleitete Zellen verwendet werden. Damit bieten sie eine leistungsfähige Testumgebung für die Entwicklung von Medikamenten, die nicht nur Tumorzellen angreifen, sondern auch ihre gefährliche Allianz mit Mikroglia stören — und so möglicherweise wirksamere Therapien näher an die Patienten bringen.
Zitation: García-Sáez, C., Alonso-Marañón, J., García-Puga, M. et al. 3D heterotypic models of glioblastoma reveal the impact of microglia on cellular organization and the production of a distinct secretome. Sci Rep 16, 7246 (2026). https://doi.org/10.1038/s41598-026-37395-0
Schlüsselwörter: Glioblastom, Mikroglia, 3D‑Tumormodelle, Medikamentenresistenz, Tumormikroumgebung