Clear Sky Science · de
Identifizierung und Charakterisierung fibroblasten‑bezogener Biomarker und proinflammatorischer Subpopulationen bei Parodontitis durch integrierte transkriptomische und Einzelzellanalyse
Warum Ihr Zahnfleisch mehr zählt als nur Ihr Lächeln
Blutendes Zahnfleisch und lockere Zähne wirken vielleicht wie kleine Probleme, aber chronische Zahnfleischerkrankungen – bekannt als Parodontitis – können den Kieferknochen schädigen, zum Zahnverlust führen und stehen in Verbindung mit Erkrankungen wie Herzkrankheiten und Diabetes. Diese Studie untersucht genau eine häufig übersehene Zellgruppe im Zahnfleisch, die Fibroblasten, um zu verstehen, wie sie Entzündungen antreiben oder dämpfen. Durch die Kombination großer Genomdatenbestände mit Einzelzellanalysen entdecken die Forschenden neue Warnsignale und Zelltypen, die die Diagnostik und Behandlung von Zahnfleischerkrankungen verbessern könnten.
Versteckte Akteure bei schmerzhaftem Zahnfleisch
Fibroblasten sind die Arbeitstiere, die das Bindegewebe aufbauen und erhalten, das die Zähne an Ort und Stelle hält. Lange galten sie hauptsächlich als strukturelles "Gerüst". Diese Forschung zeigt, dass sie weit mehr sind: Fibroblasten können wie kleine Steuerzentralen für Entzündungen fungieren. Wenn Bakterien das mikrobielle Gleichgewicht in der Mundhöhle stören, reagieren Fibroblasten, indem sie chemische Botenstoffe freisetzen, die Immunzellen anziehen und entweder bei der Gewebereparatur helfen oder die Schäden verschärfen können. Die Autorinnen und Autoren konzentrierten sich darauf, fibroblasten‑bezogene Gen‑Signale zu finden, die sich zwischen gesundem Zahnfleisch und Parodontitis unterscheiden, und Untergruppen von Fibroblasten zu identifizieren, die im erkrankten Gewebe besonders proinflammatorisch werden.
Gewebe‑Scan: Zelle für Zelle
Dafür wertete das Team mehrere große Genexpressionsdatensätze von Patientinnen und Patienten mit gesundem Zahnfleisch und Parodontitis aus sowie einen modernen Einzelzell‑Sequenzierungsdatensatz, der Tausende einzelner Zellen abbildet. Zuerst kartierten sie die wichtigsten Zelltypen im Zahnfleisch – etwa Immunzellen, Gefäßzellen und Fibroblasten – und bestätigten, dass Anzahl und Aktivität von Fibroblasten in erkranktem Gewebe erhöht sind. Anschließend suchten sie nach Genen, die sowohl bei Parodontitis verändert als auch spezifisch mit Fibroblasten verbunden sind. Mit einer statistischen Methode, die die informativsten Merkmale eingrenzt, identifizierten sie sechs zentrale fibroblasten‑bezogene Gene, deren kombiniertes Aktivitätsmuster zuverlässig Parodontitis von gesundem Gewebe über mehrere Patientengruppen hinweg unterscheidet.
Risikomuster und immunologische „Persönlichkeiten“ der Zahnfleischerkrankung
Anhand dieser sechs Gene bauten die Forschenden ein diagnostisches Modell, das Krankenproben gut von gesunden Proben trennte, und überführten es in eine einfache Punkteskala – ein sogenanntes Nomogramm –, das prinzipiell das individuelle Risiko abschätzen könnte. Als sie Patientinnen und Patienten danach gruppierten, wie stark diese Fibroblasten‑Gene exprimiert waren, traten drei unterschiedliche Formen der Parodontitis hervor. Eine Form zeigte eine stark entzündliche Immunlandschaft, reich an aggressiven T‑Zellen und „Angriffsmodus“‑Makrophagen. Eine zweite Form war von Zellen geprägt, die Immunreaktionen dämpfen, was auf ein eher unterdrücktes Milieu hindeutet. Eine dritte Form lag dazwischen, mit einer ausgewogeneren oder ruhenden Mischung von Immunzellen. Diese Muster deuten darauf hin, dass nicht alle Zahnfleischerkrankungen gleich sind und dass Fibroblasten helfen, diese verschiedenen "Persönlichkeiten" der Entzündung zu formen.
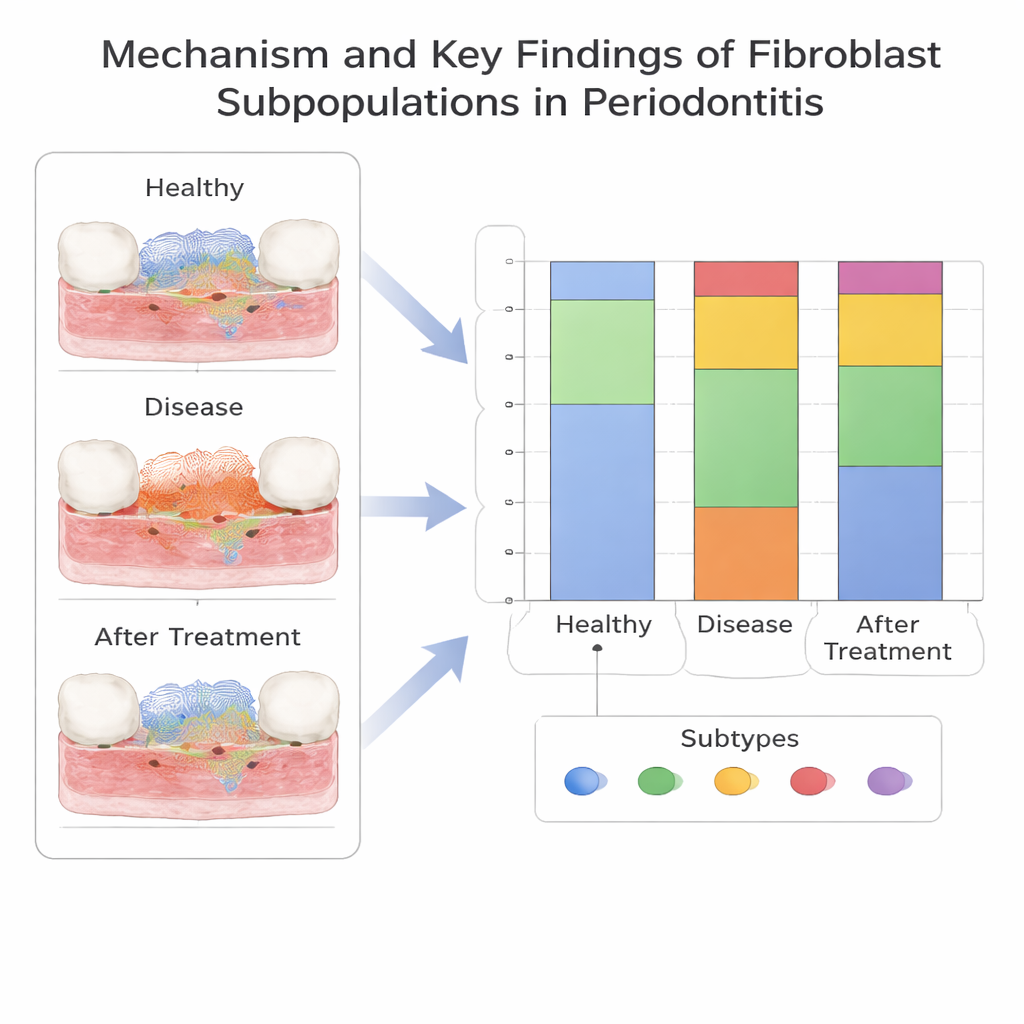
Ein neuer proinflammatorischer Fibroblasten‑Subtyp
Tiefergehend auf Einzelzellebene teilte das Team die Fibroblasten anhand ihrer Genaktivität in fünf Subtypen ein. Ein Subtyp, gekennzeichnet durch das Gen CXCL13, fiel auf, weil er bei Parodontitis deutlich häufiger vorkam als im gesunden Zahnfleisch. Diese CXCL13‑positiven Fibroblasten erschienen früh auf einem Entwicklungsweg und waren mit Signalen verbunden, die Immunzellen anlocken und die Gewebsmatrix umgestalten – Merkmale, die für eine starke proinflammatorische Rolle sprechen. Im Gegensatz dazu war ein anderer Fibroblasten‑Subtyp im gesunden Gewebe angereichert und könnte helfen, das Zahnfleischmilieu stabil zu halten. Die Autorinnen und Autoren bestätigten in Patientenproben, dass bestimmte fibroblasten‑bezogene Gene, insbesondere SELL, sowie die CXCL13‑positiven Fibroblasten selbst in erkranktem Gewebe tatsächlich erhöht sind, was die rechnerischen Befunde stützt.
Was das für die zukünftige Zahnfleischversorgung bedeutet
Einfach gesagt zeigt die Studie, dass einige Fibroblasten im Zahnfleisch wie Beschleuniger der Entzündung wirken, während andere eher als Bremsen oder Reparaturtruppen fungieren. Durch die Identifizierung präziser Genmarker und eines klaren proinflammatorischen Fibroblasten‑Subtyps öffnet die Arbeit die Tür für genauere Tests, die Parodontitis früher und zuverlässiger anzeigen. Sie legt auch nahe, dass künftige Therapien diese spezifischen fibroblastengetriebenen Wege anvisieren könnten – indem man schädliche Subsets wie CXCL13‑positive Fibroblasten dämpft oder schützende Subtypen stärkt –, um Zahnfleischentzündungen effektiver zu kontrollieren und möglicherweise ihre Auswirkungen auf die Gesamtgesundheit zu verringern.
Zitation: Huang, M., Lin, Y., Wu, Z. et al. Identification and characterization of fibroblast-related biomarkers and pro-inflammatory subpopulations in periodontitis by integrated transcriptomic and single-cell analysis. Sci Rep 16, 6223 (2026). https://doi.org/10.1038/s41598-026-37385-2
Schlüsselwörter: Parodontitis, Fibroblasten, Zahnfleischentzündung, Einzelzell‑RNA‑Sequenzierung, Biomarker