Clear Sky Science · de
Design und Immunogenität eines rekombinanten Saccharomyces boulardii, das das P2‑VP8-Subunit-Rotavirus-Impfstofffragment sezerniert
Warum eine darmfreundliche Hefe für die Gesundheit von Kindern wichtig sein könnte
Rotavirus ist eine Hauptursache für schwere Durchfallerkrankungen bei Kleinkindern, besonders in Ländern mit niedrigem Einkommen, in denen medizinische Versorgung schwerer zugänglich ist. Bestehende Impfstoffe retten viele Leben, sind in diesen Umgebungen jedoch weniger wirksam und müssen von der Fabrik bis zur Klinik gekühlt werden. Diese Studie untersucht einen sehr anderen Impfstoffansatz: eine übliche probiotische Hefe in eine winzige Fabrik zu verwandeln, die im Darm ein Rotavirus‑Protein freisetzt, mit der Hoffnung, Schutz in einer leicht zu verabreichenden, stabilen Form auszulösen.
Aus einer nützlichen Mikrobe ein Impfstoff‑Liefervehikel machen
Die Forschenden konzentrierten sich auf Saccharomyces boulardii, eine probiotische Hefe, die bereits zur Vorbeugung oder Behandlung von Durchfall eingesetzt wird. Ihre Idee war, diese Hefe so zu verändern, dass sie ein Fragment eines Rotavirus‑Oberflächenproteins namens VP8 sezerniert, das das Virus zur Anhaftung an menschliche Zellen verwendet. Sie verbanden VP8 mit einem kurzen Hilfsstück aus Protein, bekannt als P2, das zuvor gezeigt wurde, dass es Impfantworten steigert, und erzeugten so ein kombiniertes Protein namens P2‑VP8. Da nur ein kleiner, nicht infektiöser Teil des Virus verwendet wird, gehört dieser Ansatz zur größeren Familie der „Subunit“-Impfstoffe, die sicherer und leichter handhabbar sein sollen als Ganzvirus‑Impfstoffe.
Den Impfstoffkandidaten zuerst am Computer entwerfen
Bevor Tierversuche durchgeführt wurden, nutzte das Team eine Reihe von Computerwerkzeugen, um vorherzusagen, wie sich das P2‑VP8‑Protein verhalten würde. Sie kartierten Abschnitte von VP8, die wahrscheinlich von Immunzellen erkannt werden, und überprüften, ob diese Abschnitte über verschiedene menschliche genetische Hintergründe hinweg wirksam sein sollten. Anschließend bauten sie ein dreidimensionales Modell von P2‑VP8 und simulierten dessen Wechselwirkung mit TLR3, einem Sensor auf Immunzellen, der hilft, Virusinfektionen zu erkennen. Diese Simulationen legten nahe, dass P2‑VP8 stabil, löslich, nicht toxisch ist und in der Lage ist, eine starke, anhaltende Bindung an den Immunrezeptor einzugehen — alles ermutigende Hinweise für einen Impfstoffkandidaten.
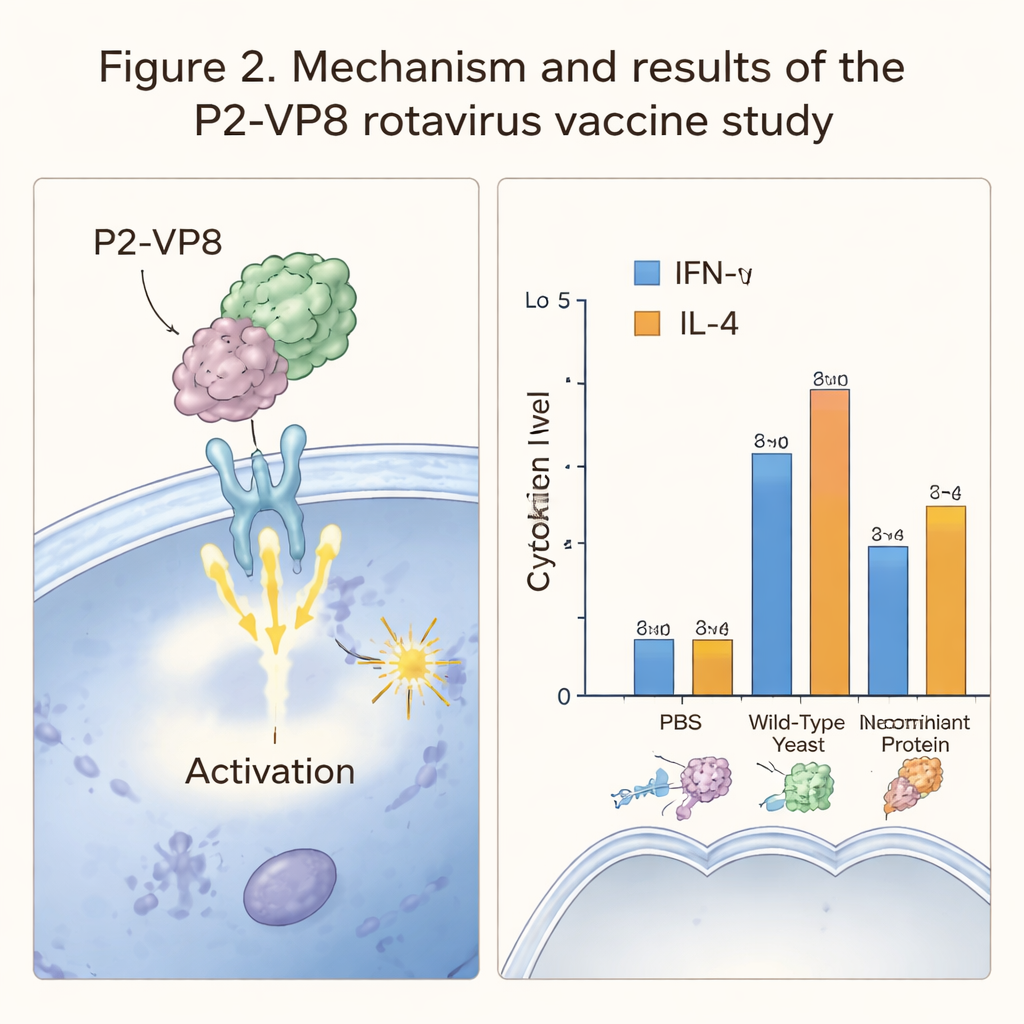
Die Hefe so verändern, dass sie das Rotavirus‑Protein sezerniert
Um die probiotische Hefe dieses Protein effizient produzieren zu lassen, schrieben die Forschenden das P2‑VP8‑Gen sorgfältig um und verwendeten dabei Codons — die dreibuchstabigen „Wörter“ der DNA — die Saccharomyces boulardii am leichtesten abliest. Diese Optimierung ist vergleichbar damit, ein Rezept in den Dialekt der Hefe zu übersetzen, damit ihre Maschinerie es schnell und genau ausführen kann. Anschließend setzten sie das optimierte Gen in einen Hefee Expressionsvektor ein und transformierten damit S. boulardii. In Laboransätzen bestätigten sie, dass die gentechnisch veränderte Hefe ein Protein der erwarteten Größe sezernierte, mittels Standard‑Proteintrennung (SDS‑PAGE) und Western‑Blot mit eigens hergestellten Antikörpern, wodurch gezeigt wurde, dass das Probiotikum tatsächlich als lebender Produzent des Impfstofffragments fungieren kann.
Prüfung der Immunantworten in Mäusen
Das Team untersuchte anschließend, wie sich dieser hefebasierte Impfstoff in lebenden Tieren verhält. Mäuse erhielten über mehrere Wochen orale Dosen verkapselter rekombinanter Hefe, während Vergleichsgruppen unbehandelte Hefe, eine Kochsalzlösung oder gereinigtes P2‑VP8‑Protein per Injektion erhielten. Nach der Impfung maßen die Forschenden wichtige Immunbotenstoffe, IFN‑γ und IL‑4, die verschiedene Arten der Immunaktivierung widerspiegeln. Mäuse, die die gentechnisch veränderte Hefe oder das injizierte Protein erhielten, zeigten höhere Spiegel dieser Zytokine als Kontrolltiere, was darauf hindeutet, dass ihr Immunsystem das Rotavirusfragment wahrgenommen und reagiert hatte. Allerdings beobachteten sie keine starke T‑Zell‑Proliferation oder robuste Antikörperspiegel in der Hefefütterungsgruppe, was darauf hindeutet, dass die Immunantwort bei oraler Verabreichung relativ schwach war.
Was diese Arbeit bedeutet und was noch verbessert werden muss
Insgesamt zeigt die Studie, dass eine probiotische Hefe in eine Fabrik verwandelt werden kann, die ein führendes Rotavirus‑Impfstofffragment sezerniert, und dass dieser Konstrukt in detaillierten Computertests wie erwartet reagiert. Bei Mäusen löste die gentechnisch veränderte Hefe einige Immunaktivitäten aus, erzeugte aber nicht die starken, schützenden Antworten, die für einen erfolgreichen Impfstoff erforderlich wären. Für eine interessierte Leserschaft ist die Quintessenz, dass das Konzept — eine freundliche Mikrobe als essbaren Impfstoff zu nutzen — technisch machbar erscheint, die derzeitige Ausführung jedoch noch nicht ausreichend wirksam ist. Zukünftige Arbeiten müssen das Proteindesign, die Dosierung und die Lieferstrategie verfeinern und direkte Tests des Schutzes gegen Rotavirus‑Infektionen einschließen, bevor ein solcher Ansatz für die Anwendung in der Praxis näher in Betracht gezogen werden kann.
Zitation: Farhani, I., Yamchi, A., Nikoo, H.R. et al. Design and immunogenicity of a recombinant Saccharomyces boulardii secreting the P2-VP8 subunit rotavirus vaccine. Sci Rep 16, 6932 (2026). https://doi.org/10.1038/s41598-026-37374-5
Schlüsselwörter: Rotavirus-Impfstoff, probiotische Hefe, Subunit-Impfstoffe, orale Immunisierung, Impfstoffdesign