Clear Sky Science · de
Effiziente Apoptose durch Doppelstrangbrüche der DNA in menschlichen Epithelzellen ausgelöst durch nicht-thermische Effekte hochfeldiger breitbandiger Terahertz‑Wellen
Neues Licht auf das Abtöten von Krebszellen
Krebsbehandlungen balancieren oft auf einem schmalen Grat: Sie müssen Tumorzellen vernichten, ohne gesundes Gewebe oder das Immunsystem stark zu schädigen. Diese Studie untersucht ein ungewöhnliches Werkzeug für diese Aufgabe — starke Terahertz(THz)-Wellen, eine Form unsichtbaren Lichts zwischen Mikrowellen und Infrarot. Die Forschenden zeigen, dass gezielt abgestimmte, hochfeldige THz‑Pulse Krebszellen kontrolliert zur „Selbsttötung“ veranlassen können, ohne das Gewebe zu erhitzen oder den unordentlichen Zelltod zu erzeugen, der zu Entzündungen führt.
Warum schonender Zelltod wichtig ist
Viele gängige Krebstherapien treiben Zellen in den Tod, verursachen dabei aber häufig Kollateralschäden. Medikamente und biologische Wirkstoffe können ihre Wirksamkeit verlieren, wenn Tumoren Resistenz entwickeln, und sie können das Immunsystem schwächen. Physikalische Methoden wie Röntgen, Radioaktivität oder hitzebasierte Ablation können das umliegende gesunde Gewebe verletzen und führen häufig zu Nekrose — einer gewaltsamen Form des Zelltods, die Entzündungen und Schmerzen auslöst. Ein Verfahren, das stattdessen Apoptose fördert, einen ordentlichen Selbstzerlegungsprozess, bei dem Zellen sich still und sauber abbauen, könnte eine deutlich weniger traumatische Möglichkeit bieten, Tumore zu verkleinern, insbesondere solche nahe der Hautoberfläche.
Terahertz‑Wellen treffen auf Brustkrebszellen
Das Team konzentrierte sich auf menschliche Brustkrebszellen (MCF‑7), einen häufig in Laborstudien verwendeten Epithelzelltyp. Sie setzten diese Zellen bis zu vier Stunden lang sehr starken, breitbandigen gepulsten THz‑Wellen aus und hielten dabei die Temperatur auf normalem Körperniveau. Die Feldstärken erreichten mehrere Millionen Volt pro Zentimeter, weit über denen alltäglicher Geräte. Unter diesen Bedingungen stieg der Anteil apoptotischer Zellen mit der Expositionsdauer stetig an. Bei der höchsten getesteten THz‑Intensität gingen nahezu 99 % der Krebszellen in Apoptose, während weniger als 1 % durch Nekrose starben. Diese massive, saubere Welle programmierter Zellsterblichkeit deutet darauf hin, dass die THz‑Pulse mehr bewirken als nur die Erwärmung der Zellen.
Nicht‑thermische Effekte und sichere Temperaturgrenzen
Da Wasser THz‑Strahlung stark absorbiert, bestand die naheliegende Sorge in unbeabsichtigter Erwärmung. Die Wissenschaftler nutzten Wärmebildaufnahmen, um Temperaturänderungen während der Bestrahlung zu verfolgen. Selbst nach vier Stunden bei moderater Intensität erwärmten sich die Krebszellen nur um etwa 3 °C, und die Nekrose blieb unter 4 %. Getrennte Kontrollversuche, in denen Zellen einfach vier Stunden lang erhitzt wurden, zeigten, dass Temperaturen unter 41 °C kaum zum Zelltod führten, während oberhalb von 43 °C ein starker Anstieg der Nekrose eintrat. Selbst bei den intensivsten THz‑Einstellungen hielten die Forschenden die Zelltemperaturen auf oder unter dieser 43‑°C‑Schwelle und beobachteten dennoch nahezu vollständige Apoptose bei minimaler Nekrose. Durch das Verringern der Wiederholrate der Pulse konnten sie zeigen, dass die Temperatur kontrollierbar bleibt, während die starken antitumoralen Effekte erhalten bleiben — ein Hinweis darauf, dass ein nicht‑thermischer Mechanismus wirkt.
Die DNA auseinanderreißen und Todesgene aktivieren
Um diesen Mechanismus zu finden, untersuchte die Gruppe die Zellen von innen. Im Elektronenmikroskop zeigten THz‑behandelte Zellen klassische frühe Zeichen der Apoptose: kondensiertes genetisches Material, veränderte Zellkerne und intakte Außenmembranen. Mit einem fluoreszenten Marker namens γ‑H2AX detektierten sie umfangreiche Doppelstrangbrüche in der DNA — Schäden, die in bestrahlten Zellen deutlich häufiger waren als in unbehandelten oder leicht erhitzten Kontrollen. Das Schadensmuster folgte dem Intensitätsprofil des THz‑Strahls und wurde zur Mitte hin stärker. Gen‑ und Proteinanalysen zeigten, dass eine Reihe stress‑ und schädigungsreaktiver Moleküle, wie GADD45B und c‑Jun, stark aktiviert waren, während bekannte Akteure klassischer Zelltodwege, darunter p53 und viele Caspasen, kaum Veränderungen zeigten. Die Autorinnen und Autoren schlagen vor, dass intensive THz‑Felder heftige vibrationale „Resonanzen“ in der DNA anregen könnten, die die Doppelhelix physikalisch beanspruchen und brechen und so einen eigenen, p53‑ und caspase‑unabhängigen Apoptoseweg auslösen.
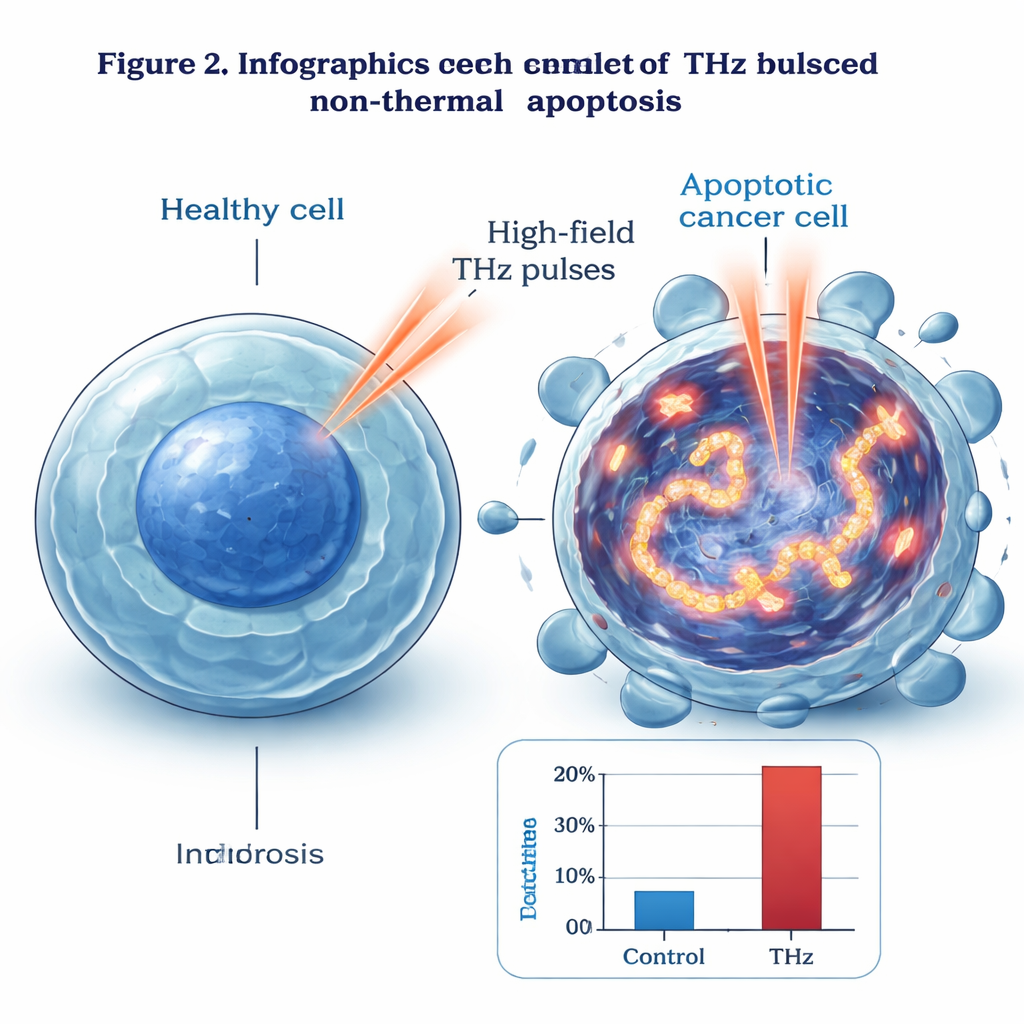
Vom Labor zur möglichen Therapie
Obwohl diese Experimente in Zellkulturen durchgeführt wurden, deuten sie auf einen neuen Ansatz physikalischer Krebstherapie hin. Hochfeldige THz‑Wellen scheinen mehrere Millimeter in feuchtes Gewebe eindringen zu können — genug, um oberflächliche Tumore zu erreichen — verlieren jedoch schnell an Stärke, wodurch tiefere Organe geschont werden könnten. Da der Effekt überwiegend nicht‑thermisch ist, könnte er prinzipiell Krebszellen Schicht für Schicht abtöten, ohne umliegendes Gewebe zu verbrennen oder starke Entzündungen hervorzurufen. Viel Arbeit bleibt: Der vorgeschlagene DNA‑„Resonanz“‑Mechanismus muss bestätigt werden, die Sicherheit für normale Zellen bedarf gründlicher Prüfung, und Tier‑ sowie klinische Studien sind erforderlich. Dennoch öffnet diese Forschung die Tür zu der Vorstellung, dass sorgfältig konstruierte Lichtpulse, abgestimmt auf die natürlichen Bewegungen von Biomolekülen, eines Tages eine präzise und vergleichsweise schonende Möglichkeit zur Ablation bestimmter Krebserkrankungen bieten könnten.
Zitation: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
Schlüsselwörter: Terahertz-Krebstherapie, nicht-thermische Apoptose, DNA-Doppelstrangbrüche, Brustkrebszellen, physikalische Tumorablation