Clear Sky Science · de
Generalisierte Blutgefäßmodelle für die onkologische Magnetnanopartikel-Anwendung: geometrische und mikrofluidische Eigenschaften
Winzige Magnete durch den Körper steuern
Stellen Sie sich vor, man könnte Krebsmedikamente mithilfe eines Magneten direkt in einen Tumor ziehen und so den Rest des Körpers vor starken Nebenwirkungen verschonen. Diese Studie untersucht, wie winzige magnetische Partikel durch gefäßähnliche Netzwerke wandern, und stellt eine auf den ersten Blick einfache Frage: Unter realistischen Strömungsbedingungen, können Magnete diese Partikel tatsächlich dorthin lenken, wo Ärzte sie haben wollen?
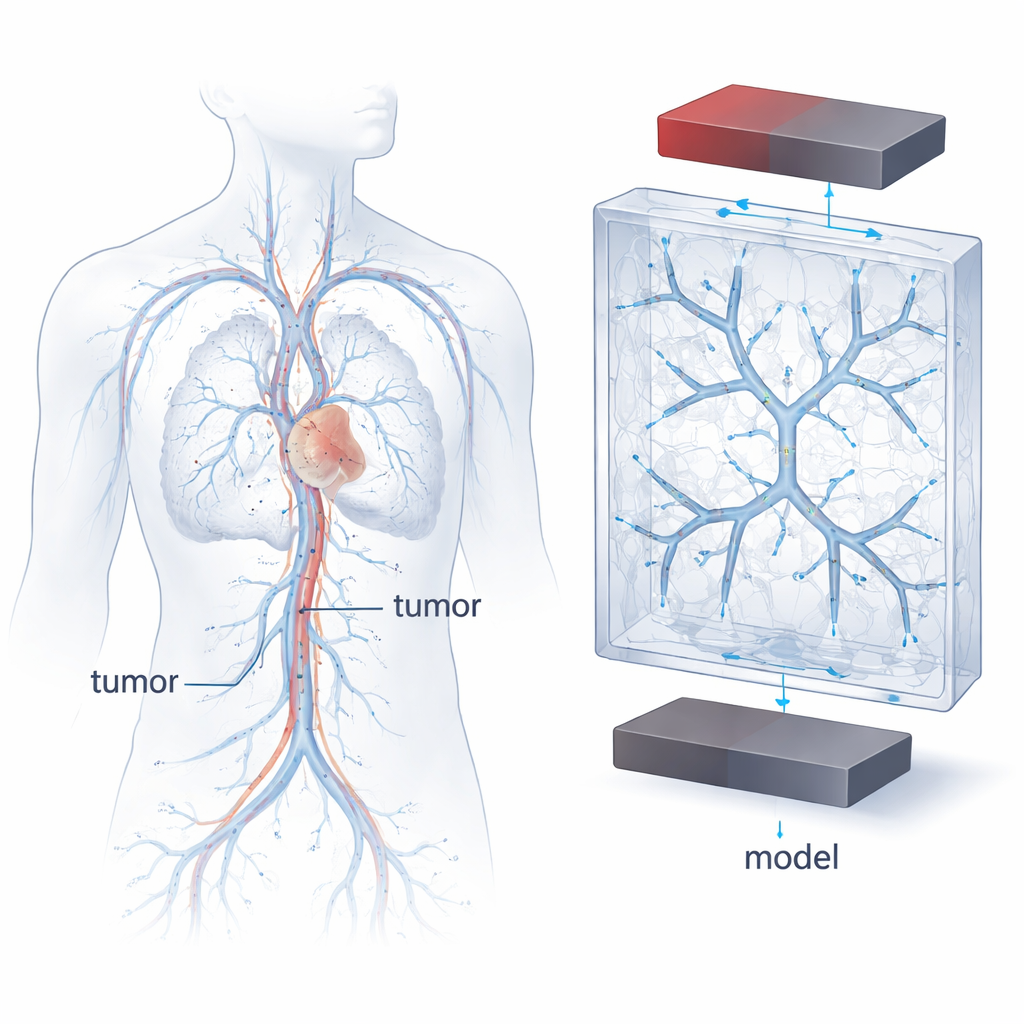
Warum Gefäßgeometrie und Strömung wichtig sind
Magnetische Krebstherapien beruhen auf superparamagnetischen Eisenoxid-Nanopartikeln (SPIONs), die von einem Magnetfeld angezogen werden können, während sie Medikamente durch den Blutkreislauf transportieren. Blutgefäße sind jedoch keine einfachen geraden Röhren: sie verzweigen, verengen, krümmen und teilen sich, und die Blutgeschwindigkeit nimmt zu oder ab. Diese Änderungen in Form und Strömung beeinflussen, wie sich Partikel bewegen, wo sie sich anreichern und ob sie lange genug die Gefäßwände berühren, um anzuhaften. Die Gefäßstrukturen realer Patienten sind äußerst variabel, was Vergleiche von Experimenten oder Vorhersagen zum Verhalten neuer Therapien erschwert. Die Autoren haben sich daher zum Ziel gesetzt, eine hochkontrollierte, reproduzierbare „Modellvaskulatur“ zu entwickeln, die dennoch die wesentlichen Merkmale tumorversorgender Gefäße einfängt.
Konstruktion idealisierter tumorversorgender Gefäßnetzwerke
Zur Gestaltung dieser Modellgefäße griff das Team auf klassische Regeln zurück, die beschreiben, wie echte Arterien verzweigen. Eine solcher Regeln, Murphys Gesetz (Murray’s law), verknüpft die Durchmesser von Mutter- und Tochtergefäßen in einem energieeffizienten Netzwerk. Mit klinischen Messungen aus Brusttumoren und diesen Skalierungsgesetzen generierten die Forscher mathematisch verzweigende Bäume, die nachahmen, wie tumorversorgende Gefäße sich bis zum Kapillarbett verkleinern. Anschließend nutzten sie hochauflösendes 3D-Drucken, um hohle Kanalnetzwerke mit zwei, drei oder vier Verzweigungsebenen in transparente Kunststoffblöcke einzubetten. Die Kanäle folgten einem symmetrischen Verzweigungsmuster und erstreckten sich dreidimensional, wodurch eine vereinfachte, aber physiologisch inspirierte Umgebung entstand, in der Partikelbewegungen untersucht werden konnten.
Beobachtung magnetischer Partikel in Aktion
Durch diese gedruckten Netzwerke pumpte das Team Wasser als Ersatz für Blut, injizierte stromaufwärts eine SPION‑haltige Flüssigkeit und legte ein statisches Magnetfeld um das Modell an. Hochgeschwindigkeitsaufnahmen lieferten einen filmähnlichen Verlauf, wie sich die dunklen Partikelwolken durch die verschiedenen Verzweigungen bewegten, während Computeranalysen Helligkeitsänderungen in zeitaufgelöste Signale umwandelten, die das lokale Partikelvorkommen reflektieren. Durch Variation von Hintergrundströmung, Partikelkonzentration, Verzweigungsdichte und Anwesenheit oder Abwesenheit eines Magneten konnten die Forscher herausarbeiten, wie jeder Faktor die Partikelverteilung, die Verweilzeit und die letztliche Ablagerung an den Kanalwänden beeinflusst.
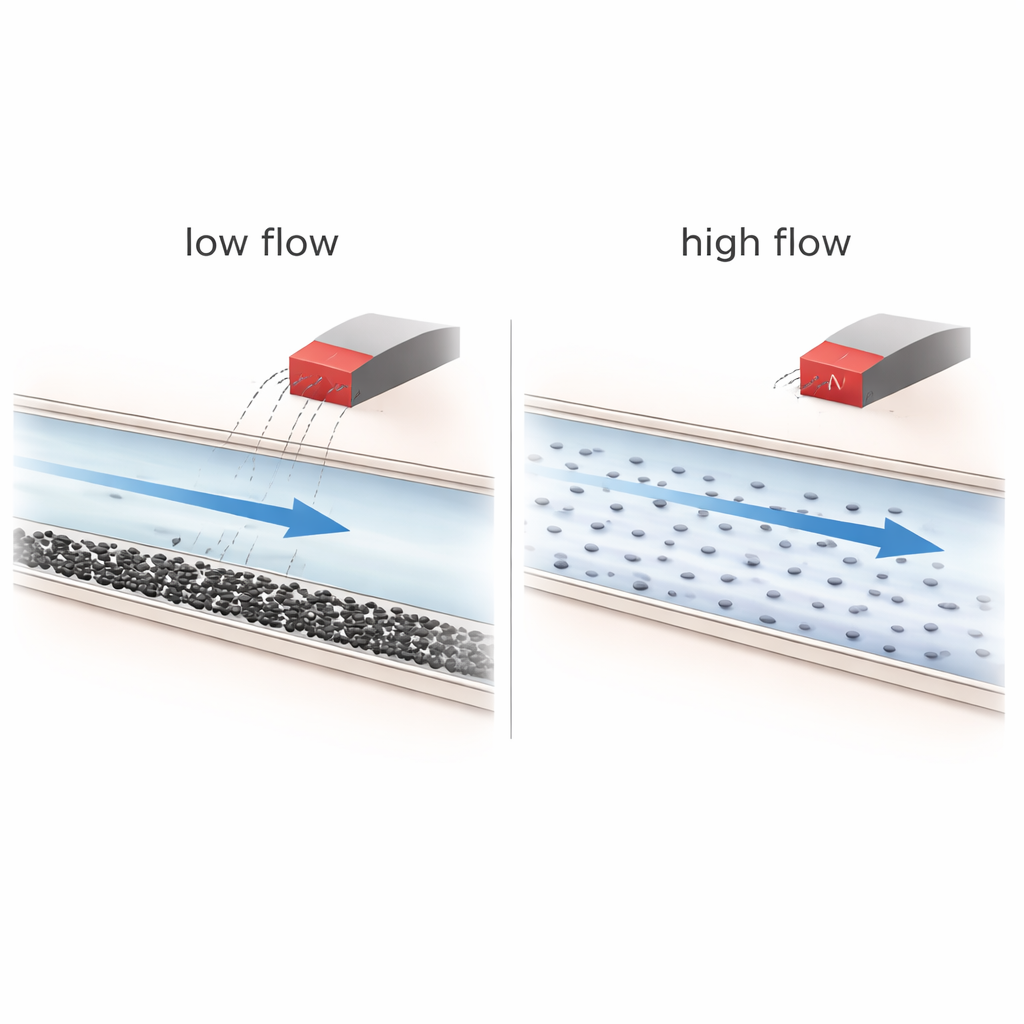
Wenn Magnete helfen — und wenn nicht
Die Experimente zeigen, dass die Strömungsbedingungen das Geschehen dominieren. Bei höheren Flussraten wird die Flüssigkeit gut durchmischt und die Nanopartikel bewegen sich schnell; unter diesen Bedingungen hat das Magnetfeld nahezu keinen Einfluss, und die Partikel folgen einfach den Stromlinien durch das Netzwerk. Bei niedrigen Flussraten hingegen führen Schwerkraft- und Konzentrationseffekte dazu, dass Partikel zur Unterseite der Kanäle absinken, schichtartige Verteilungen und gelegentlich lockere Cluster bilden. In dieser bereits ungleichmäßigen Situation kann der Magnet mehr Partikel in bestimmte Verzweigungen lenken und ihre Verweilzeit leicht verlängern, besonders in komplexeren, stark verzweigten Netzwerken. Rechnungen zeigen jedoch, dass die magnetische Kraft auf ein einzelnes 40-Nanometer-Partikel um viele Größenordnungen schwächer ist als die viskose Reibung durch die fließende Flüssigkeit, sodass ein echtes „Steuern einzelner Partikel“ unter den getesteten Bedingungen physikalisch unrealistisch ist.
Was das für zukünftige Krebstherapien bedeutet
Für Nicht‑Spezialisten lautet die wichtigste Erkenntnis, dass Magnete allein nicht zuverlässig frei suspendierte Nanopartikel aus einem schnell fließenden Blutstrom herausziehen können. Deutliche magnetische Effekte treten vielmehr nur dann auf, wenn Partikel bereits verlangsamt, abgesunken oder verklumpt sind — Situationen, die ihre magnetische Reaktion effektiv verstärken. Die hier vorgestellten generalisierten, 3D-gedruckten Gefäßmodelle bieten eine standardisierte Methode, um solche Effekte über verschiedene Netzwerkgeometrien und Strömungsregime hinweg zu erforschen. Für die zukünftige magnetische Wirkstofflenkung deutet diese Arbeit darauf hin, dass erfolgreiche Strategien wahrscheinlich kollektive Verhaltensweisen nutzen müssen — etwa kontrollierte Aggregation oder Trägersysteme — statt sich auf das Lenken einzelner Nanopartikel durch große, schnell perfundierte Gefäße zu verlassen.
Zitation: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
Schlüsselwörter: magnetische Wirkstofflenkung, Nanopartikel, Tumorvascularisation, Mikrofluidische Modelle, Arzneimittelabgabe