Clear Sky Science · de
Ein Tri‑Omics‑ und Machine‑Learning‑Rahmenwerk identifiziert prognostische Biomarker und metabolische Signaturen bei Sepsis
Warum das für Menschen mit schweren Infektionen wichtig ist
Sepsis ist eine lebensbedrohliche Reaktion auf eine Infektion, bei der das Immunsystem überreagieren und Organe versagen können. Ärztinnen und Ärzte wissen, dass das frühe Erkennen von Sepsis und die auf den einzelnen Patient zugeschnittene Behandlung Leben retten können, aber die heutigen Bluttests sind grobe Werkzeuge: Sie geben oft wenig Aufschluss darüber, wer sich erholen wird und wer das höchste Risiko trägt. In dieser Studie wird eine kraftvolle Kombination aus drei Arten molekularer Messungen und modernem Machine Learning eingesetzt, um genauere Warnsignale im Blut von Sepsispatienten zu finden.
Blutbetrachtung durch drei verschiedene Linsen
Anstatt sich auf eine Molekülart zu konzentrieren, haben die Forschenden dieselben Patienten gleichzeitig auf drei Arten charakterisiert. Sie maßen, welche Gene an- oder abgeschaltet sind (Transkriptomik), welche Proteine tatsächlich vorhanden und aktiv sind (Proteomik) und welche kleinen Stoffwechselmoleküle zirkulieren (Metabolomik). Sie entnahmen Blut von 21 Sepsispatienten und 10 gesunden Freiwilligen und nutzten fortgeschrittene Statistik, um zu untersuchen, wie diese drei Ebenen zusammen im Krankheitsfall verändert sind. Diese „Tri‑Omics“‑Sicht hilft, ein zentrales Problem zu überwinden: Bei Sepsis können Genaktivität und Proteinspiegel entkoppelt sein, sodass die Betrachtung nur einer Ebene irreführend sein kann.
Algorithmen beibringen, Hochrisikomuster zu erkennen
Aus Tausenden von Genen und Proteinen nutzte das Team zunächst eine Netzwerk‑Methode, um Gruppen zu finden, die sich bei Sepsis gemeinsam veränderten. Diese Gruppen wurden dann mit Proteinen abgeglichen, die sich klar zwischen Patienten und gesunden Kontrollen unterschieden, wodurch 32 starke Kandidaten übrigblieben. Um die Liste weiter zu verdichten, wandten sie Machine Learning an und nutzten zwei komplementäre Algorithmen, um schwächere Signale zu entfernen und nur die informativsten Merkmale zu behalten. Als sie prüften, wie diese verbleibenden Gene mit dem Überleben in einem großen öffentlichen Sepsisdaten‑Set zusammenhängen, hoben sich zwei hervor: TPR und ERN1. Patienten mit höheren TPR‑Werten tendierten zu längerer Überlebensdauer, während höhere ERN1‑Werte mit schlechteren Outcomes assoziiert waren.
Verknüpfung von Immunzellen und gestörtem Stoffwechsel
Die Studie blieb nicht bei Genen und Proteinen stehen. Durch das Scannen von Tausenden von Metaboliten im Blut der Patienten fanden die Forschenden 136 kleine Moleküle, die eng mit TPR und ERN1 korrelierten. Viele stammen aus Stoffwechselwegen, die Membranlipide und Fettsäuren verarbeiten – Wege, die entscheidend sind für die Signalübertragung von Immunzellen und die Ausbreitung von Entzündungen. Gleichzeitig zeigte eine Einzelzellanalyse — die einzelne Immunzellen statt eines gemischten Zellpools betrachtet — dass TPR und ERN1 besonders in Monozyten, Makrophagen und natürlichen Killerzellen aktiv sind. Zusammengenommen deuten diese Befunde darauf hin, dass die beiden Marker an der Schnittstelle zwischen den infektionabwehrenden Zellen des Körpers und der Art und Weise stehen, wie diese Zellen Fette und Energie bei Sepsis nutzen und umgestalten.
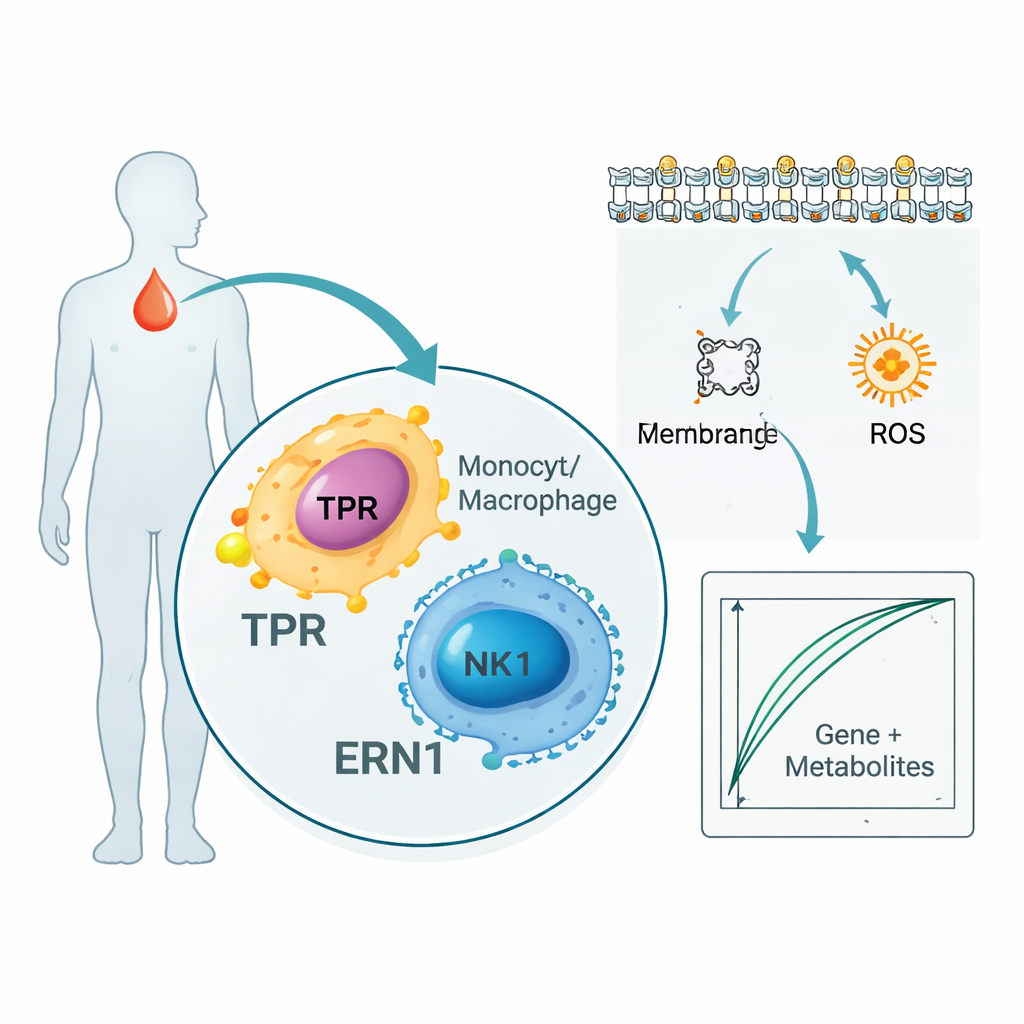
Aufbau eines Proof‑of‑Concept‑Bluttests
Um zu untersuchen, wie sich diese Entdeckungen in der Praxis nutzen lassen könnten, kombinierten die Autorinnen und Autoren die beiden Gene mit fünf der informativsten Metaboliten und trainierten einfache Computermodelle, die Sepsispatienten von gesunden Personen unterscheiden sollten. In ihrem kleinen internen Datensatz konnten diese kombinierten „Gen‑plus‑Metabolit“‑Signaturen fast perfekt zeigen, wer an Sepsis litt. Die Forschenden überprüften außerdem große öffentliche Datenbanken, die Blutproteine und Krankheitsrisiken in Zehntausenden von Personen verknüpfen, und fanden, dass TPR‑ und ERN1‑Proteinspiegel konsistent mit sepsisverwandten Erkrankungen assoziiert waren, was eine zusätzliche Unterstützungs‑Ebene liefert. Dennoch betonen die Autorinnen und Autoren, dass es sich bei diesen Modellen um Werkzeuge in einem frühen Stadium handelt, die Hypothesen erzeugen sollen, nicht um sofort einsatzbereite Kliniktests.
Pflanzenstoffe als frühe Hinweise, nicht als Heilmittel
In einem letzten Schritt fragten die Forschenden, ob natürliche Moleküle TPR oder ERN1 beeinflussen könnten. Sie durchsuchten eine spezialisierte Datenbank mit fast 500 gereinigten Verbindungen aus der traditionellen chinesischen Medizin, jede mit einem eigenen Genaktivitätsprofil. Mehrere Verbindungen schienen diese beiden Gene in kultivierten Zellen stark nach oben oder unten zu regulieren, was andeutet, dass sie eines Tages Forschenden helfen könnten, die Biologie der Sepsis zu erforschen oder neue Wirkstoffe zu entwerfen. Diese Ergebnisse basieren jedoch ausschließlich auf computergestützter Zuordnung: Sie zeigen nicht, dass irgendeine dieser Substanzen für Menschen mit Sepsis sicher oder wirksam ist.
Was diese Arbeit tatsächlich aussagt
Diese Studie liefert eher eine detaillierte Landkarte als eine fertige Lösung. Indem drei molekulare Ebenen, Einzelzelldaten und Machine Learning verknüpft werden, heben die Autorinnen und Autoren TPR und ERN1 — sowie die damit verbundenen metabolischen Veränderungen — als vielversprechende Wegweiser dafür hervor, wie Immunsystem und Stoffwechsel bei Sepsis aus dem Gleichgewicht geraten. Für Laien lautet die zentrale Botschaft, dass Sepsis keine einheitliche Krankheit ist, sondern ein wechselndes Muster immuner und metabolischer Zustände, und dass intelligentere Bluttests eines Tages Ärztinnen und Ärzten helfen könnten zu erkennen, in welchem Zustand sich ein Patient befindet und die Therapie entsprechend anzupassen. Bevor es so weit ist, müssen diese frühen Signale in deutlich größeren, vielfältigen Patientengruppen und in Laboruntersuchungen geprüft werden, die Ursache und Wirkung nachweisen können.
Zitation: Li, X., Ke, G., Hu, Y. et al. A tri-omics and machine learning framework identifies prognostic biomarkers and metabolic signatures in sepsis. Sci Rep 16, 6648 (2026). https://doi.org/10.1038/s41598-026-37342-z
Schlüsselwörter: Sepsis‑Biomarker, Multi‑Omics, Machine Learning in der Medizin, Immunstoffwechsel, präzise Diagnostik