Clear Sky Science · de
Die Zielrichtung der Akt–EphA2‑Achse und Zell‑zu‑Zell‑Adhäsion erhöht die Anoikis‑Empfindlichkeit in Krebszellen
Warum frei‑schwimmende Krebszellen wichtig sind
Wenn Krebszellen sich von einem Tumor lösen und durch den Blutkreislauf wandern, sollten sie normalerweise sterben, weil sie den Kontakt zum umgebenden Gewebe verlieren. Dieses eingebaute Sicherheitsprogramm, das man detachment‑induced cell death nennt, verhindert, dass Zellen an Orten wachsen, an denen sie nicht hingehören. Metastasierende Krebszellen lernen jedoch oft, dieses Signal zu ignorieren und im schwebenden Zustand zu überleben, was es ihnen erleichtert, neue Tumoren zu bilden. Die Studie stellt eine auf den ersten Blick einfache Frage: Wenn wir in aggressiven Brustkrebszellen einen entscheidenden mechanischen „Tastsinn“ wiederherstellen, können wir diese umherwandernden Zellen zum Absterben zwingen — und falls nicht, welche Ausweichtricks nutzen sie zum Überleben?
Wiedererweckung eines verlorenen Tastsinns
Zellen prüfen ständig, wie steif ihre Umgebung ist, indem sie an den Strukturen ziehen, die sie verankern. In gesundem Gewebe führt der Verlust von Kontakt oder das Andocken auf einer sehr weichen Oberfläche häufig zur Selbstzerstörung. Das Protein Tropomyosin 2.1 (Tpm2.1) ist ein wichtiger Bestandteil dieser internen Spannungsausrüstung und fehlt in Krebszellen oft oder ist reduziert. Die Forschenden verwendeten eine weit untersuchte metastatische Brustkrebszelllinie und brachten sie dazu, mehr Tpm2.1 zu produzieren, wodurch ein großer Teil dieses Rigiditätssinns wiederhergestellt wurde. Als diese modifizierten Zellen gezwungen wurden, auf speziellen nicht‑haftenden Gefäßen zu wachsen, die ein Anhaften verhindern, zeigten sie tatsächlich vermehrt Zelltod, wuchsen langsamer und bewegten sich weniger als unbehandelte Krebszellen. Dennoch waren selbst nach mehreren Tagen in Suspension noch etwa 70 % der Tpm2.1‑expressierenden Zellen lebensfähig, was darauf hindeutet, dass die Wiederherstellung des Tastsinns allein das Problem nicht vollständig löst.
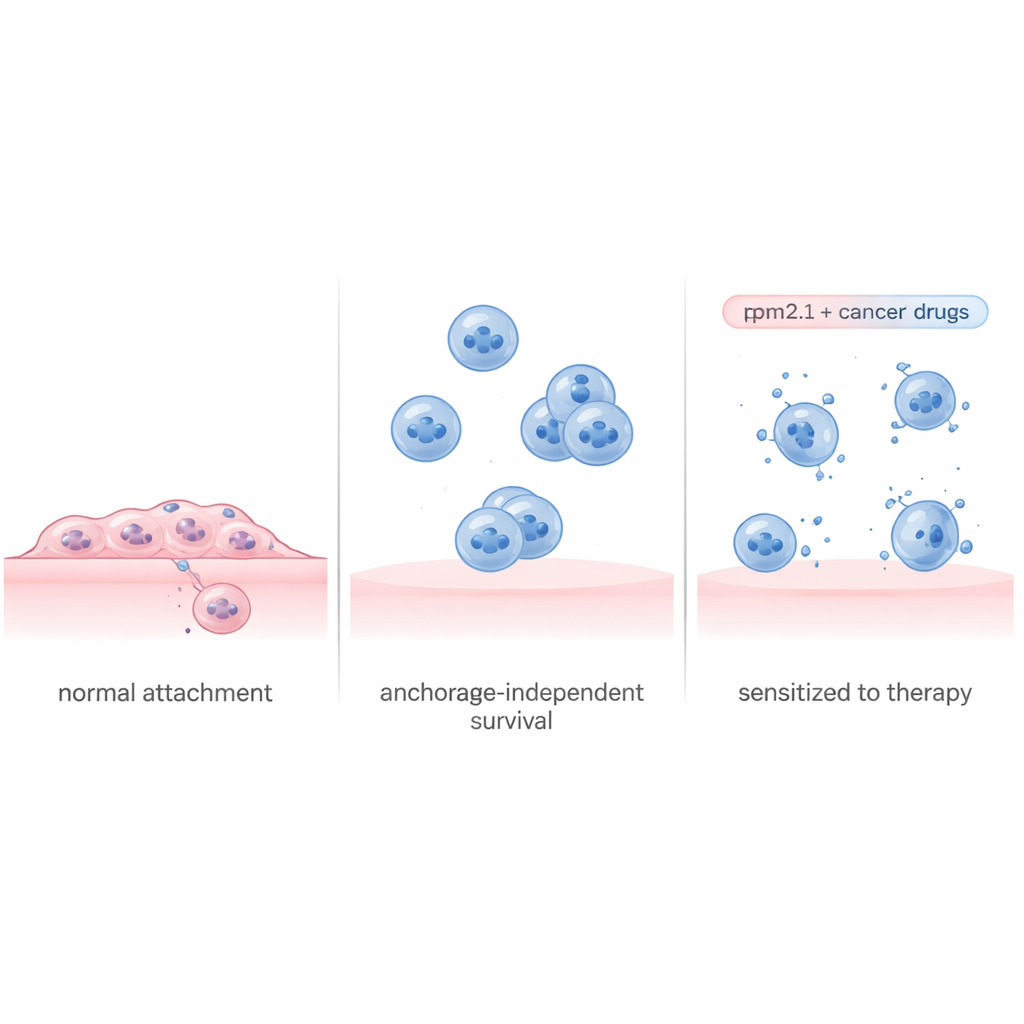
Das Überlebens‑Handbuch von Krebszellen lesen
Um zu verstehen, warum einige Zellen starben, während andere überlebten, teilte das Team die schwebenden Tpm2.1‑expressierenden Zellen in zwei Gruppen: solche mit frühen Anzeichen von Zelltod und solche, die gesund wirkten. Sie bestimmten anschließend, welche Gene in jeder Gruppe über vier Tage hinweg ein‑ oder ausgeschaltet waren. Die sterbenden Zellen zeigten eine weitreichende Abschaltung von Programmen, die an Zellteilung, DNA‑Reparatur und Anheftung beteiligt sind, zusammen mit Stresssignalen, die wie ein unaufhaltsamer Weg zur Selbstzerstörung wirkten. Im Gegensatz dazu aktivierten die überlebenden Zellen einen koordinierten Überlebensplan. Kurz nach der Ablösung schalteten sie Entzündungs‑ und Immunwege an und erhöhten später zentrale Wachstums‑ und Überlebensschaltungen, darunter einen bekannten Signalweg, der um das Protein Akt zentriert ist. Gleichzeitig steigerten sie stark Gene, die Zellen helfen, aneinander zu haften, sodass sie schützende Cluster bilden können, auch ohne am umgebenden Matrix zu verankern.
Stärke in der Anzahl: wie Zellcluster dem Tod widerstehen
Da die Genanalysen auf eine erhöhte Zell‑zu‑Zell‑Adhäsion hinwiesen, prüften die Forschenden, ob einfaches Zusammendrängen den Zellen im Schwebezustand helfen kann zu überleben. Wuchsen Tpm2.1‑expressierende Zellen bei hoher Dichte, wo Clusterbildung leicht möglich war, starben deutlich weniger Zellen als bei spärlicher Besiedlung. Ein Adhäsionsmolekül, ICAM1, hob sich in den überlebenden Zellen als besonders erhöht hervor und ist bereits dafür bekannt, die Bildung von Clustern zirkulierender Tumorzellen zu unterstützen und deren Einnistung in entfernten Geweben zu erleichtern. Das Blockieren von ICAM1 mit einem kleinen Molekül‑Inhibitor erhöhte den Zelltod in Suspension bei den Tpm2.1‑expressierenden Zellen, während es in normalen angehefteten Kulturen kaum Wirkung zeigte. Diese Befunde stützen die Idee, dass Krebszellen, sobald ihre internen Mechaniken teilweise wiederhergestellt sind, dem Tod entgehen können, indem sie sich buchstäblich aneinander festhalten statt an ihrer Umgebung.
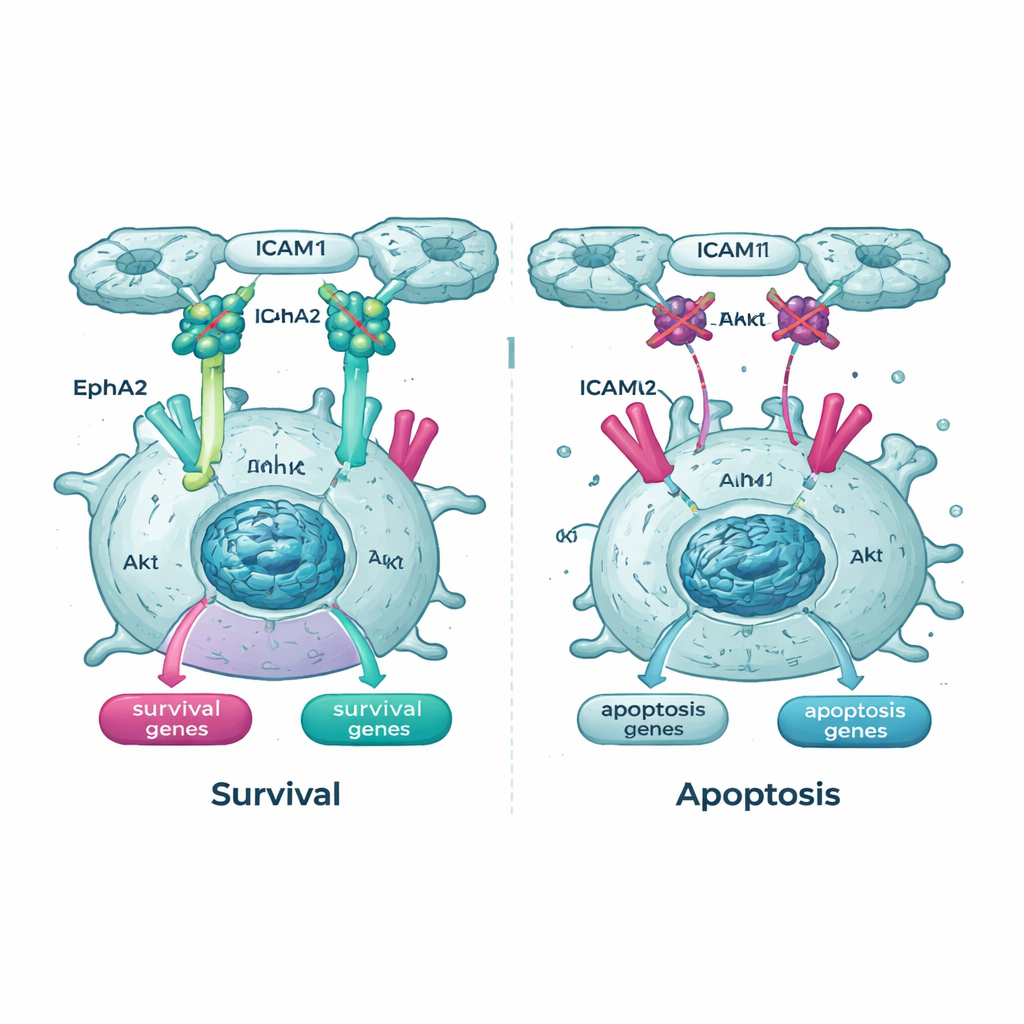
Wesentliche Lebensadern innerhalb der Zelle kappen
Die genetischen Untersuchungen hoben außerdem den Akt‑Signalweg und einen seiner Partner, einen Rezeptor namens EphA2, als wichtige Lebensadern für schwebende Krebszellen hervor. In Tpm2.1‑expressierenden Zellen war die aktive, phosphorylierte Form von Akt in Suspension niedriger als in Kontrollzellen, und auch die Menge und Aktivität von EphA2 war reduziert. Behandelten die Forschenden die Zellen mit Wirkstoffen, die Akt oder EphA2 blockieren, wurden sowohl normale als auch Tpm2.1‑expressierende Krebszellen deutlich wahrscheinlicher in Suspension abgetötet. Bemerkenswert war, dass die Zellen mit wiederhergestelltem Rigiditätssinn über die Zeit besonders empfindlich auf diese Medikamente reagierten, was nahelegt, dass sie, sobald ihre mechanischen Sicherheitschecks teilweise wieder angeknüpft sind, stärker von den verbleibenden Überlebenssignalen abhängen.
Aus einem vorbereiteten Zustand eine tödliche Verwundbarkeit machen
Für Nicht‑Spezialisten lautet die Kernaussage, dass das Reparieren eines defekten Sicherheitsmechanismus in Krebszellen — ihre Fähigkeit, das Verlieren des Kontakts zu spüren und darauf zu reagieren — notwendig, aber nicht ausreichend ist, um sie zur Selbstzerstörung zu bringen. Die Zellen, die überleben, tun dies, indem sie sich zusammenschließen und ihre interne Verschaltung über alternative Wachstums‑ und Überlebenswege umlenken. Diese Arbeit zeigt, dass die Wiederherstellung des Rigiditätssinns mit Tpm2.1 metastatische Brustkrebszellen in einen „vorbereiteten“ Zustand versetzt, in dem sie dem Tod näher sind, aber noch nicht unumkehrbar verloren. Indem dann die Akt–EphA2‑Achse blockiert und die Zell‑zu‑Zell‑Adhäsion über ICAM1 gestört wird, können Forschende diese vorbereiteten Zellen über die Kante stoßen und detachment‑induzierten Zelltod deutlich erhöhen. Praktisch skizziert die Studie eine Strategie für zukünftige Kombinations‑Therapien, die darauf abzielen, frei‑schwimmende Tumorzellen zu eliminieren, bevor sie neue Metastasen aussäen können.
Zitation: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
Schlüsselwörter: Mammakarzinom‑Metastasen, Zelladhäsion, Anoikis, Akt‑Signalgebung, Rigiditätssinn