Clear Sky Science · de
Purpur LED‑Licht und Rohglycerin verstärken synergistisch die Astaxanthin‑Produktion in Aurantiochytrium limacinum
Warum leuchtende Mikroben für Sie wichtig sein könnten
Farbige Verbindungen aus der mikroskopischen Welt verändern still und leise, wie wir Nahrungsergänzungsmittel, Kosmetika und sogar Fischfutter herstellen. Diese Studie untersucht, wie ein winziger Meeresorganismus, Aurantiochytrium limacinum, mit Hilfe von purpurnem LED‑Licht und preiswerten industriellen Nebenprodukten dazu gebracht werden kann, wertvolle Moleküle wie Astaxanthin — ein starkes rotes Antioxidans, das auch in Lachs und Garnelen vorkommt — sowie gesunde Omega‑3‑Fette wie DHA zu produzieren. Die Arbeit weist auf nachhaltigere und kostengünstigere Wege zur Herstellung dieser Inhaltsstoffe hin, ohne auf wilden Fischfang oder energieintensive Chemiefabriken angewiesen zu sein.
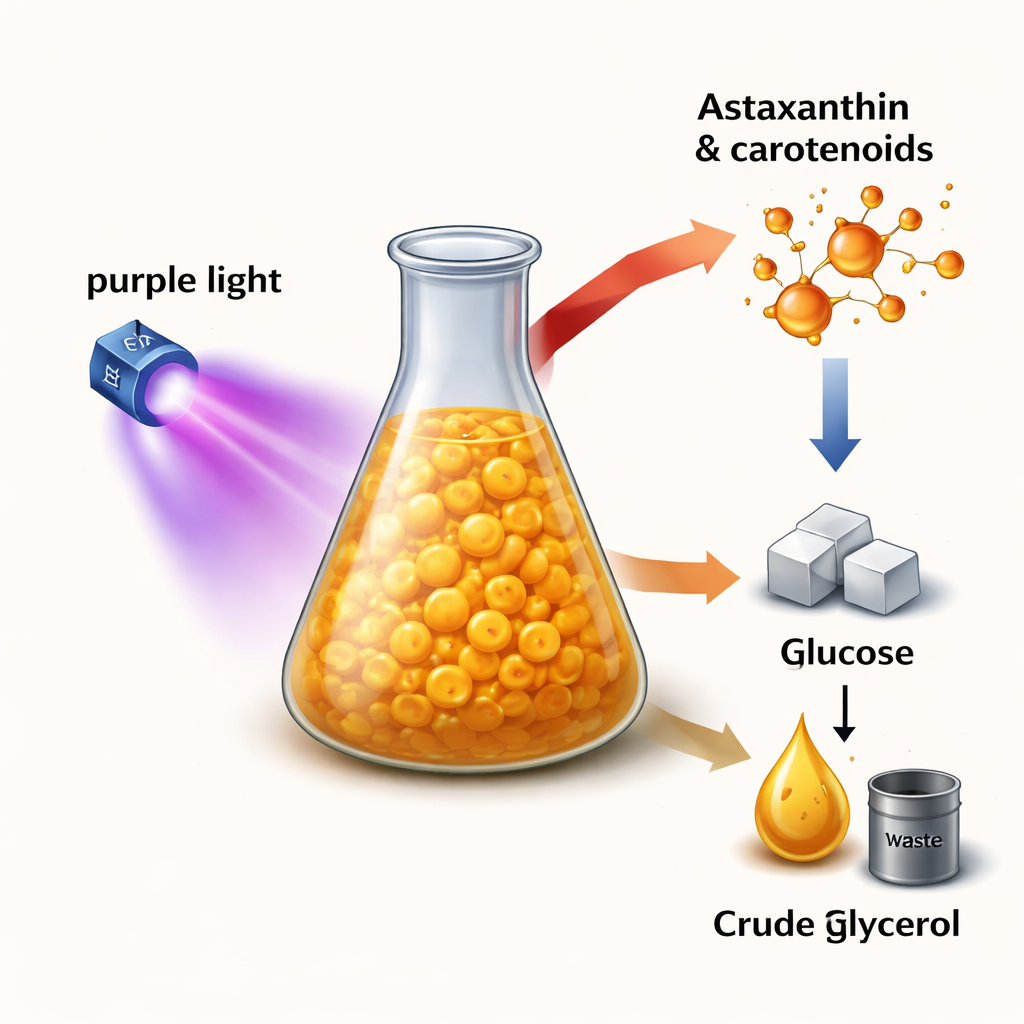
Eine winzige Fabrik aus dem Meer
Aurantiochytrium limacinum ist ein mikroskopischer mariner Protist, der im Dunkeln gedeiht und organischen Kohlenstoff statt Sonnenlicht als Energiequelle nutzt. Für die Industrie ist er attraktiv, weil er gleichzeitig zwei wertvolle Produkte herstellen kann: DHA, ein Omega‑3‑Fett, das für Gehirn und Herz wichtig ist, und Carotinoide, die Pigmente, die vielen Pflanzen und Tieren ihre gelben, orangefarbenen und roten Farbtöne verleihen. Unter diesen Carotinoiden sticht Astaxanthin durch seine starke antioxidative und entzündungshemmende Wirkung hervor, was die Nachfrage in Nahrungsergänzungsmitteln, funktionellen Lebensmitteln und Hautpflege erhöht hat. Bisher stammt der Großteil des Astaxanthins entweder aus Fischöl oder aus energieintensiver chemischer Synthese, beides Varianten, die Fragen zur Nachhaltigkeit und Sicherheit aufwerfen.
Das richtige Licht einschalten
Die Forschenden untersuchten, wie verschiedene Lichtfarben — Dunkelheit, normales Weißlicht und schmalbandige purpurfarbene LEDs (410–420 nm) — das Stoffwechselbild dieses Mikroorganismus beeinflussen. Sie züchteten Kulturen mit entweder Glukose (einem einfachen Zucker) oder Glycerin als Hauptnährstoff und maßen anschließend Zellwachstum, Fettspeicherung und Carotinoidgehalte. Die Zellen wuchsen unter allen Lichtfarben ähnlich gut, und ihr Gesamtfettgehalt blieb weitgehend unverändert. Dramatisch verändert hat sich jedoch die Pigmentzusammensetzung: Unter purpurnem Licht wurden die höchsten Carotinoidwerte erreicht, gefolgt von Weißlicht; im Dunkeln fiel die Produktion am geringsten aus. Sowohl β‑Carotin als auch Canthaxanthin, orangefarbene Pigmente, die stromaufwärts im Astaxanthin‑Biosyntheseweg liegen, stiegen unter purpurnem Licht stark an, besonders wenn Glycerin als Kohlenstoffquelle verwendet wurde. Astaxanthin selbst war jedoch am häufigsten in Kulturen mit Glukose als Nährstoff, was zeigt, dass Lichtfarbe und Futtertyp subtil steuern, wie weit der Pigmentweg in den Zellen durchlaufen wird.
Abfall in Farbe und Öl verwandeln
Eine große Herausforderung bei der Markteinführung dieses Mikroorganismus ist die Fütterungskosten. Glukose ist auf industrieller Ebene relativ teuer, während die Biodieselproduktion große Mengen an Rohglycerin erzeugt, einem geringwertigen Nebenprodukt, das schwer zu entsorgen sein kann. Die Autorinnen und Autoren prüften, ob dieses unreinere Glycerin lediglich so weit gereinigt werden muss, dass es als brauchbares Substrat dient. Nach einfachen Behandlungen — Verdünnung, Ansäuerung zur Entfernung von Seifen und Salzen und in einigen Fällen eine zusätzliche Aktivkohle‑Politur — unterstützte das Rohglycerin das Mikrobiellwachstum in vergleichbarem Maß wie reines Glukose‑ bzw. Glycerinmedium. Unter purpurnem LED‑Licht produzierten aufbereitetes Rohglycerin beziehende Kulturen hohe Mengen an β‑Carotin und Canthaxanthin und erreichten schließlich Astaxanthinmengen, die denen in Standardmedien ähnelten, während die Neutralfettsynthese (Ölproduktion) erhalten blieb.
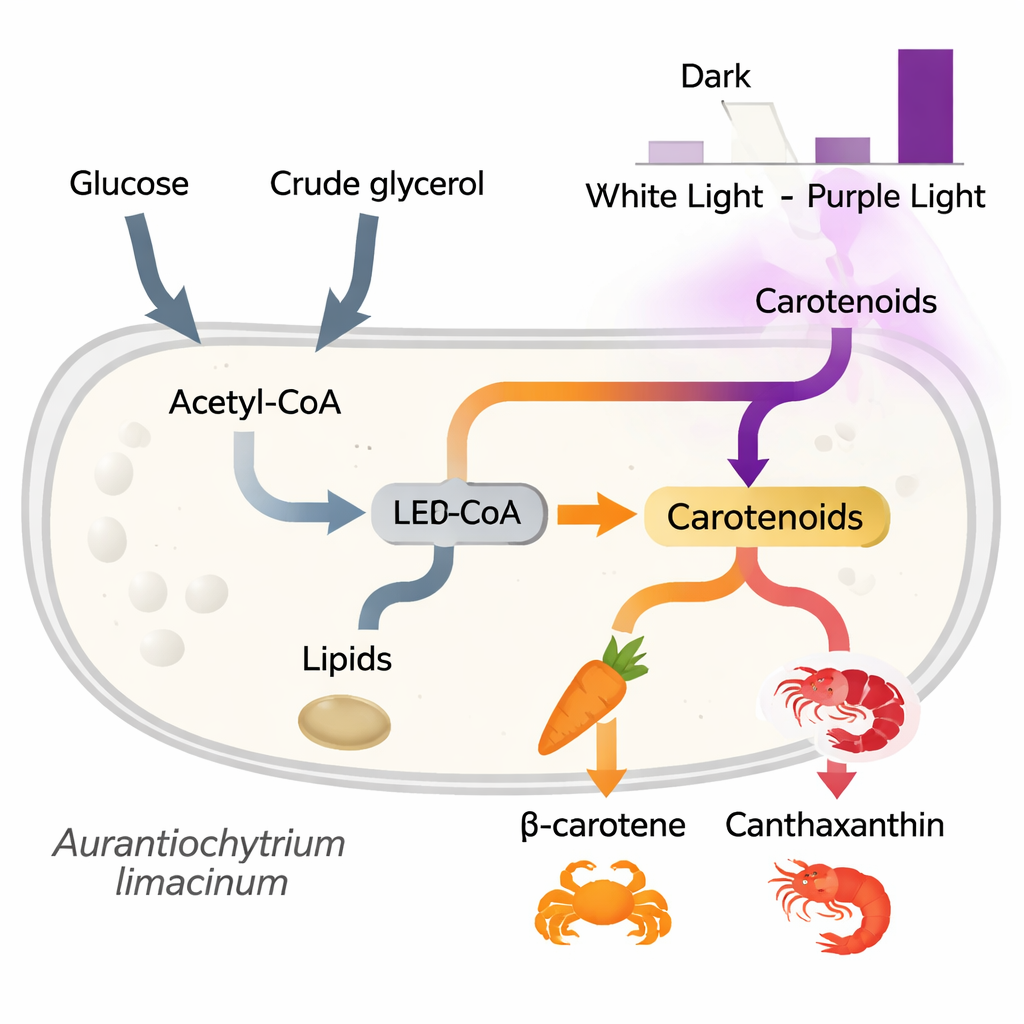
Ein Blick unter die Haube der Zelle
Um zu verstehen, wie Licht und Nährstofftyp den Stoffwechsel umgestalten, untersuchte das Team zudem mittels RNA‑Sequenzierung, welche Gene unter den verschiedenen Bedingungen an‑ oder abgeschaltet wurden. Sie fanden, dass Gene, die an der Aufnahme und Verarbeitung von Glycerin beteiligt sind, stark aktiviert wurden, wenn Glycerin als Nährstoff diente, was bestätigt, dass die Zellen dieses abfallbasierte Kohlenstoffsubstrat effizient in den zentralen Stoffwechsel leiten können. Überraschenderweise waren viele Gene, die mit Fett‑ und Carotinoidsynthese verknüpft sind, zu einem frühen Zeitpunkt unter purpurnem Licht weniger aktiv, obwohl die Pigmentlevel später höher waren. Dieses Muster spricht dafür, dass die Zellen unter Lichtstress zunächst einige Prozesse dämpfen und dann später als Schutzreaktion die Pigmentproduktion hochfahren, wobei Carotinoide als natürliche „Sonnenschutzmittel“ und Antioxidantien dienen.
Was das für künftige Produkte bedeutet
Für Nicht‑Spezialisten ist die wichtigste Erkenntnis, dass durch sorgfältige Abstimmung von Beleuchtung und Nährstoffangebot ein Meeresmikroorganismus zu einer flexiblen, kostengünstigen Produktionsplattform für gesundheitsbezogene Inhaltsstoffe werden kann. Purpurfarbene LED‑Beleuchtung erhöht die Produktion farbiger, schützender Pigmente, ohne die Herstellung nützlicher Öle zu beeinträchtigen, während leicht gereinigtes Rohglycerin — im Grunde ein industrieller Abfallstrom — teurere Zucker als Hauptnährstoff ersetzen kann. Zusammen weisen diese Strategien auf eine umweltfreundlichere und wirtschaftlichere Produktion von Astaxanthin und DHA hin, die den Druck auf Wildfischbestände und fossilstoffbasierte Chemie verringert und die stille Kraft der mikrobiellen Biotechnologie nutzt.
Zitation: Yamakawa, K., Kawano, K., Kato, S. et al. Purple LED light and crude glycerol synergistically enhance astaxanthin production in Aurantiochytrium limacinum. Sci Rep 16, 6623 (2026). https://doi.org/10.1038/s41598-026-37313-4
Schlüsselwörter: Astaxanthin, Aurantiochytrium, purpur LED‑Licht, Rohglycerin, mikrobielle Bioprodukte