Clear Sky Science · de
Auswirkung der definierten Oligo‑MM12‑Mikrobiota auf die intestinale Kolonisation und Dissemination von Listeria monocytogenes
Warum die Keime in Ihrem Darm wichtig sind
Viele Menschen kennen Listeria monocytogenes als gefährlichen, lebensmittelbedingten Erreger, der mit kontaminierten Fertigprodukten und schweren Erkrankungen bei anfälligen Personen in Verbindung gebracht wird. Weniger offensichtlich ist jedoch, dass das Eindringen dieses Bakteriums nicht nur von unserem Immunsystem abhängt, sondern auch von der lebhaften Gemeinschaft von Mikroben, die bereits in unserem Darm lebt. Diese Studie verwendet speziell gestaltete Mausmodelle und einen Miniatur‑„künstlichen Kolon“, um eine einfache, aber wichtige Frage zu stellen: Wie beeinflusst die Komplexität des Darmmikrobioms die Fähigkeit von Listeria, den Darm zu besiedeln und sich im Körper auszubreiten?
Die Geschichte zweier mikrobieller Nachbarschaften
Um diese Frage zu untersuchen, verglichen die Forschenden zwei Mäusegruppen. Eine Gruppe, bezeichnet als SPF‑Mäuse, trug eine reichhaltige, natürliche Mischung von Darmbakterien, wie sie in vielen Labortieren zu finden ist. Die andere Gruppe, Oligo‑MM12‑Mäuse, beherbergte eine deutlich einfachere Gemeinschaft, bestehend aus nur 12 gut charakterisierten Bakterienstämmen. Da jedes Mitglied dieser Gemeinschaft bekannt ist und generationsübergreifend stabil bleibt, sind Oligo‑MM12‑Mäuse ein leistungsfähiges Werkzeug, um zu analysieren, welche Mikroben Eindringlinge blockieren und welche Lücken in unseren Abwehrmechanismen hinterlassen könnten. Durch den Vergleich dieser Mäuse konnte das Team testen, wie sich ein dichtes, diverses Darmökosystem von einem schlanken, minimalistischen darin unterscheidet, wie es mit einer Infektionsherausforderung umgeht.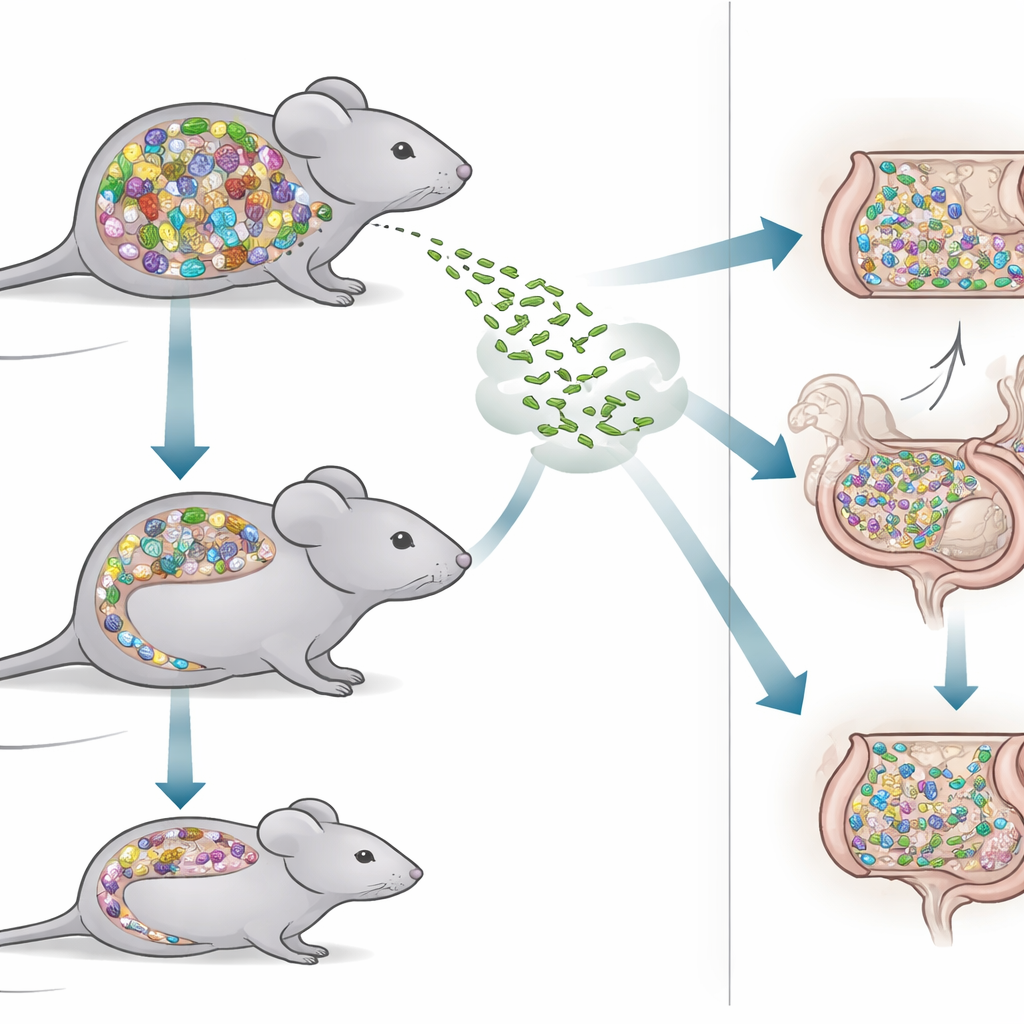
Listeria durch Darm und darüber hinaus verfolgen
Die Wissenschaftler infizierten beide Maustypen mit derselben oralen Dosis von Listeria und verfolgten, wie viele Bakterien sich über drei Tage im Kot und in inneren Organen nachweisen ließen. Interessanterweise schien die einfachere Oligo‑MM12‑Gemeinschaft anfänglich besser darin zu sein, Listeria in Schach zu halten: Am ersten Tag nach der Infektion scheiden diese Mäuse weniger Listeria‑Zellen mit dem Stuhl aus als SPF‑Mäuse. Dieser frühe Vorteil verflog jedoch. Am dritten Tag scheiden Oligo‑MM12‑Mäuse mehr Listeria aus, während SPF‑Mäuse die Werte kontinuierlich senken konnten. Trotz dieser deutlichen Unterschiede im Darm waren die Listeria‑Zahlen in inneren Organen wie Leber, Milz und Lymphknoten zwischen den beiden Mausmodellen ähnlich, was darauf hindeutet, dass die Komplexität des Mikrobioms eine geringere Rolle spielt, sobald Listeria tiefere Gewebe erreicht.
Den Kolon in einer kontrollierten Box simulieren
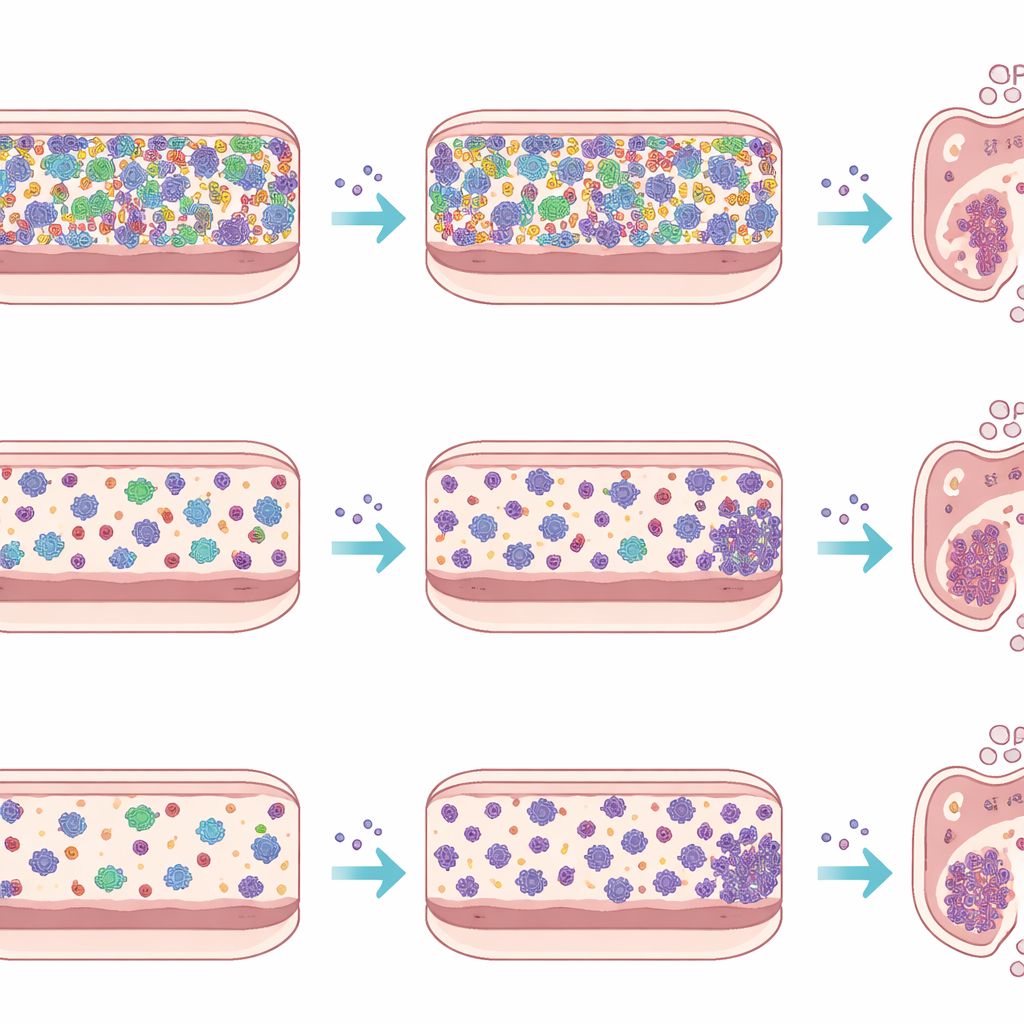
Um die Effekte von Wirtsgeweben und Immunität von dem Verhalten der Mikroben selbst zu trennen, führte das Team auch ein ex vivo Experiment mit einem Gerät namens micro‑Matrix‑Bioreaktor durch. Sie stellten Fäkalsuspensionen aus jedem Maustyp her, fügten diese in ein nährstoffreiches Medium in versiegelten, sauerstofffreien Vertiefungen ein und setzten Listeria in einige dieser Miniaturkulturen ein, während andere als Kontrollen blieben. Über fünf Tage maßen sie Listeria‑Zahlen und sequenzierten bakterielle DNA, um die Entwicklung der Gemeinschaften zu verfolgen. In diesem künstlichen Kolon wuchs Listeria auf ähnliche Niveaus, unabhängig davon, ob es auf die komplexe SPF‑Mikrobiota oder die einfachere Oligo‑MM12‑Gemeinschaft traf, und seine Anwesenheit verursachte nur mäßige Verschiebungen in der Gesamtzusammensetzung. Dieser Gegensatz zu den lebenden Tieren unterstreicht, wie stark das Immunsystem, die Darmwand sowie Galle- und Schleimströme die Infektion im realen Darm formen.
Wichtige mikrobielle Gewinner, Verlierer und Zuschauer
Durch die Betrachtung der bakteriellen Gruppen, die während der Infektion zunahmen oder abnahmen, identifiziert die Studie Kandidaten, die den Erfolg von Listeria beeinflussen könnten. In Oligo‑MM12‑Mäusen sanken die Werte von Akkermansia, einem schleimassoziierten Bakterium, das oft mit Darmgesundheit in Verbindung gebracht wird, am zweiten Tag und erholten sich dann bis zum dritten Tag stark. Bei SPF‑Mäusen gingen mehrere Gattungen zurück, die dafür bekannt sind, nützliche Metaboliten zu produzieren oder die Barriereintegrität zu unterstützen, etwa Blautia und Bacteroides, während bestimmte Prevotella‑ähnliche Bakterien komplexe Anstiege und Abnahmen zeigten, die auf eine direkte Beeinflussung durch Listerias eigene antimikrobielle Verbindungen hindeuten könnten. Ex vivo waren diese Muster weitgehend abgeschwächt, was die Idee bestärkt, dass viele der beobachteten Verschiebungen aus Drei‑Wege‑Interaktionen zwischen Erreger, ansässigen Mikroben und der Wirtsumgebung entstehen, statt aus einfacher Mikrobe‑gegen‑Mikrobe‑Konkurrenz allein.
Was das für den Schutz von Menschen bedeutet
Für Nichtfachleute ist die zentrale Botschaft, dass nicht alle gesund wirkenden Mikrobiome auf dieselbe Weise vor Infektionen schützen und dass „mehr Vielfalt“ nicht immer in jedem Moment besser ist. Die vereinfachte Oligo‑MM12‑Gemeinschaft bot im Darm eine starke frühe Resistenz gegen Listeria, doch im Verlauf zeigte das komplexere SPF‑Mikrobiom eine bessere Fähigkeit, den Eindringling zu eliminieren. Die Arbeit zeigt, dass sorgfältig konstruierte, niedrigkomplexe Mikrobiotamodelle in Kombination mit kontrollierbaren ex vivo‑Systemen aufdecken können, welche Bakteriengruppen und Umweltfaktoren entscheidend sind, um gefährliche lebensmittelbedingte Erreger zu blockieren. Letztlich könnten solche Erkenntnisse gezielte Probiotika oder mikrobielle Therapien leiten, die zur richtigen Zeit die richtigen mikrobiellen Verbündeten stärken, um schwere Listeria‑Infektionen bei gefährdeten Patientengruppen zu verhindern.
Zitation: Cazzaniga, M., Bra, K.K., Herzog, M.K.M. et al. Impact of the defined Oligo-MM12 microbiota on intestinal colonisation and dissemination of Listeria monocytogenes. Sci Rep 16, 8434 (2026). https://doi.org/10.1038/s41598-026-37294-4
Schlüsselwörter: Listeria‑Infektion, Darmmikrobiom, Kolonisierungsresistenz, Mausmodell, Probiotika