Clear Sky Science · de
Ein Deep‑Learning‑Ensemble‑Framework zur Klassifikation mehrerer Subtypen von Nierentumoren anhand kontrastverstärkter CT
Warum es wichtig ist, Nierentumoren früh zu erkennen
Nierenkrebs kann jahrelang still verlaufen und wenige Symptome zeigen, bis er sich bereits ausgebreitet hat. Mit modernen Bildgebungsverfahren werden jedoch viele Nierenläsionen zufällig entdeckt, etwa bei Untersuchungen wegen Rückenschmerzen oder anderer Beschwerden. Die zentrale Frage lautet dann: Handelt es sich um einen gefährlichen Krebs, der operiert werden muss, oder um eine harmlose Läsion, die beobachtet werden kann? Diese Studie untersucht, wie künstliche Intelligenz Ärzten helfen kann, CT‑Scans genauer zu lesen, unnötige Operationen zu verringern und gleichzeitig aggressive Tumoren rechtzeitig zu erkennen.
Fünf Arten von Nierentumoren, eine schwierige Entscheidung
Nicht alle Nierentumoren sind gleich. Einige, wie Angiomyolipom (AML) und renales Onkozytom (RO), sind gutartig und bedrohen möglicherweise nie das Leben einer Person. Andere, unter dem Begriff Nierenzellkarzinom (RCC) zusammengefasst, sind bösartig und können in andere Organe streuen. Unter den bösartigen Nierenkrebsen ist das klarzellige RCC (ccRCC) am häufigsten und am stärksten metastasierungsgefährdet; papilläres RCC (pRCC) und chromophobes RCC (chRCC) sind im Allgemeinen weniger aggressiv, aber ebenfalls ernst zu nehmen. Auf den üblichen Scans können sich diese Subtypen jedoch überraschend ähnlich darstellen, sodass Ärzte oft auf Biopsie oder Operation zur sicheren Diagnosestellung angewiesen sind. Die Autoren prüften, ob ein fortgeschrittenes Computersystem diese fünf Tumortypen allein anhand kontrastverstärkter CT‑Bilder zuverlässig unterscheiden kann.
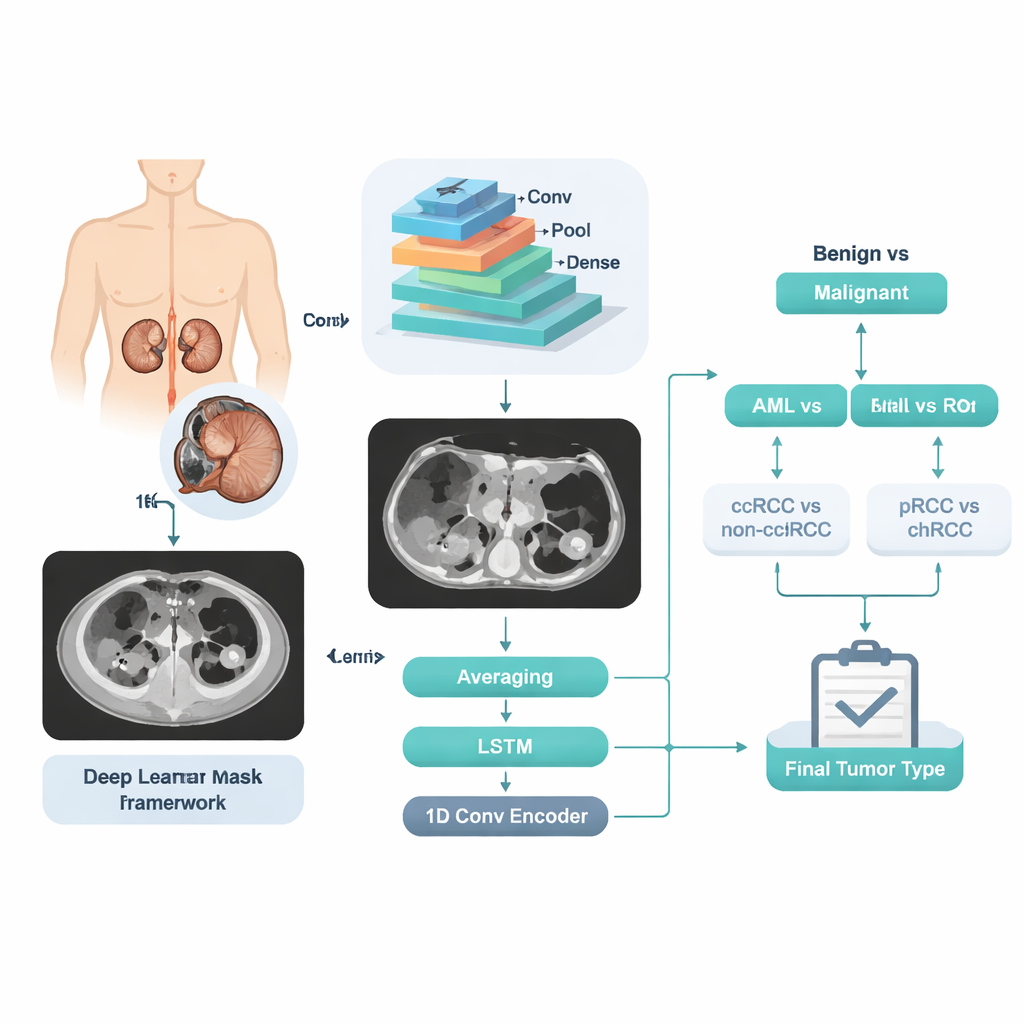
CT‑Scans in lernbare Muster verwandeln
Das Team sammelte kontrastverstärkte CT‑Aufnahmen von 280 Patienten, bei denen die Nierentumoren bereits histologisch bestätigt worden waren. Experten radiologen zogen die Tumorränder sorgfältig, Schicht für Schicht, nach, um präzise „Ground‑Truth“‑Regionen bereitzustellen, aus denen das System lernen konnte. Verwendet wurde nur eine CT‑Phase – die portalvenöse Phase, die in der Routineversorgung gebräuchlich ist – um zu betonen, dass die Methode mit Standard‑Krankenhausaufnahmen funktionieren soll. Der Datensatz umfasste schließlich fünf klar beschriftete Gruppen: 84 ccRCC, 36 pRCC, 48 chRCC, 72 AML und 40 RO‑Fälle, verteilt über ein breites Alterspektrum und beide Geschlechter. Die Fälle wurden davon patientenbasiert in Trainings‑, Validierungs‑ und Testsets aufgeteilt, sodass Aufnahmen derselben Person nie in mehr als einer Gruppe vorkamen.
Eine schrittweise digitale Zweitmeinung
Anstatt das System direkt vom Bild zu einer von fünf Klassen springen zu lassen, entwarfen die Forscher eine stufenweise Entscheidungs‑Pipeline, die dem klinischen Denkprozess eines Arztes ähnelt. Zuerst entscheidet das System, ob ein Tumor gutartig oder bösartig ist. Ist er gutartig, trennt eine zweite Entscheidung AML von RO. Bei bösartigen Tumoren trennt eine weitere Stufe ccRCC von den anderen RCC‑Typen, gefolgt von einem letzten Schritt, der pRCC von chRCC unterscheidet. In jeder Stufe analysiert ein leistungsfähiges Bildverarbeitungsmodul – ein Convolutional Neural Network – viele Schichten desselben Patienten. Die internen numerischen „Features“ werden danach auf drei verschiedene Arten verarbeitet: durch einfaches Mittelwertbilden der Schicht‑Vorhersagen, durch ein sequenzbewusstes Modell, das die Veränderungen des Tumors über die Schichten betrachtet, und durch ein kompaktes Kodierungsnetzwerk, das den gesamten Schichtstapel in eine einzige Signatur zusammenfasst. Die drei Einschätzungen werden zu einer finalen Wahrscheinlichkeit für diese Stufe kombiniert.
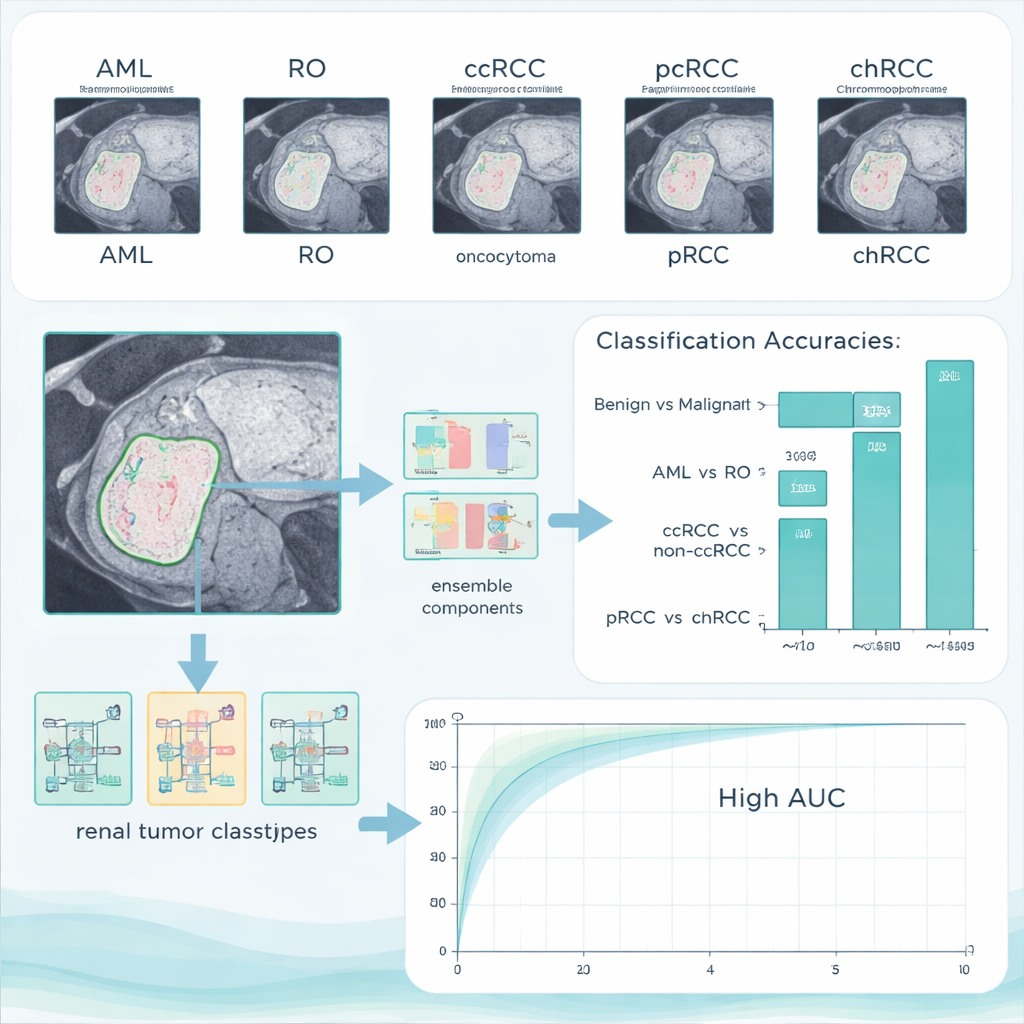
Wie gut das KI‑System abschnitt
Auf ihrem Haupttestset erreichte das kombinierte System eine Genauigkeit von 96,4 % bei der Trennung gutartiger von bösartigen Tumoren, wobei keine gutartigen Fälle fälschlich als Krebs eingestuft wurden und nur eine kleine Zahl von Krebserkrankungen übersehen wurde. Bei der Unterscheidung der beiden gutartigen Typen erzielte es eine perfekte Genauigkeit von 100 %. Die anspruchsvolleren Aufgaben – die Unterscheidung von ccRCC gegenüber den anderen RCC‑Typen sowie papilläres gegenüber chromophobem Krebs – waren schwieriger, doch das System erreichte auch hier Genauigkeiten von über 90 %. Wichtig ist, dass die Autoren ihr trainiertes Modell auch an einem völlig anderen, öffentlich verfügbaren Datensatz getestet haben, der anderswo erhoben wurde. Die Leistung blieb hoch, was darauf hindeutet, dass die Methode nicht nur die Bildgebung eines einzelnen Krankenhauses auswendig lernt, sondern auf neue Patienten und Scanner generalisierbar ist.
Was das für Patienten bedeuten könnte
Einfach ausgedrückt zeigt diese Forschung, dass ein KI‑„Assistent“ Nieren‑CTs so lesen kann, dass er aktuellen manuellen Methoden zur Trennung harmloser von gefährlichen Läsionen und zur Identifikation wichtiger Krebs‑Subtypen sehr nahekommt und sie in manchen Aspekten übertrifft. Bei weiterer Validierung könnte ein solches System Radiologen helfen, unnötige Biopsien und Operationen bei gutartigen Tumoren zu vermeiden und zugleich mehr Sicherheit bei frühen Therapieentscheidungen für aggressive Tumoren zu geben. Für Patientinnen und Patienten könnte das weniger invasive Eingriffe, schnellere Antworten und eine stärker personalisierte Behandlung entsprechend der genauen Natur ihres Nierentumors bedeuten.
Zitation: Abdeltawab, H., Alksas, A., Ghazal, M. et al. A deep learning ensemble framework for multi-subtype renal tumor classification using contrast-enhanced CT. Sci Rep 16, 6657 (2026). https://doi.org/10.1038/s41598-026-37283-7
Schlüsselwörter: Nierenkrebs, Bildgebung von Nierentumoren, Deep Learning, CT‑Scan, computerassistierte Diagnose