Clear Sky Science · de
Integrierte Analyse globaler Regulatoren und Efflux‑Gene, die mit der Umkehr der antimikrobiellen Resistenz bei multiresistenten Klebsiella pneumoniae assoziiert sind
Warum diese Krankenhauskeime so schwer zu töten sind
In Krankenhäusern weltweit sind bestimmte Stämme des Bakteriums Klebsiella pneumoniae notorisch schwer zu behandeln geworden. Sie wehren sich gegen mehrere Antibiotika, die einst zuverlässig wirkten, und verwandeln routinemäßige Infektionen in lebensbedrohliche Notfälle. Diese Studie blickt unter die mikrobiologische Haube, um einen wichtigen Trick dieser Bakterien zu verstehen: mikroskopische Pumpen, die Antibiotika wieder aus der Zelle herausschleudern, und die genetischen Schalter, die diese Pumpen hoch- oder herunterregeln.
Superkeime und ihre molekularen Fluchtklappen
Multiresistente Klebsiella pneumoniae-Stämme werden inzwischen in vielen Krankenhäusern angetroffen, auch in dem irakischen medizinischen Zentrum, in dem diese Forschung durchgeführt wurde. Diese Bakterien können mehrere große Antibiotikagruppen gleichzeitig überleben, wie Fluorchinolone, Aminoglykoside und Cephalosporine der dritten Generation. Eine Strategie, die sie dabei nutzen, ist das Einbauen leistungsfähiger „Effluxpumpen“ in ihre Zellhülle. Eine der wichtigsten ist ein System namens AcrAB‑TolC, das die bakteriellen Membranen durchspannt und wie eine winzige Schmutzwasserpumpe funktioniert: Es greift Antibiotikamoleküle im Inneren der Zelle und drückt sie wieder nach außen, bevor die Wirkstoffe ernsthaften Schaden anrichten können. Sind diese Pumpen sehr aktiv, steigt die Antibiotikakonzentration innerhalb des Bakteriums nie hoch genug, um tödlich zu wirken.
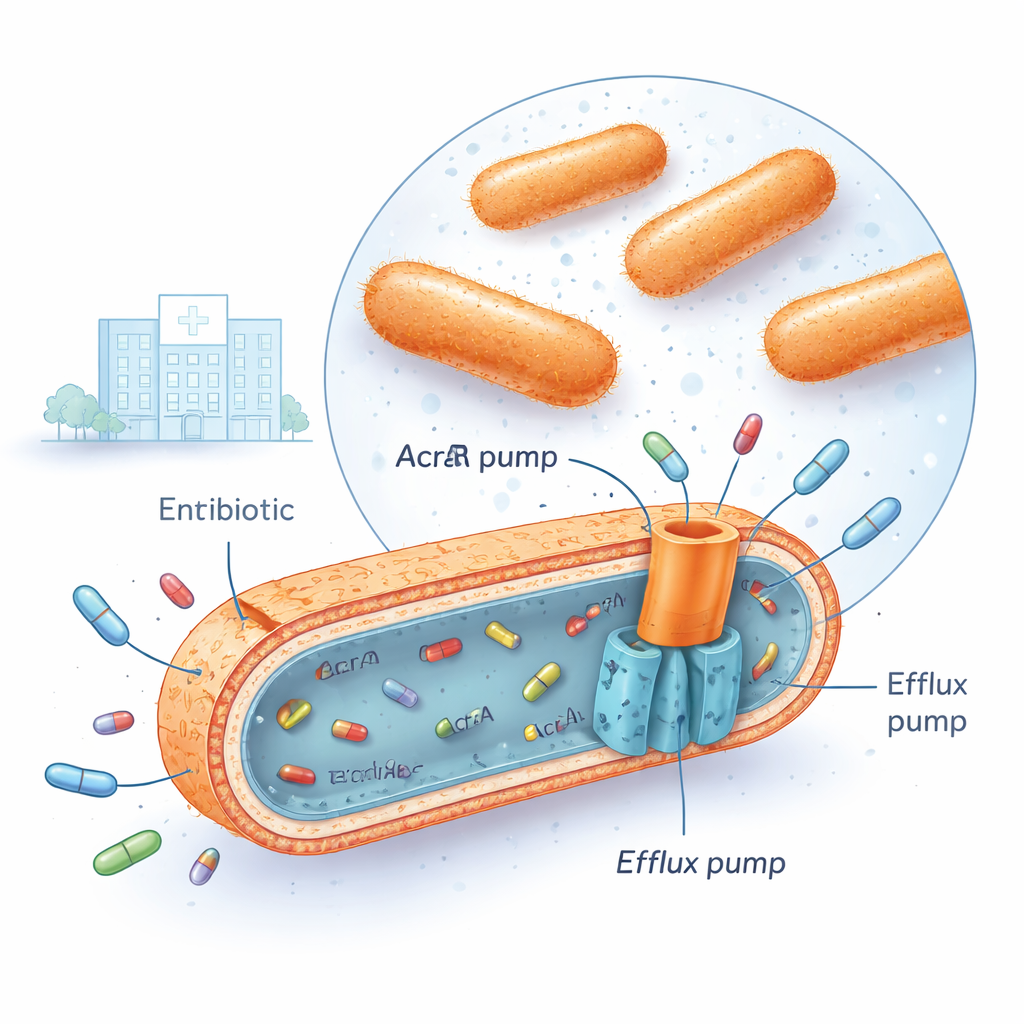
Genschalter, die mit Pumpenüberdreh auftreten
Die Forschenden sammelten 30 multiresistente klinische Isolate von Klebsiella pneumoniae und verglichen sie mit 10 antibiotikaempfindlichen Isolaten sowie einem Standardreferenzstamm. Mithilfe einer Technik namens quantitativer Echtzeit‑PCR maßen sie, wie stark bestimmte Gene eingeschaltet sind. Sie konzentrierten sich auf drei „globale Regulatoren“—die Gene marA, soxS und rob—sowie auf die drei Komponenten der AcrAB‑TolC‑Pumpe selbst (acrA, acrB und tolC). In den resistenten Stämmen waren zwei Regulatoren, marA und soxS, typischerweise etwa vier- bis fünffach hochreguliert im Vergleich zu empfindlichen Bakterien, während acrB, eine zentrale Pumpenkomponente, nahezu achtfach erhöht war. Statistische Analysen zeigten, dass bei hohen marA- und soxS-Spiegeln meist auch acrB-Spiegel erhöht waren und diese Stämme tendenziell deutlich höhere Dosen von Fluorchinolon‑Antibiotika wie Ciprofloxacin aushielten. Ein dritter Regulator, rob, veränderte sich kaum und stand nicht in Einklang mit der Pumpenaktivität, was darauf hindeutet, dass er unter den getesteten Bedingungen eine kleinere Rolle spielt.
Die Pumpen abschalten, um die Resistenz zu schwächen
Die Beobachtung, dass Pumpen‑ und Regulatorgene gemeinsam aktiv sind, ist aussagekräftig, aber nicht ausreichend, um zu beweisen, dass sie tatsächlich die Resistenz antreiben. Um zu testen, ob die Pumpen funktionell wichtig sind, griff das Team zu einem chemischen Werkzeug namens PAβN. Diese Verbindung wird nicht als Medikament beim Menschen verwendet, kann im Labor aber AcrAB‑TolC‑ähnliche Pumpen blockieren und deren Auswurf von Antibiotika stoppen. Die Wissenschaftler wählten zehn resistente Isolate mit besonders hohen acrB-Werten und bestimmten, wie viel Ciprofloxacin nötig war, um ihr Wachstum zu stoppen – mit und ohne PAβN. In acht dieser zehn Stämme senkte das Blockieren der Pumpe die erforderliche Ciprofloxacin‑Dosis mindestens vierfach und teilweise bis zu sechzehnfach. Dieser Rückgang zeigt, dass in vielen dieser Superkeime aktive Effluxpumpen tatsächlich ein Hauptgrund dafür sind, dass sie hohe Antibiotikadosen tolerieren.
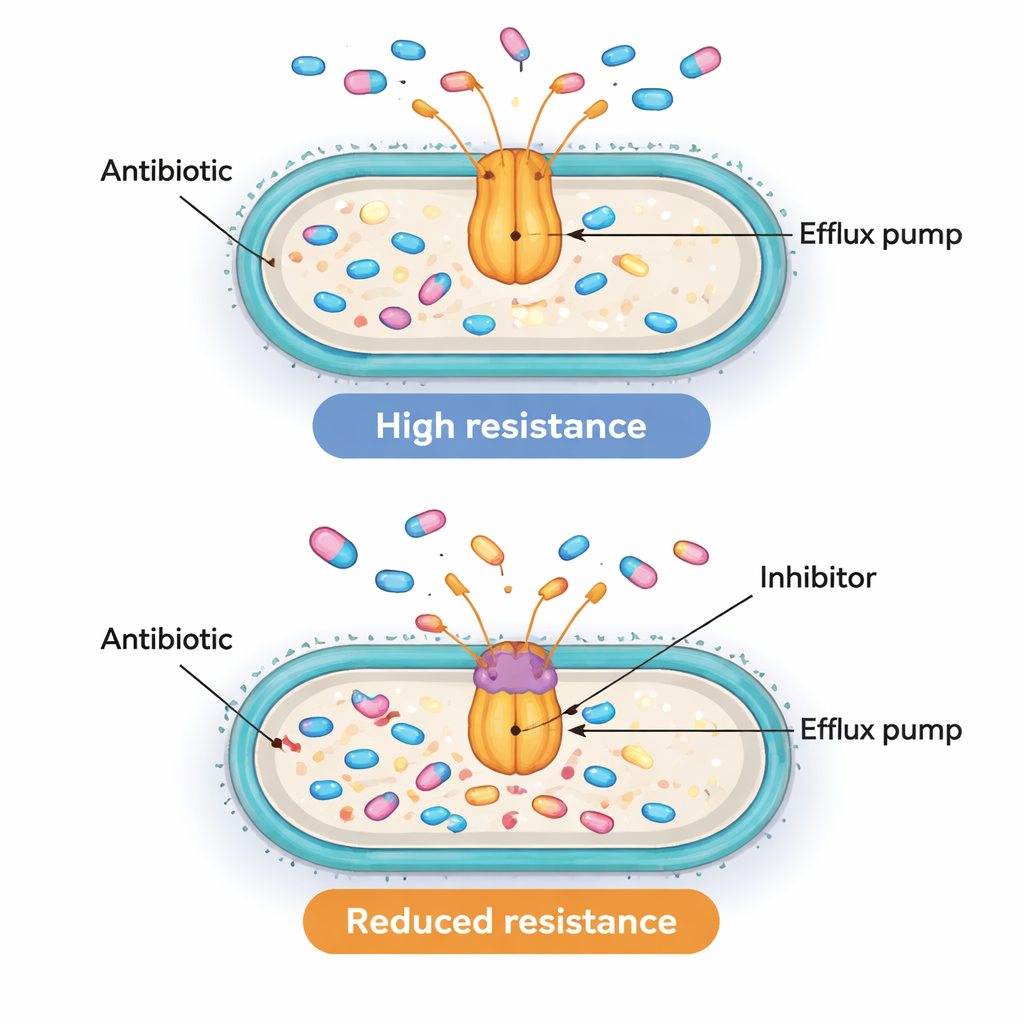
Ein komplexes Resistenzrätsel mit vielversprechenden Angriffspunkten
Nicht jeder Stamm verhielt sich gleich. Einige Bakterien mit stark exprimierten Pumpengene gewannen nur teilweise an Empfindlichkeit zurück, wenn die Pumpen blockiert wurden. Das deutet darauf hin, dass weitere Resistenzmechanismen—etwa Veränderungen am Zielort des Antibiotikums innerhalb der Zelle, Produktion von wirkungszerstörenden Enzymen oder alternative Pumpen—ebenfalls beitragen. Gentamicin, ein Aminoglykosid‑Antibiotikum, blieb zum Beispiel weitgehend unbeeinflusst von den in marA/soxS und AcrAB‑TolC gesehenen Mustern, was unterstreicht, dass Multiresistenz in der Regel aus mehreren sich überschneidenden Verteidigungsmechanismen besteht und nicht aus einem einzelnen Mechanismus.
Was das für künftige Behandlungen bedeutet
Für Nicht‑Spezialisten ist die zentrale Botschaft: Einige Krankenhausbakterien überleben Antibiotika nicht nur durch Blockieren oder Spalten der Wirkstoffe, sondern indem sie sie aktiv herausschleudern. Diese Studie verbindet eine höhere Aktivität von zwei genetischen „Schaltern“, MarA und SoxS, mit aktiveren Effluxpumpen und stärkerer Resistenz gegen eine häufig verwendete Antibiotikaklasse. Werden die Pumpen experimentell blockiert, werden viele dieser Bakterien zumindest teilweise wieder empfänglich. Auch wenn die Arbeit noch nicht genau belegt, wie diese Schalter die Pumpen steuern, hebt sie sowohl die Regulatoren als auch die Pumpen als attraktive Ziele hervor. Langfristig könnte die Kombination herkömmlicher Antibiotika mit sicheren Pumpenblockern—oder mit Wirkstoffen, die diese globalen Regulatoren herunterfahren—dazu beitragen, die Wirksamkeit bestehender Behandlungen gegen ansonsten schwer zu behandelnde multiresistente Infektionen wiederherzustellen.
Zitation: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Schlüsselwörter: antibiotikaresistenz, Effluxpumpen, Klebsiella pneumoniae, Fluorchinolone, Resistenzumkehr