Clear Sky Science · de
Die Herunterregulierung des deubiquitinierenden Enzyms USP10 korreliert mit neuronalem Zelltod bei HTLV-1-assoziierter Myelopathie
Warum das für Menschen mit viralen Nervenerkrankungen wichtig ist
Einige Viren verursachen nicht nur kurzzeitige Infektionen; sie können über viele Jahre hinweg stillschweigend das Nervensystem schädigen. Das Humane T‑Zell-Leukämie-Virus Typ 1 (HTLV‑1) ist ein solches Virus und kann zu einer chronischen Rückenmarkserkrankung führen, die als HTLV‑1-assoziierte Myelopathie (HAM) bezeichnet wird. Menschen mit HAM verlieren allmählich Kraft und Kontrolle in den Beinen, verbunden mit Blasen- und Sensibilitätsstörungen. Diese Studie stellt eine einfache, aber entscheidende Frage: Warum sterben in dieser Erkrankung Nervenzellen im Rückenmark, und könnte ein einzelnes schützendes Molekül erklären, wer besser oder schlechter davonkommt?
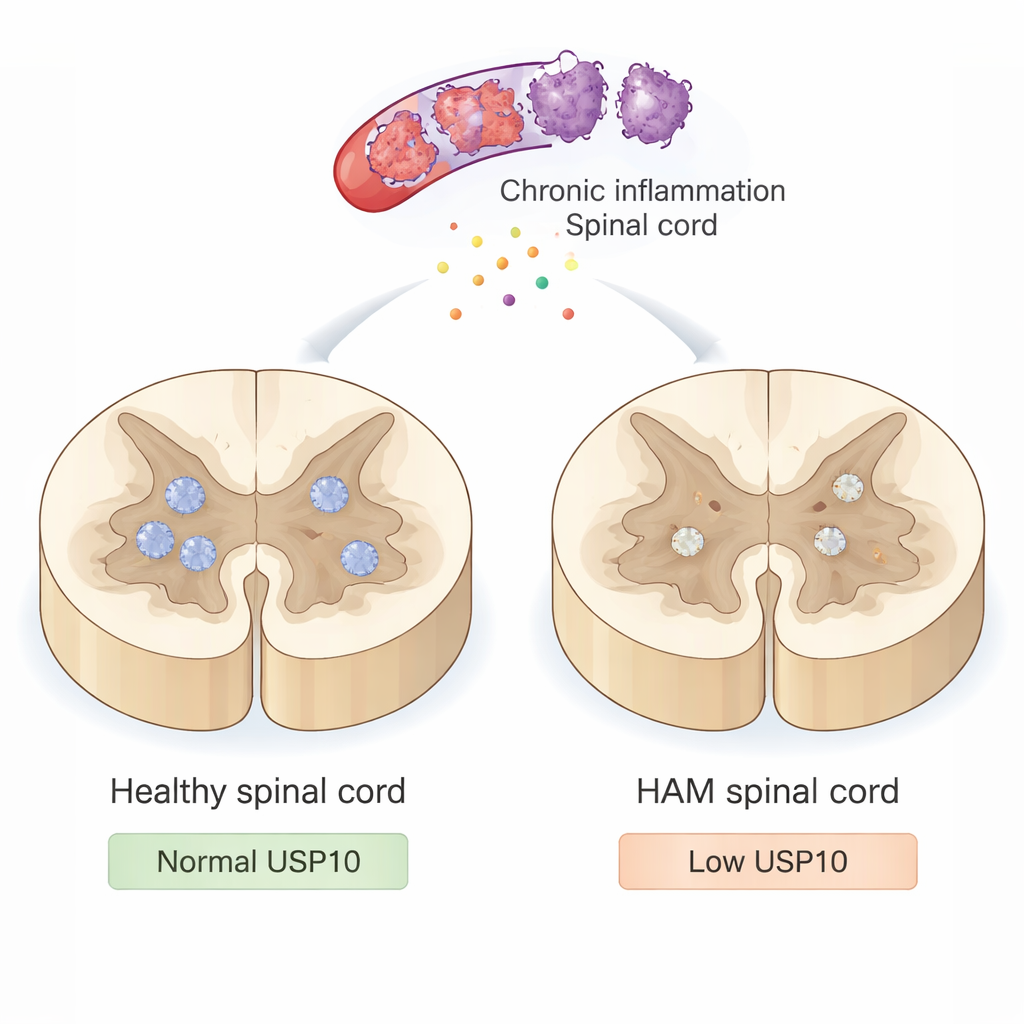
Ein langsamer Angriff auf das Rückenmark
HAM wird nicht dadurch verursacht, dass das Virus direkt Nervenzellen infiziert. Stattdessen infiziert HTLV‑1 Immunzellen, die in das Rückenmark eindringen und lang anhaltende Entzündungen auslösen. Diese überaktivierten Immunzellen setzen toxische Substanzen und entzündliche Signale frei, die zwar der Infektionskontrolle dienen sollen, gleichzeitig aber benachbarte Neurone und ihre isolierende Myelinschicht schädigen. Im Laufe der Zeit führt dieser schwelende Angriff zu steifen, schwachen Beinen und Gehproblemen. Trotzdem verstehen Ärztinnen und Ärzte noch nicht vollständig, warum einige Neurone diesem entzündlichen Umfeld zum Opfer fallen, während andere Jahrzehnte überleben.
Ein zelluläres „Aufräum“-Enzym unter Verdacht
Die Forschenden konzentrierten sich auf ein Protein namens USP10, ein Enzym, das das Proteinqualitätskontrollsystem der Zelle unterstützt und dafür bekannt ist, zellulären Stress und programmierte Zellsterben (Apoptose) zu begrenzen. USP10 ist in vielen Geweben aktiv, einschließlich Gehirn und Rückenmark, und frühere Arbeiten bei Parkinson, Schlaganfall und anderen Erkrankungen legen nahe, dass es Neurone gegen oxidative und entzündliche Schäden schützt. Mithilfe von Rückenmarksproben von acht Menschen, die mit HAM gestorben waren, und zwei neurologisch gesunden Kontrollen verwendete das Team Färbetechniken, um zu sehen, wo USP10 vorhanden war und wie stark es in Nervenzellen exprimiert wurde.
Weniger USP10, mehr sterbende Neurone
In gesunden Rückenmarken war USP10 in vielen Neuronen stark sichtbar. In den meisten HAM-Fällen war die USP10-Färbung in Neuronen jedoch deutlich reduziert, und bei einem Patienten war sie nahezu nicht vorhanden. Die Wissenschaftler suchten dann nach Kennzeichen der Apoptose mit zwei Methoden: einem TUNEL-Test, der fragmentierte DNA nachweist, und einer Färbung für aktives Caspase‑3, ein Protein, das früh im Zellsterbeprozess beteiligt ist. Bei den Kontrollen zeigten praktisch keine Neurone diese Todeszeichen. Im Gegensatz dazu waren bei HAM-Patienten viele Neurone TUNEL-positiv, und viele zeigten aktives Caspase‑3. Wichtig ist, dass Proben mit niedriger USP10-Expression tendenziell mehr apoptotische Neurone und weniger überlebende Neurone aufwiesen, markiert durch NeuN, einen gängigen neuronalen Marker. Ein bemerkenswerter HAM-Patient, der nach 22 Jahren noch mit nur einem Stock gehen konnte, zeigte starke USP10-Expression und vergleichsweise erhaltene Neuronenzahlen, was darauf hindeutet, dass höherer USP10-Spiegel vor schwerer Behinderung schützen könnte.
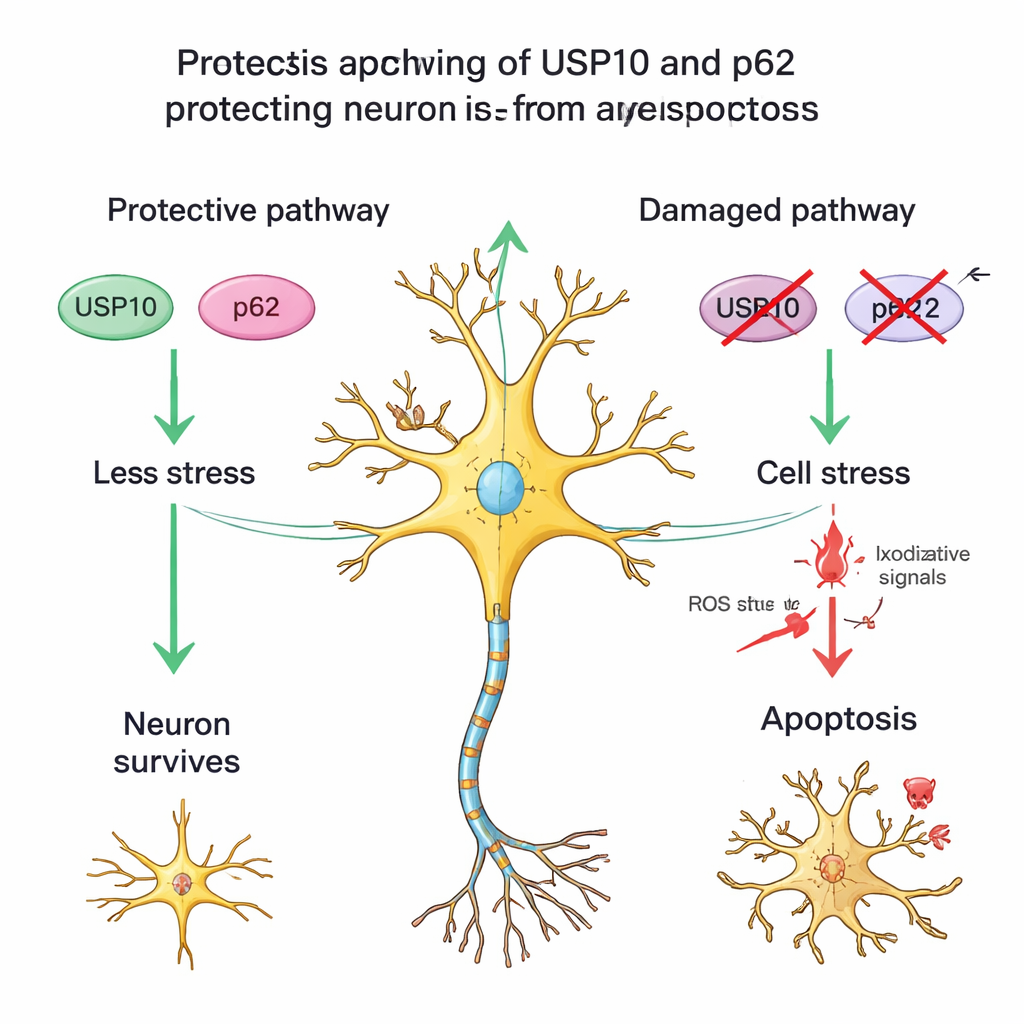
Ein Partnerprotein und gestresste, aber überlebende Zellen
Das Team untersuchte außerdem ein weiteres Protein, p62, das mit USP10 bei der Handhabung beschädigter Proteine sowie der Regulation von Stress- und Überlebenswegen zusammenarbeitet. In gesunden Rückenmarken war die p62-Färbung mäßig; bei HAM-Patienten hatten diejenigen mit niedrigem USP10 oft ebenfalls eine schwächere p62-Färbung und weniger überlebende Neurone. Dieses Muster stützt die Idee einer USP10–p62-Partnerschaft, die Neurone hilft, chronische Entzündungen zu überstehen. Die Forschenden bemerkten außerdem viele Neurone im HAM-Gewebe, die zwar die typische Gestalt von Nervenzellen aufwiesen, aber die NeuN-Färbung verloren hatten — ein Zeichen, das auch bei anderen Hirnverletzungen beobachtet wird, wenn Neurone unter erheblichem Stress stehen, aber noch nicht vollständig abgestorben sind. Das legt nahe, dass bei HAM einige Neurone nicht nur verloren gehen, sondern andere in einem geschädigten, verletzlichen Zustand verharren, möglicherweise weil USP10-verbundene Abwehrmechanismen geschwächt sind.
Was das für zukünftige Diagnose und Behandlung bedeuten könnte
Diese Studie beweist nicht, dass der Verlust von USP10 direkt das Absterben von Neuronen verursacht, da sie auf einer kleinen Zahl von Autopsieproben basiert und Veränderungen über die Zeit nicht nachverfolgen kann. Dennoch deuten die konsistenten Zusammenhänge zwischen niedrigem USP10, reduziertem p62, verstärkten Apoptosezeichen und weniger überlebenden Neuronen auf einen gemeinsamen Weg hin, der chronische Entzündung und langsame neuronale Degeneration bei HAM verbinden könnte. Für Patientinnen und Patienten eröffnet sich damit eine ermutigende Möglichkeit: Das Messen oder Verstärken von USP10-verwandten Signalwegen im Rückenmark — oder möglicherweise in besser zugänglichen Proben wie Liquor — könnte eines Tages helfen, jene mit höherem Risiko für rasche Progression zu identifizieren, das Monitoring zu leiten oder neue Therapien zu inspirieren, die das zelleigene Stressschutzsystem bei virusbedingten neuroinflammatorischen Erkrankungen stärken.
Zitation: Arishima, S., Takahashi, M., Dozono, M. et al. Downregulation of the deubiquitinating enzyme USP10 correlates with neuronal apoptosis in HTLV-1-associated myelopathy. Sci Rep 16, 6062 (2026). https://doi.org/10.1038/s41598-026-37271-x
Schlüsselwörter: HTLV-1-assoziierte Myelopathie, Neuroinflammation, neuronaler Apoptose, USP10, Rückenmarksdegeneration