Clear Sky Science · de
Antibakterielle Aktivität und Zytotoxizität von trikalziumsilikatbasierten Zementen mit verschiedenen antibakteriellen Zusätzen
Warum das für Ihre nächste Füllung wichtig ist
Bei einer tiefen Karies versuchen Zahnärzte heute, so viel natürlichen Zahn wie möglich zu erhalten, statt alles wegzuschleifen. Das bedeutet häufig, dass unter der Füllung eine dünne Schicht aufgeweichter, bakterienhaltiger Dentinreste zurückbleibt. Diese Studie stellt eine einfache, aber entscheidende Frage: Kann man einen weit verbreiteten Zahnreparaturzement so verändern, dass er unauffällig verbliebene Keime abtötet, ohne die lebenden Zellen im Zahn zu schädigen?
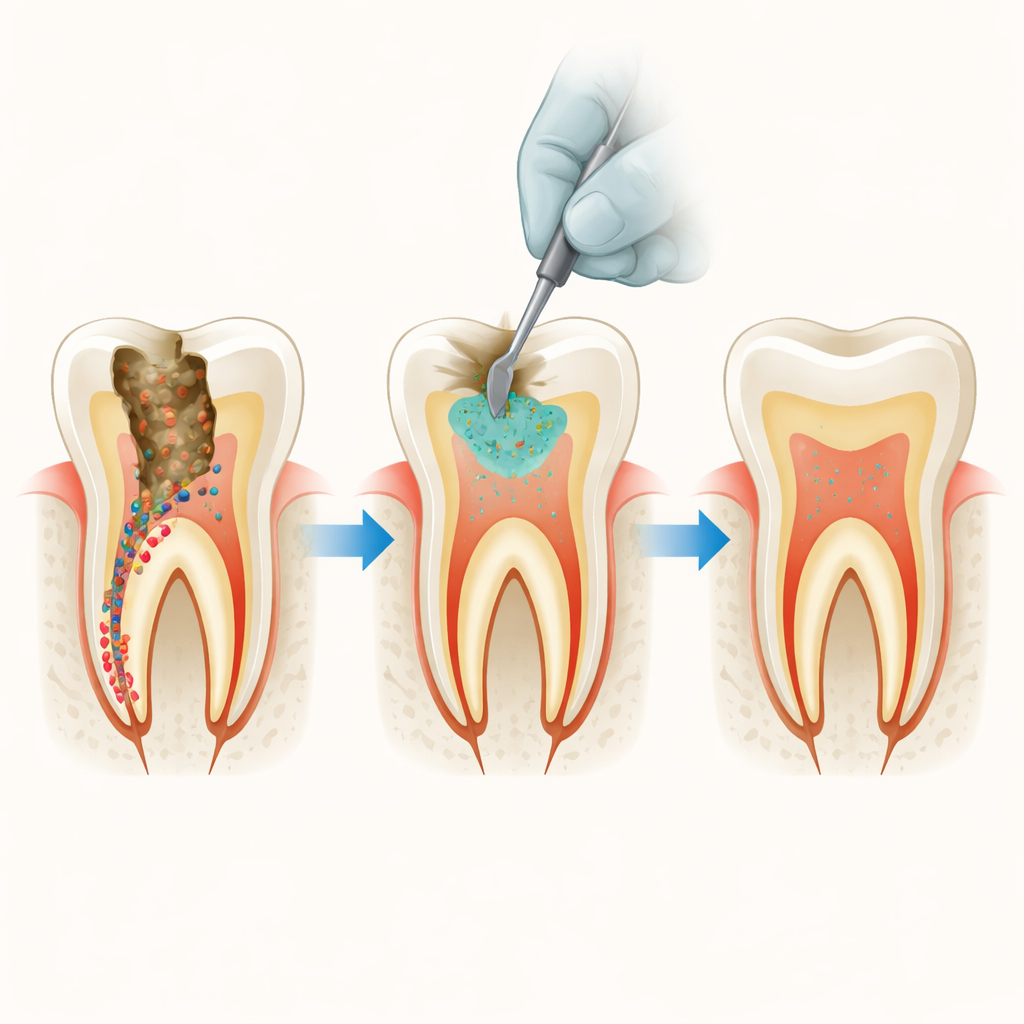
Tiefe Karies und verborgene Keime
Moderne „minimalinvasive“ Techniken zielen darauf ab, das weiche Innere des Zahns, die Pulpa, nicht freizulegen, indem Dentin stehenbleibt, das wieder aushärten kann. Der Nachteil ist, dass einige kariesauslösende Bakterien, wie Streptococcus mutans und Lactobacillus‑Arten, in dieser Schicht verbleiben können. Mit der Zeit können diese Bakterien unter einer scheinbar intakten Füllung neuen Zerfall auslösen. Trikalziumsilikatbasierte Zemente sind beliebt zum Verschließen tiefer Kavitäten, weil sie die Remineralisation unterstützen und eine dichte Barriere bilden, allein sind sie jedoch nicht sehr wirkungsvoll gegen Bakterien.
Aus einem gebräuchlichen Zement einen Keimkämpfer machen
Die Forscher nahmen diesen bekannten Zement und mischten fünf verschiedene antibakterielle Zusätze in unterschiedlichen Konzentrationen bei. Zwei waren organische Verbindungen, die häufig in Desinfektionsmitteln vorkommen (Benzalkoniumchlorid und Cetrimid), und drei waren anorganische Substanzen, die in dentalen Produkten oder Materialien verwendet werden (Titanoxid, Zinkoxid und Zinnfluorid). Sie pressten diese Mischungen zu winzigen Scheiben und legten sie auf Platten, die mit fünf Bakterienarten bedeckt waren, die mit Zahnhohlräumen und oralen Infektionen in Verbindung stehen. Durch das Messen der klaren Zonen um jede Scheibe, in denen kein Bakterienwachstum stattfand, konnten sie sehen, wie stark jede Rezeptur Keime zurückhielt.
Die Balance finden zwischen Keimtötung und Zellschonung
Da ein Material, das Bakterien tötet, aber auch Zahnzellen vergiftet, im Mund nutzlos wäre, untersuchte das Team außerdem, wie die vielversprechendsten Zusätze lebende Zellen beeinflussen. Sie setzten zwei menschliche Zelltypen—Fibroblasten, die als häufige Stütz‑Zellen dienen, und pulpanaher Zahnmarksstammzellen, die bei der Reparatur von Zahngewebe helfen—indirekt den Zementen aus. Ein Farbwechseltest maß, wie viele Zellen aktiv blieben, und spezielle fluoreszierende Farbstoffe zeigten lebende (grün) und tote (rot) Zellen unter dem Mikroskop. Dieses Setting ahmte die reale Situation in einer tiefen Kavität nach, bei der der Zement durch eine dünne Dentinschicht von der Pulpa getrennt ist und Substanzen abgibt, die zu den Zellen diffundieren.
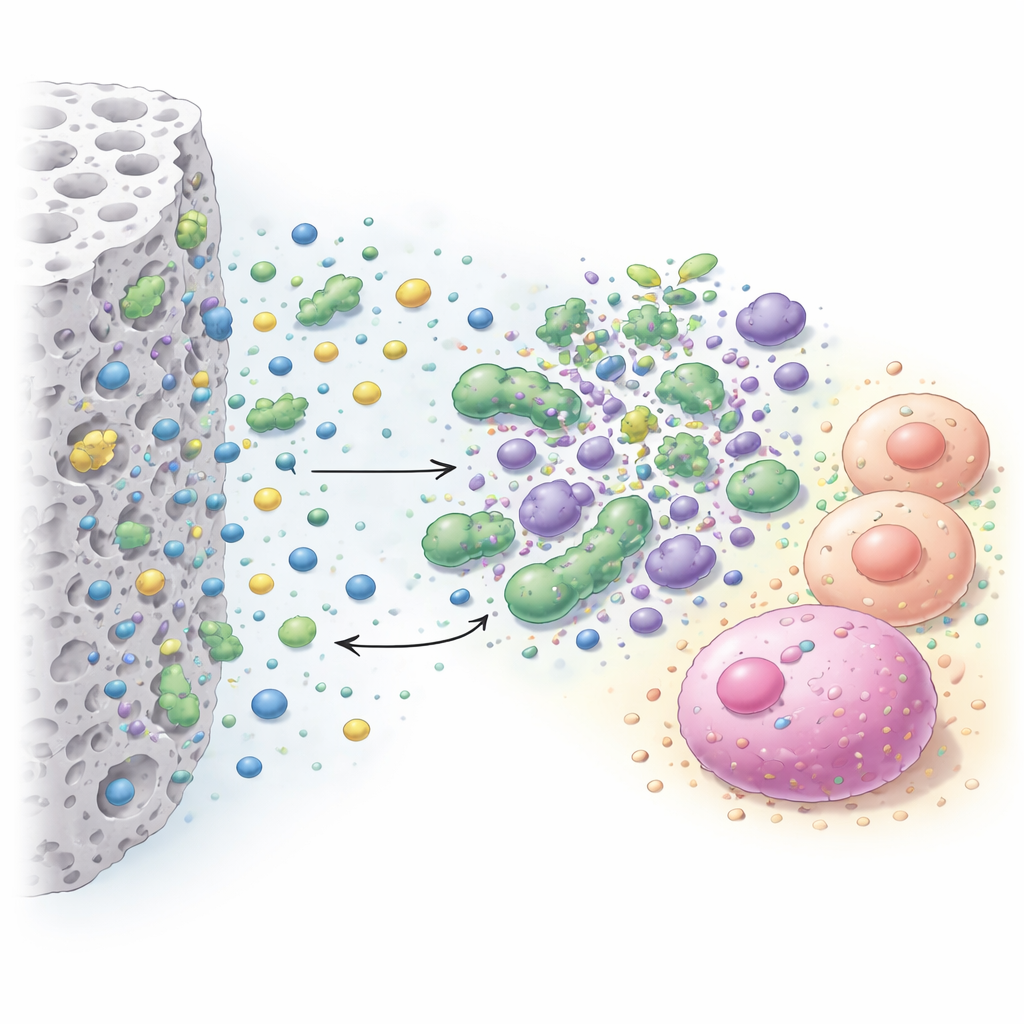
Was am besten wirkte und was zu scharf war
Die Ergebnisse zeigten, dass Art und Menge des Zusatzes stark ins Gewicht fielen. Benzalkoniumchlorid zeigte die stärkste und breiteste antibakterielle Wirkung und erzeugte große keimfreie Zonen gegen alle getesteten Spezies, insbesondere gegen die Lactobacillus‑Stämme, die häufig in tiefer Karies vorkommen. Cetrimid half ebenfalls, benötigte aber im Allgemeinen höhere Konzentrationen, um die Leistung von Benzalkonium zu erreichen. Die drei anorganischen Wirkstoffe verbesserten die antibakterielle Wirkung des Zements nur bei höheren getesteten Dosen und auch dann hauptsächlich gegen bestimmte Bakterien wie S. mutans und Actinomyces. Was die Sicherheit betrifft, so war der Basiszement allein für beide Zelltypen verträglich und schien sogar die Fibroblasten zu unterstützen. Die Zugabe von Benzalkoniumchlorid blieb für Fibroblasten bis etwa 1 % ungefährlich, wurde bei 2–4 % leicht schädlich und bei 7 % deutlich toxisch. Die pulpanahen Stammzellen waren insgesamt empfindlicher: Sowohl Benzalkoniumchlorid als auch Cetrimid reduzierten ihr Überleben, wobei Cetrimid ab etwa 2 % mäßig toxisch wirkte.
Was das für die zukünftige Zahnmedizin bedeuten könnte
In der Gesamtschau deutet die Studie auf ein besonders vielversprechendes Rezept hin: ein trikalziumsilikatbasierter Zement mit 1 % Benzalkoniumchlorid. Auf diesem Niveau unterdrückte das Material schädliche Bakterien stark, während Fibroblasten völlig intakt blieben und pulpanahen Stammzellen größtenteils lebensfähig blieben. In praktischen Worten deutet das darauf hin, dass zukünftige tiefe Füllungen aus einem Zement bestehen könnten, der unauffällig verbliebene Keime unter der Oberfläche bekämpft und gleichzeitig schonend genug für das lebende Gewebe im Zahn bleibt. Weitere Arbeiten sind nötig—insbesondere unter den komplexen, realen Bedingungen im Mund—aber diese ausgewogene Formel könnte Zahnärzten helfen, Zähne bei minimalinvasiven Behandlungen besser zu schützen.
Zitation: Banon, R., Martens, L., De Coster, P. et al. Antibacterial activity and cytotoxicity of tricalcium silicate-based cements with different antibacterial additives. Sci Rep 16, 8349 (2026). https://doi.org/10.1038/s41598-026-37269-5
Schlüsselwörter: tiefe Zahnkaries, antibakterieller Zahnzement, trikalziumsilikat, Benzalkoniumchlorid, Biokompatibilität von Pulpa‑Zellen