Clear Sky Science · de
Darstellung interzellulärer Biomoleküle mit fluoreszenten Proteinindikatoren und Lipid‑PEG‑Ankern
Zellen beim Gespräch in Echtzeit beobachten
Unser Gehirn und Körper beruhen auf einem fortwährenden chemischen Austausch zwischen Zellen. Ionen und Neurotransmitter transportieren Nachrichten über winzige Spalten — diese schnellen, kurzlebigen Signale sind jedoch schwer zu sehen, ohne sie zu stören. In dieser Studie wird ein einfacher Weg vorgestellt, lebende Zellen mit leuchtenden Sensoren „zu bemalen“, die sich an ihre Außenseite anheften und es Forschern ermöglichen, diese Nachrichten — insbesondere Kaliumionen und den Neurotransmitter Glutamat — live und detailliert zu verfolgen. 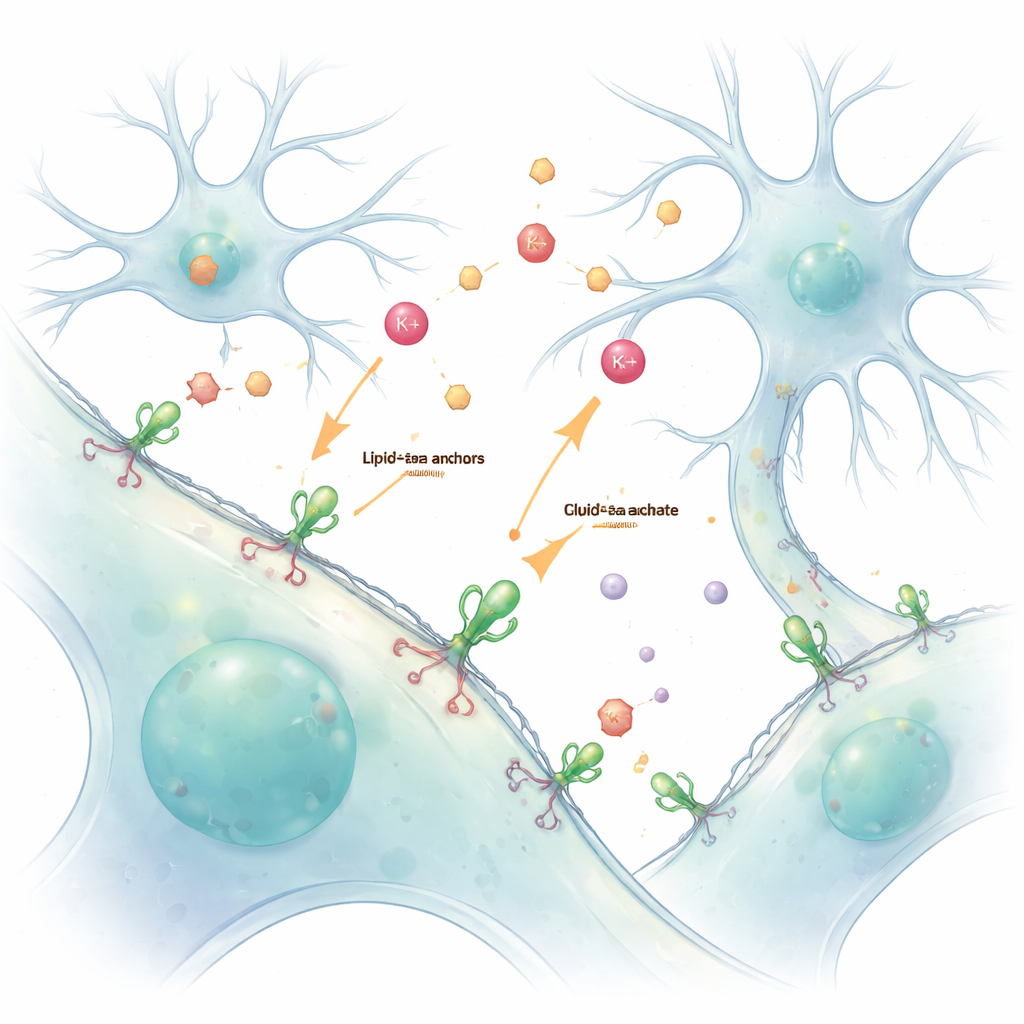
Eine neue Methode, die Zelloberfläche zu markieren
Traditionell bringen Forschende Zellen dazu, fluoreszierende Proteinsensoren über deren eigene DNA herzustellen. Obwohl mächtig, führt dieser genetische Ansatz oft dazu, dass die Sensoren im Zellinneren landen, wodurch es schwierig wird, Innen- und Außenvorgänge zu trennen. Die Autoren lösten dies mithilfe einer chemischen Griffhilfe, einem Lipid–PEG‑Anker. Ein Ende dieses Moleküls steckt sich in die äußere Membran, während das andere Ende chemisch mit einem fluoreszenten Proteinsensor verbunden ist. Werden diese vorbereiteten Sensoren einfach zu lebenden Zellen hinzugegeben, überziehen sie spontan die Außenseite und bilden eine stabile, leuchtende Schicht, die berichtet, was in der umgebenden Flüssigkeit geschieht.
Kalium und Glutamat in Licht verwandeln
Das Team passte zwei bestehende fluoreszente Indikatoren an: GINKO2, das auf Kaliumionen reagiert, und R‑iGluSnFR1, das auf Glutamat anspricht. Sie reinigten diese Proteine aus Bakterien und befestigten anschließend die Lipid–PEG‑Anker. In kultivierten menschlichen Zellen bildete der verankerte Kaliumsensor eine klare Kontur entlang der Zelloberfläche und wurde heller, sobald extrazelluläres Kalium anstieg, und dunkelte wieder ab, wenn die Konzentration fiel. Wichtig ist, dass seine lichtemittierenden Eigenschaften und Empfindlichkeit im Wesentlichen mit dem ursprünglichen, unveränderten Sensor im Reagenzglas übereinstimmten — das Ankern beeinträchtigte die Leistungsfähigkeit nicht. Dasselbe galt für den Glutamatsensor, der nach dem Ankern weiterhin ansprechbar blieb und Glutamat deutlich im Raum direkt außerhalb der Zellen hervorhob.
Neuronen in Kulturen und Schnitten belauschen
Die Forschenden gingen dann zu Nervenzellen aus dem Maus‑Hippocampus über, einer Hirnregion, die für Lernen und Gedächtnis wichtig ist. Sie beschichteten diese Neuronen mit dem lipid–PEG‑verankerten Glutamatsensor und luden das Innere derselben Zellen mit einem separaten Calciumsfarbstoff, der elektrische Aktivität anzeigt. Mit totaler interne Reflexionsmikroskopie konnten sie rote Blitze von Glutamat an der Zelloberfläche beobachten, während grüne Signale innerhalb der Zellen das Feuern berichteten. Dieser zweifarbige Blick zeigte, dass die verankerten Sensoren spontane Neurotransmitterfreisetzung verfolgen konnten, ohne die Neuronen genetisch zu verändern.
Chemische Wellen im Hirngewebe kartieren
Als Nächstes testete das Team die Methode in akuten Hirnschnitten, die die natürliche Verschaltung des Hippocampus bewahren. Sie applizierten den verankerten Kaliumsensor auf Schnitten und reizten Nervenfasern elektrisch. Der verankerte Sensor erzeugte nach jedem Stimulus deutliche, wiederholbare Fluoreszenzanstiege, während nicht‑verankerte Sensoren schnell wegdiffundierten und schwache, instabile Signale lieferten. Durch das Bad der Schnitte in Lösungen mit bekannten Kaliumkonzentrationen und unter Korrektur für das eigene schwache Gewebe‑Nachleuchten erstellten die Autoren eine Kalibrierkurve und schätzten die tatsächlichen extrazellulären Kaliumkonzentrationen. Die Baseline lag bei etwa 2,5 Millimolar und stieg bei moderater Stimulation auf etwa 3,4 Millimolar — im Einklang mit klassischen Elektrodenmessungen. Verankerte Sensoren für sowohl Kalium als auch Glutamat zeigten, wie sich diese Signale unterschiedlich ausbreiten: Glutamatänderungen blieben nahe aktiver Synapsen, während Kaliumanstiege sich über Hunderte von Mikrometern erstreckten und auf breitere Effekte auf die Netzwerk‑Erregbarkeit hinweisen. 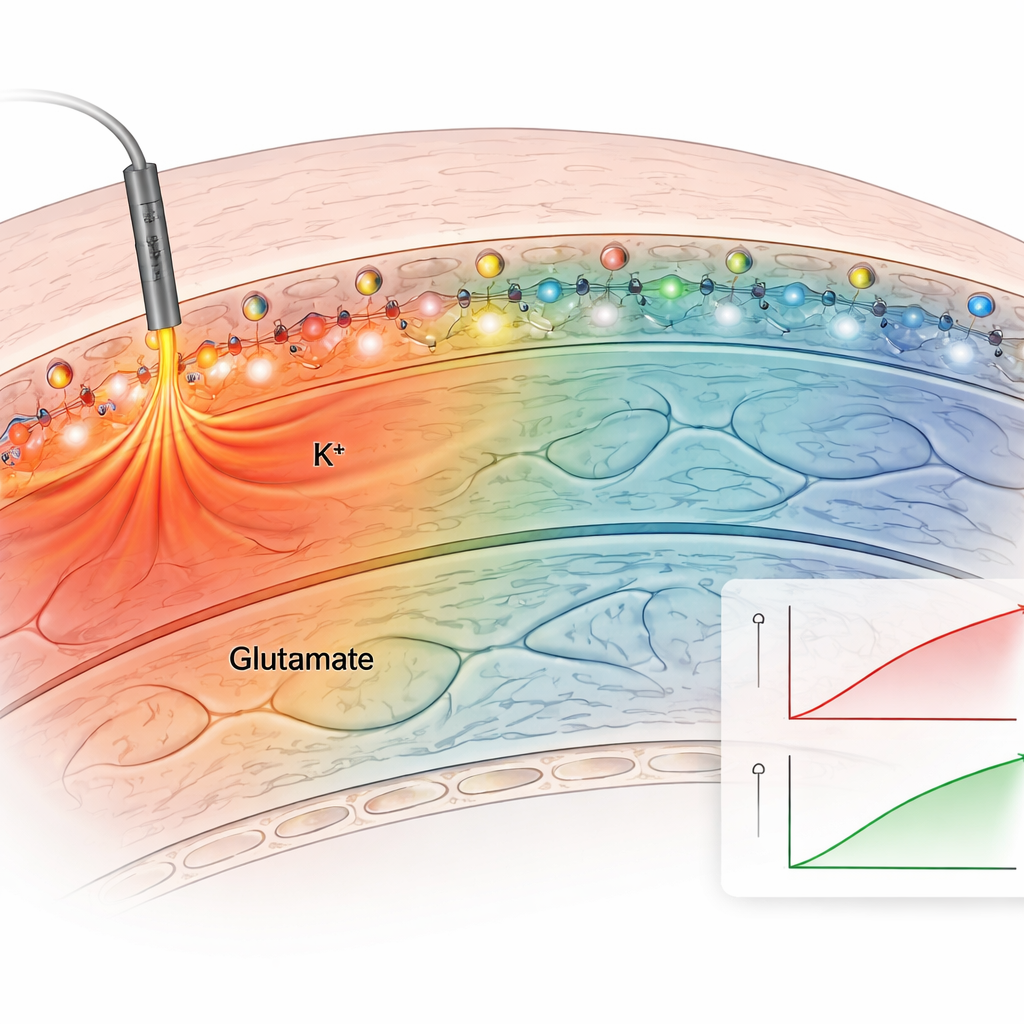
Untersuchen, wie das Gehirn Signale entfernt und erzeugt
Da die Sensoren an der Zelloberfläche fixiert sind, konnten die Autoren untersuchen, welche Prozesse diese extrazellulären Wellen formen. Das Blockieren von Glutamattransportern, die normalerweise Glutamat aufnehmen, führte dazu, dass der verankerte Glutamatsensor größere und länger anhaltende Signale zeigte — ein Beleg dafür, dass lokale Aufnahme die Ausbreitung von Glutamat begrenzt. Das Blockieren von AMPA‑Typ Glutamatrezeptoren reduzierte sowohl elektrische Antworten als auch Kaliumsignale, was darauf hindeutet, dass der Großteil des Kaliumanstiegs von postsynaptischen Neuronen stammt, die durch synaptische Eingänge aktiviert werden. Das Blockieren von Natriumkanälen mit Tetrodotoxin hob Kaliumänderungen nahezu vollständig auf und verband sie direkt mit Aktionspotenzialen. Zusammen veranschaulichen diese Experimente, wie verankerte Sensoren komplexe, verteilte Chemie in anschauliche Filme und Karten verwandeln können.
Warum das für künftige Hirnforschung wichtig ist
Für Nicht‑Spezialisten lautet die Kernbotschaft: Diese Arbeit bietet einen schnellen, nicht‑genetischen Weg, lebende Zellen und Gewebe mit hochempfindlichen molekularen Reportern zu beschichten. Statt jede Zellart neu zu gentechnisch zu verändern, können Forschende vorgefertigte Sensorproteine von außen hinzufügen und sofort sehen, wie sich Ionen und Neurotransmitter in Echtzeit an der Zelloberfläche verändern. Dieser Ansatz verbessert Kontrolle, Reproduzierbarkeit und räumliche Präzision und umgeht die Herausforderungen der Genübertragung, besonders in empfindlichen Präparationen wie akuten Hirnschnitten. Mit der Entwicklung weiterer fluoreszenter Indikatoren für unterschiedliche Chemikalien könnte die gleiche Lipid–PEG‑Ankerstrategie zu einem breit verwendeten Werkzeugkasten werden, um die chemische Sprache der Zellen im ganzen Körper zu beobachten.
Zitation: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Schlüsselwörter: extrazelluläre Signalübertragung, fluoreszente Biosensoren, Glutamat‑Bildgebung, Kaliumdynamik, hippocampale Neuronen