Clear Sky Science · de
Schnelle Beseitigung von Bakterien aus dem mütterlichen Blutkreislauf nach der Geburt bei Schwangerschaften mit vorzeitigem vor der Wehen einsetzenden Blasensprung
Warum diese Forschung für Mütter und Babys wichtig ist
Komplikationen in der Schwangerschaft, die zu sehr frühen Geburten führen, zählen zu den bedrohlichsten Situationen für Familien und Ärztinnen und Ärzte. Eine solche Erkrankung, der vorzeitige vor den Wehen einsetzende Blasensprung (PPROM), tritt auf, wenn die Fruchtblase Wochen vor dem errechneten Termin reißt. Das erhöht das Risiko gefährlicher Infektionen für Mutter und Kind. Die in diesem Beitrag zusammengefasste Studie stellt eine einfache, aber wichtige Frage: Wenn Keime bei PPROM die Fruchtblase erreichen, gelangen sie um die Geburt herum in den mütterlichen Blutkreislauf, und wenn ja, wie schnell kann der Körper sie wieder beseitigen?
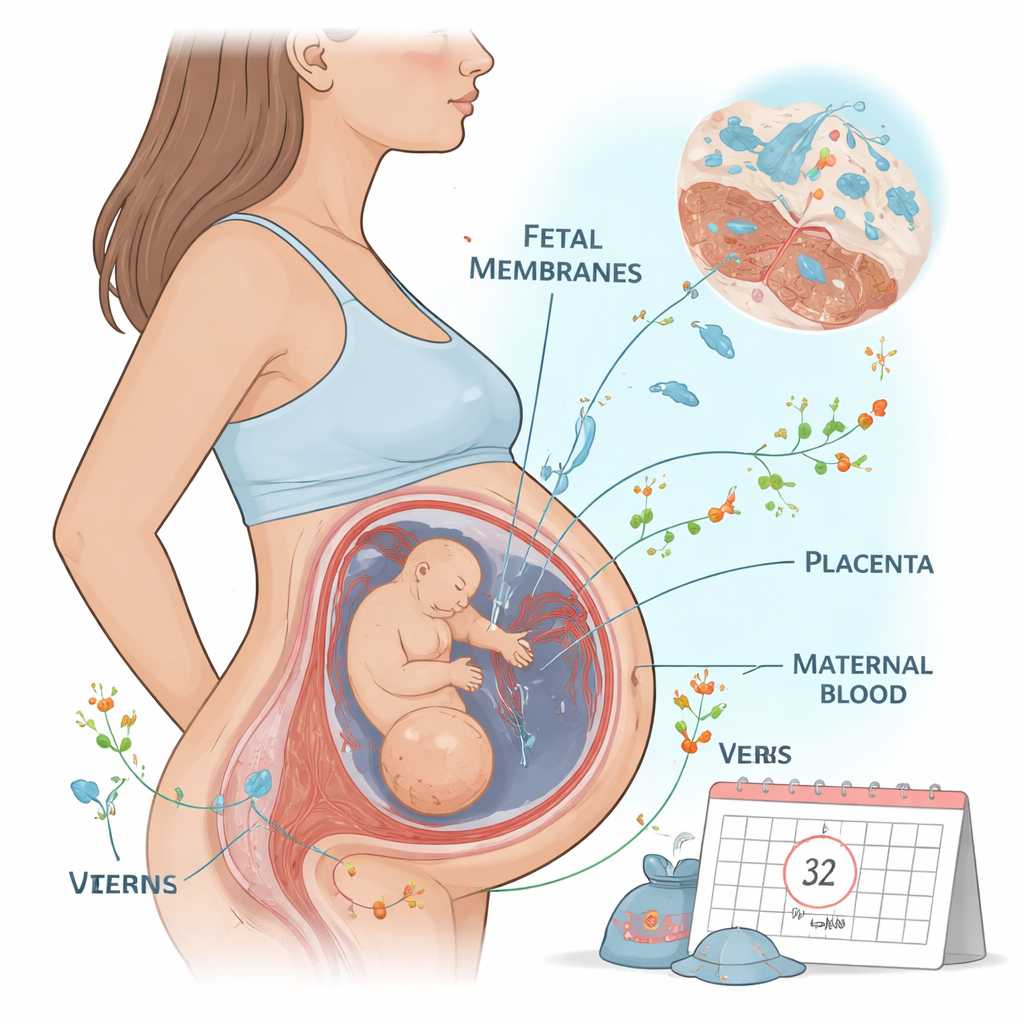
Ein genauerer Blick auf das vorzeitige Blasenspringen
Bei einer normalen Schwangerschaft sind die Flüssigkeit um das Kind und die dünnen fetalen Membranen, die sie enthalten, üblicherweise frei von Mikroben. Reißen die Membranen jedoch zu früh, können vaginale Bakterien aufsteigen und die Fruchtblase sowie die Plazenta infizieren. Ärztinnen und Ärzte fürchten eine Sepsis, eine lebensbedrohliche systemische Reaktion auf eine Infektion, müssen aber häufig die Risiken einer Infektion gegen die Schäden einer extrem frühzeitigen Entbindung abwägen. Die Forschenden rekrutierten 66 Frauen mit PPROM, die meisten bei etwa 32 Schwangerschaftswochen, um bakterielle Belastung und Entzündungszeichen im mütterlichen Blut und in den das Kind stützenden Geweben bei der Entbindung zu verfolgen.
Bakterien vom Mutterleib in den Blutkreislauf verfolgen
Das Team entnahm mütterliches Blut unmittelbar vor der Geburt und erneut innerhalb einer Stunde nach der Entbindung. In einer Untergruppe wurden außerdem fetale Membranen und Plazentagewebe untersucht. Statt sich auf Standardkulturen zu verlassen, die viele Mikroben übersehen, nutzten sie empfindliche DNA-basierte Methoden, die selbst winzige Spuren bakteriellen Erbguts nachweisen können. Gleichzeitig bestimmten sie Signalproteine im mütterlichen Blut—Zytokine wie Interleukin-6 (IL-6) und Interleukin-10 (IL-10)—und verwendeten Nabelschnurbluttests sowie plazentare Befunde, um zu beurteilen, ob jedes Baby im Mutterleib einer ausgeprägten Entzündungsreaktion ausgesetzt gewesen war, einem Zustand, den sie als „Triple I“ bezeichnen.
Verborgene Keime und eine rasche Reinigung
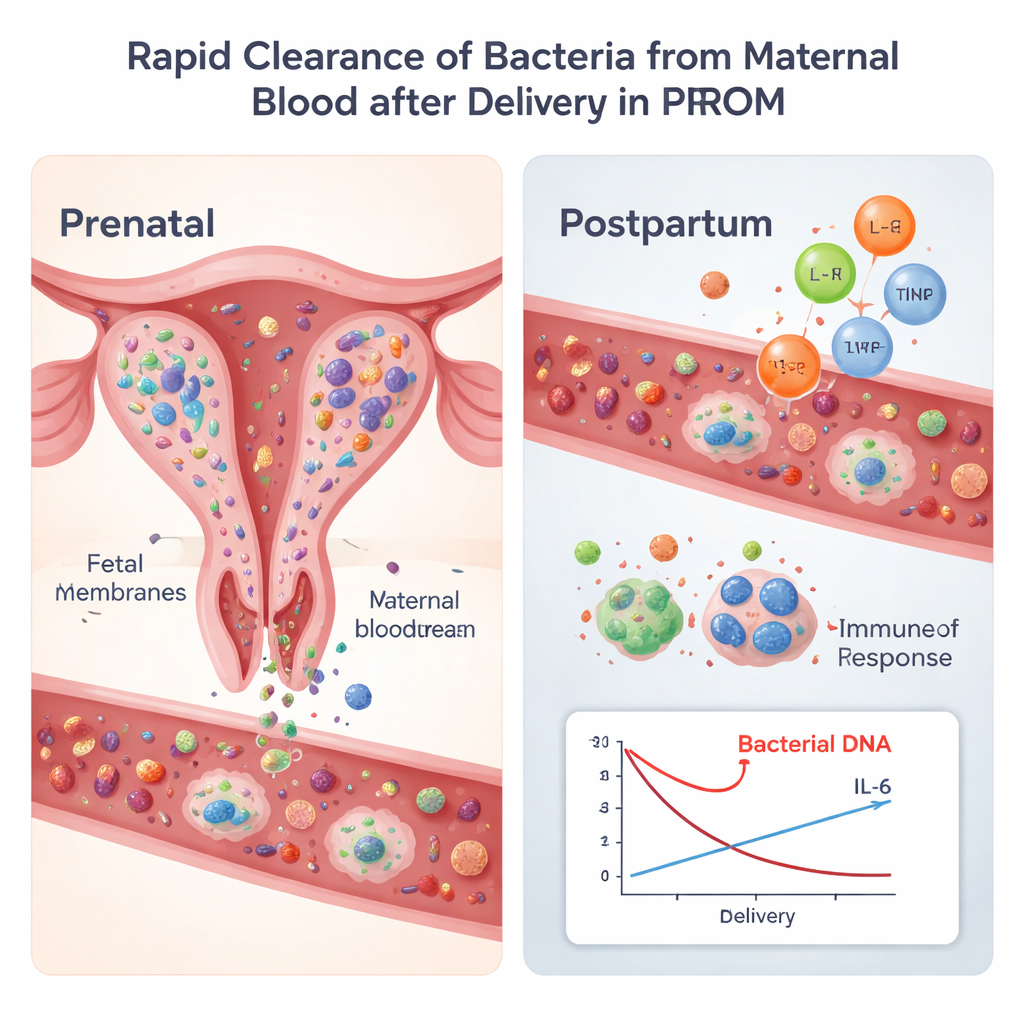
Bakterielle DNA war in mütterlichem Blut überraschend häufig: Sie wurde in über 80 % der Proben sowohl vor als auch nach der Geburt nachgewiesen. Verglich man die bakteriellen Mengen jedoch sorgfältig mit einem stabilen humanen Referenzgen, sank die Gesamtmenge bakterieller DNA im Blut nach der Geburt bei etwa zwei Dritteln der Frauen signifikant. Gleichzeitig stiegen die Konzentrationen von IL-6 und IL-10 im mütterlichen Blut deutlich an, insbesondere bei Schwangerschaften, in denen das Kind klare Anzeichen einer entzündlichen Exposition zeigte. In diesen höher-riskanten Schwangerschaften korrelierte ein größerer Anstieg von IL-6 nach der Geburt mit einem stärkeren Rückgang bakterieller DNA, was darauf hindeutet, dass die mütterliche Immunantwort aktiv dazu beitrug, bakterielle Fragmente aus der Zirkulation zu entfernen.
Wo die Bakterien wirklich sitzen
Beim Vergleich bakterieller DNA im Blut mit der in fetalen Membranen und Plazentagewebe zeigte sich, dass die Membranen deutlich mehr Bakterien und eine reichere Artenvielfalt aufwiesen als Plazenta oder Blut. Die Membranen waren dominiert von Mycoplasmen und anderen Organismen, die häufig mit Infektionen des Genitaltrakts in Verbindung gebracht werden. Dieselben Bakterien fehlten jedoch größtenteils im mütterlichen Blut, wo nur eine begrenzte Anzahl bakterieller Familien—oft mit Darm- oder Mundkeimen verwandte Gruppen wie Escherichia-Shigella und Pseudomonas—nachgewiesen wurde. Es gab nur sehr geringe Überschneidungen zwischen den im Blut nachgewiesenen Bakterien und denen in den reproduktiven Geweben, was gegen die Vorstellung spricht, dass die Entbindung routinemäßig Bakterien aus den Membranen in die mütterliche Zirkulation „spült“.
Was das für Patientinnen und Versorgung bedeutet
Für Familien und klinische Teams, die mit PPROM konfrontiert sind, liefert diese Studie eine gewisse Beruhigung. Sie zeigt, dass zwar vor der Geburt häufig Spuren bakterieller DNA im mütterlichen Blut vorhanden sind, der Körper diese Last jedoch in der Regel schnell nach der Entbindung reduziert, einhergehend mit einem Anstieg schützender Immunbotenstoffe. Die fetalen Membranen können eine beträchtliche Gemeinschaft von Mikroben beherbergen, doch diese Organismen scheinen nur selten in großen Mengen in den mütterlichen Blutkreislauf zu gelangen. Vielmehr scheint das mütterliche Immunsystem eine dynamische, effektive Reinigung durchzuführen. Zu verstehen, wie genau dieser Schutz funktioniert, könnte Ärztinnen und Ärzten helfen, die wenigen Patientinnen zu erkennen, bei denen die Abwehr versagt—und letztlich die Ergebnisse für Mütter und ihre frühgeborenen Kinder zu verbessern.
Zitation: Buhimschi, C.S., Zhao, G., Rood, K.M. et al. Rapid clearance of bacteria from maternal bloodstream after delivery in pregnancies complicated by preterm pre-labor rupture of the membranes. Sci Rep 16, 6725 (2026). https://doi.org/10.1038/s41598-026-37231-5
Schlüsselwörter: Frühgeburt, PPROM, mütterliche Infektion, Blut-Mikrobiom, fetale Membranen