Clear Sky Science · de
MRT-basierte Neurobildgebung zur Stadieneinteilung der Alzheimer-Krankheit mithilfe eines tiefen neuronalen Netzes mit Convolutional Block Attention Module und GAN-ähnlicher Rauschinjektion
Warum frühe Hirnuntersuchungen wichtig sind
Die Alzheimer-Krankheit raubt langsam Gedächtnis und Selbstständigkeit, oft lange bevor Symptome deutlich werden. Angehörige, Ärztinnen und Ärzte sowie Betroffene wünschen sich ein Verfahren, das die Erkrankung früh erkennt, wenn Behandlungen und Lebensstiländerungen am meisten bewirken können. Diese Studie beschreibt ein neues Computersystem, das routinemäßige Hirnscans analysiert und Menschen mit bemerkenswerter Genauigkeit in vier Stadien Alzheimer-assoziierten Gedächtnisverlusts einordnet – womöglich als schnellere, günstigere und konsistentere zweite Meinung für Kliniker.
Ein genauerer Blick ins Gehirn
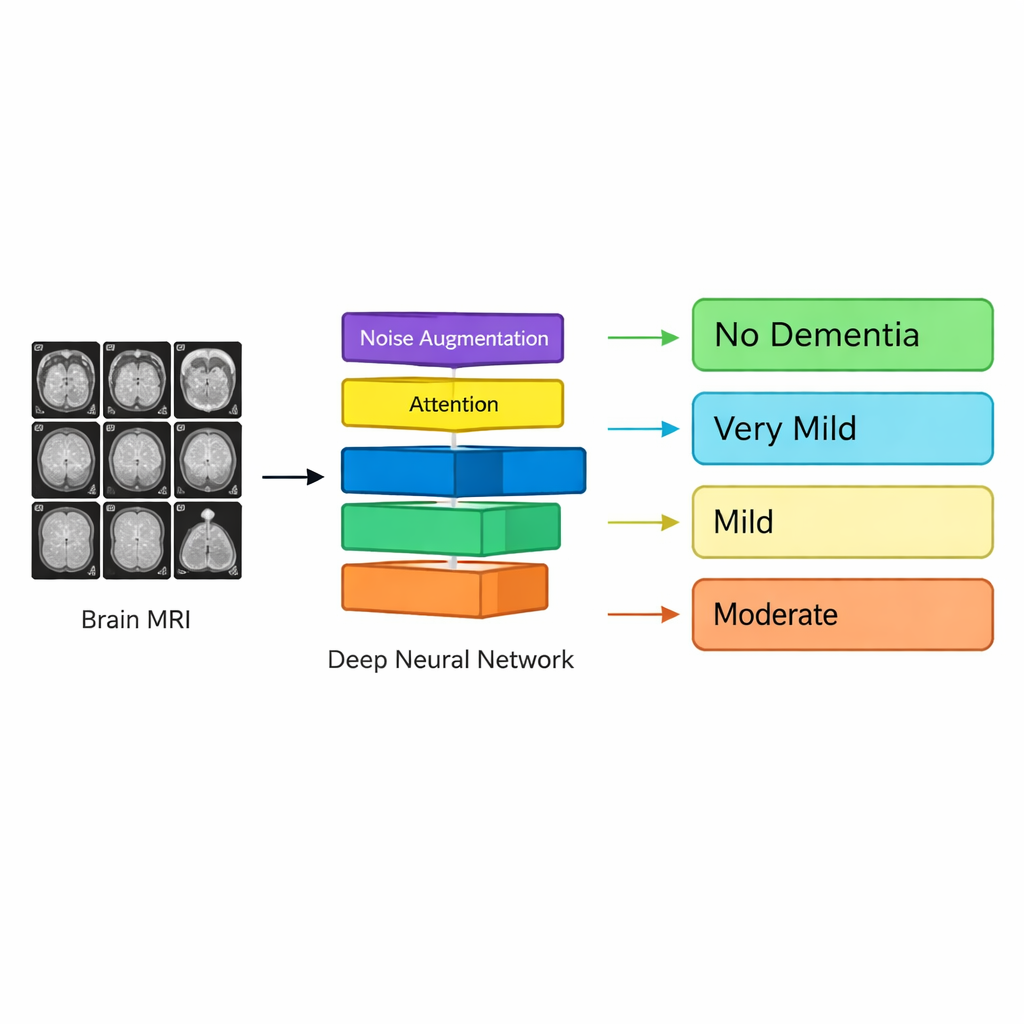
Die Forschenden konzentrieren sich auf MRT-Aufnahmen, die detaillierte Bilder der Gehirnstruktur ohne Operation oder Strahlung liefern. Sie nutzen Daten aus einem großen internationalen Projekt namens Alzheimer’s Disease Neuroimaging Initiative (ADNI), in dem Freiwillige im Alter von 55 bis 90 Jahren regelmäßig Gedächtnistests und Bildgebung unterziehen. Aus diesen Scans extrahiert das Team 2D-Schnitte des Gehirns und sortiert sie in vier Gruppen: Personen ohne Demenz sowie solche mit sehr leichter, leichter oder mäßiger Demenz. Das reflektiert den typischen Verlauf der Alzheimer-Erkrankung in der Praxis, bei dem sich kleine Veränderungen von Gedächtnis und Denken allmählich verschlechtern.
Dem Computer beibringen, subtile Veränderungen zu sehen
Anstatt menschliche Expertinnen und Experten Regionen und Merkmale von Hand auswählen zu lassen, trainieren die Autorinnen und Autoren ein Deep-Learning-System – in seiner Ausrichtung ähnlich zu denen, die für Gesichtserkennung oder autonomes Fahren verwendet werden – sodass es direkt aus den Bildern lernt. Ihr Modell, Neuro_CBAM-ADNet genannt, ist eine Art Convolutional Neural Network, das besonders gut darin ist, Muster in Bildern zu erkennen. Wenn das MRT-Bild durch das Netzwerk läuft, wird es von gestapelten Schichten verarbeitet, die Kanten, Texturen und komplexere Formen erkennen, bis das System Muster unterscheiden kann, die mit verschiedenen Demenzstadien korrelieren – viele davon zu subtil, um sie mit bloßem Auge zu sehen.
Dem Computer helfen, sich auf Relevantes zu konzentrieren
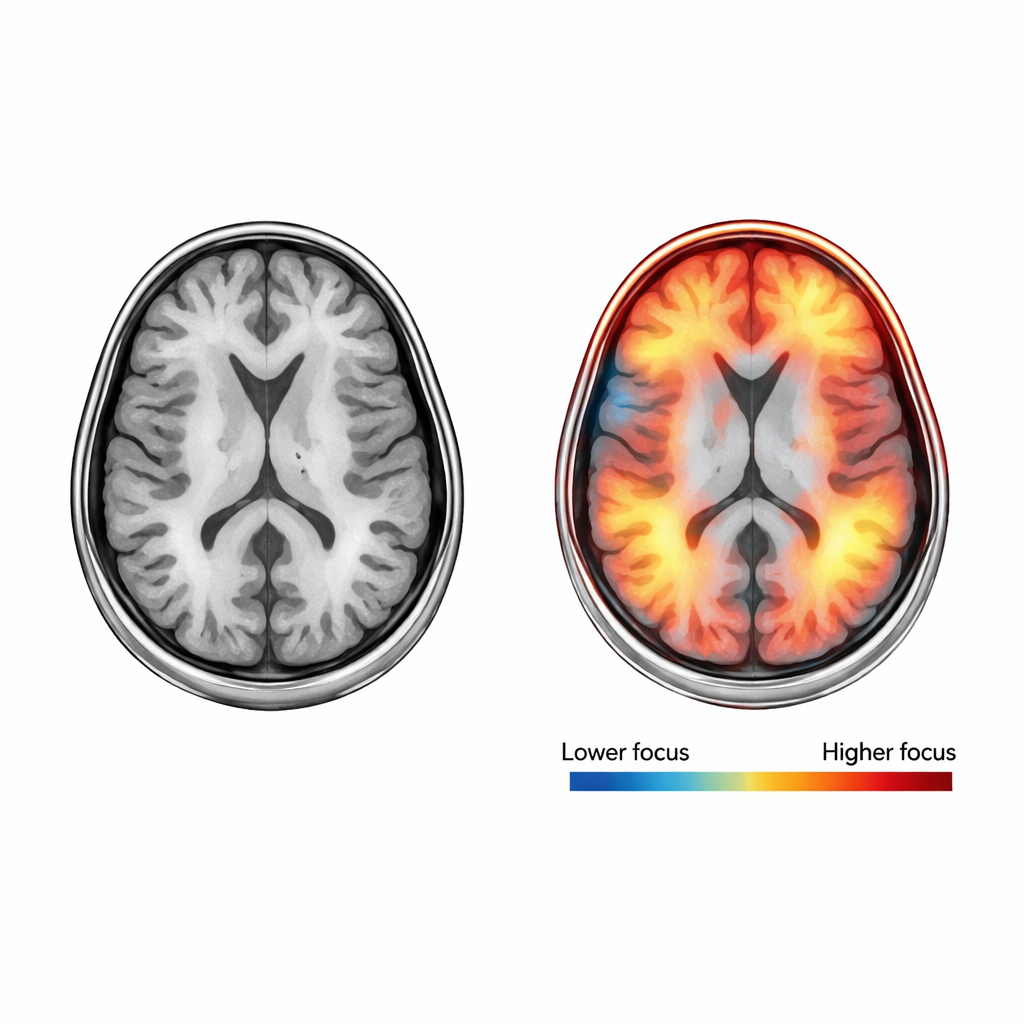
Eine zentrale Neuerung ist ein «Attention»-Mechanismus, der das Netzwerk gezielt dazu bringt, sich auf die informativsten Bereiche des Scans zu konzentrieren. Praktisch lernt das Modell, welche Positionen und internen Merkmale des Gehirns mit dem Fortschreiten der Alzheimer-Krankheit gewöhnlich verändert sind – etwa Areale, die mit Gedächtnis und kognitiven Fähigkeiten zu tun haben – und gleichzeitig weniger relevante Hintergründe zu ignorieren. Die Forschenden gehen auch ein häufiges Problem medizinischer Daten an: Manche Krankheitsstadien sind deutlich seltener als andere, sodass das Modell sonst zugunsten der Majoritätsklasse voreingenommen sein könnte. Um dem entgegenzuwirken, erzeugen sie zusätzliche Trainingsbilder für unterrepräsentierte Gruppen, indem sie kontrolliert Rauschen zu bestehenden Scans hinzufügen, wodurch die natürliche Variabilität realer Patientinnen und Patienten nachgeahmt wird, ohne die zugrunde liegende Anatomie zu verfälschen.
Das System auf die Probe stellen
Um die Zuverlässigkeit ihres Systems zu überprüfen, trainiert und testet das Team es wiederholt auf unterschiedlichen Teilmengen der Daten, ein Verfahren, das Kreuzvalidierung genannt wird. Über fünf unabhängige Durchläufe klassifiziert Neuro_CBAM-ADNet das Demenzstadium in etwa 98 Prozent der Fälle korrekt, mit ähnlich hohen Werten für Sensitivität (Betroffene erkennen), Präzision (Fehlalarme vermeiden) und einer kombinierten Kennzahl, dem F1-Score. Das System ist besonders stark darin, deutlich verschiedene Gruppen auseinanderzuhalten, etwa mäßige Demenz versus keine Demenz; die meisten Fehler treten zwischen benachbarten Stadien wie keine Demenz und sehr leichter Demenz auf, wo selbst Spezialisten oft uneins sind. Zusätzliche Werkzeuge wie Grad-CAM-Heatmaps zeigen, wo im Gehirn das Modell «hinguckt», wenn es eine Entscheidung trifft, und liefern damit visuelle Hinweise, die mit bekannten Krankheitsmarkern abgeglichen werden können.
Was das für Patientinnen, Patienten und Ärztinnen und Ärzte bedeutet
Einfach gesagt zeigt diese Arbeit, dass ein gut gestaltetes KI-System Hirnscans lesen und Menschen in vier Stadien Alzheimer-assoziierten Abbaus einordnen kann – mit einer Konsistenz, die frühere Ansätze erreicht oder in manchen Fällen übertrifft. Gleichzeitig macht es die Hirnregionen transparent, die seine Entscheidungen antreiben, was das Vertrauen von Klinikerinnen und Klinikern stärken kann. Obwohl das Werkzeug noch breitere Tests an verschiedenen Krankenhäusern und mit unterschiedlichen Scannern braucht, deutet es auf eine Zukunft hin, in der routinemäßige MRT-Untersuchungen in Kombination mit transparenter KI frühe Hirnveränderungen aufspüren, sicherere Diagnosen unterstützen und Behandlungsentscheidungen leiten könnten, bevor die Krankheit zu weit fortgeschritten ist.
Zitation: Kumar, S., Shastri, S., Mansotra, V. et al. MRI neuroimaging-based Alzheimer’s disease stage classification using deep neural network with convolutional block attention module and GAN-style noise injection. Sci Rep 16, 6946 (2026). https://doi.org/10.1038/s41598-026-37226-2
Schlüsselwörter: Alzheimer-Krankheit, Gehirn-MRT, Deep Learning, frühe Diagnose, KI in der medizinischen Bildgebung