Clear Sky Science · de
Dynamische Graphkonvolution mit umfassendem Pruning und GNN-Klassifikation zur präzisen Erkennung von Lymphknotenmetastasen
Warum winzige Veränderungen in Lymphknoten wichtig sind
Wenn Brustkrebs streut, sind die Lymphknoten entlang des Drainagesystems des Körpers oft die erste Station. Zu erkennen, ob Krebszellen diese Knoten erreicht haben, ist einer der wichtigsten Hinweise, die Ärztinnen und Ärzte bei der Wahl von Operation, Chemotherapie und Bestrahlung heranziehen. Dennoch können selbst erfahrene Pathologinnen und Pathologen sehr kleine Zellverbände auf digitalen Mikroskopaufnahmen übersehen, besonders wenn sie gesundem Gewebe stark ähneln. Diese Studie stellt einen neuen KI‑Rahmen vor, der Gewebe als Netzwerk verbundener Regionen behandelt und so subtile Hinweise auf Streuung mit bemerkenswerter Genauigkeit findet.
Gewebeabbildungen in Netzwerke überführen
Die Forschenden arbeiten mit riesigen digitalen Schnitten gefärbter Gewebsproben, sogenannten Whole‑Slide‑Images, aus Lymphknotenbiopsien bei Brustkrebs. Diese Bilder enthalten Millionen von Pixeln und eine verwirrende Vielfalt an Zelltypen, Farben und Texturen. Um diese Komplexität zu bändigen, bereinigt das Team die Bilder zuerst: Sie normalisieren Helligkeit und Farbe, reduzieren Rauschen und erzeugen augmentierte Kopien durch Rotation und Spiegelung von Patches, damit der Rechner mit natürlicher Variabilität zurechtkommt. Jeder Bildpatch wird dann in kleine, relativ einheitliche Regionen („Superpixel“) zerlegt, die zu Punkten — bzw. Knoten — in einem Graphen werden, während die Beziehungen zwischen benachbarten Regionen die verbindenden Linien — also Kanten — bilden. Diese Netzwerk‑Sicht bewahrt die unregelmäßigen Formen und Anordnungen echten Gewebes besser als herkömmliche rasterbasierte Bildmethoden.
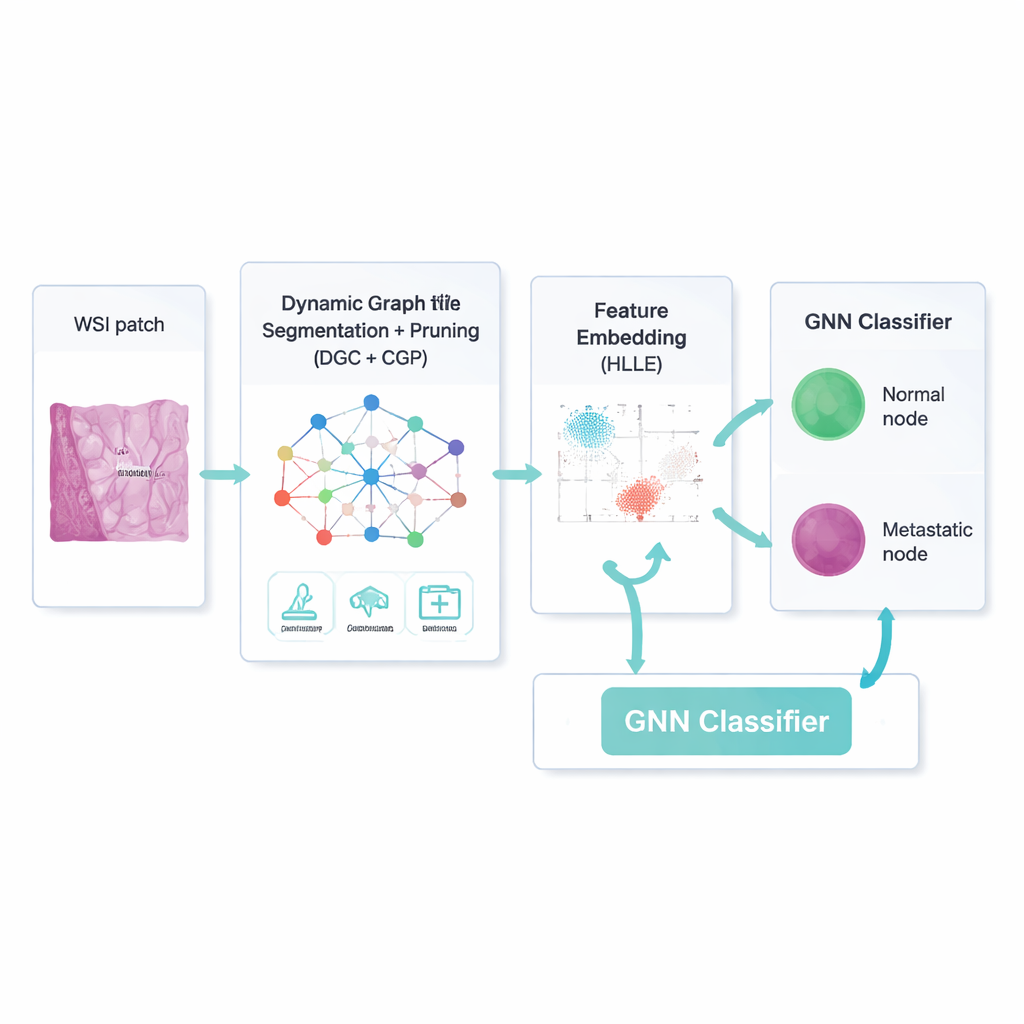
Ein klügerer Weg, sich auf das Wesentliche zu konzentrieren
Allein ein Netzwerk zu bauen reicht nicht; viele Verbindungen und Bildmerkmale sind irrelevant oder sogar irreführend. Der Rahmen verwendet daher einen dynamischen graphkonvolutionalen Autoencoder — eine Art neuronales Netz, das sowohl lernt, wie jede Region aussieht, als auch wie Regionen einander beeinflussen. Ein zusätzliches „Attention“-Mechanismus bringt dem Modell bei, manche Bildkanäle stärker zu gewichten als andere, etwa um Kanten an einer Tumorgrenze hervorzuheben. Parallel dazu entfernt eine Strategie namens Comprehensive Graph Gradual Pruning schrittweise unbrauchbare Teile: schwache Verbindungen zwischen Regionen, weniger nützliche numerische Merkmale und Modellgewichte mit geringem Einfluss. Dieses Pruning findet während des Trainings statt, nicht danach, sodass das System lernt, mit weniger mehr zu leisten und am Ende sowohl schneller als auch leichter interpretierbar ist.
Muster komprimieren, ohne ihre Gestalt zu verlieren
Nachdem das Modell wahrscheinliche Lymphknotenregionen vom Hintergrundgewebe getrennt hat, muss es jede Region noch so beschreiben, dass die Darstellung kompakt, aber aussagekräftig ist. Dazu nutzen die Autorinnen und Autoren eine Technik namens Hessian‑basierte Locally Linear Embedding. Einfach ausgedrückt komprimiert sie viele numerische Merkmale in eine kleinere Menge, dabei versucht sie die gekrümmte „Gestalt“ der Anordnung echter Beispiele im Merkmalsraum zu bewahren — etwa wie sich winzige Metastasen entlang subtiler Textur‑ oder Farbverläufe von normalen Immunzellen unterscheiden. Diese komprimierten Beschreibungen werden Eingabe für einen graphbasierten neuronalen Klassifikator, der erneut auf dem Netzwerk der Regionen und dessen bereinigten Verbindungen arbeitet und für jeden Knoten entscheidet, ob er metastatisch ist oder nicht.
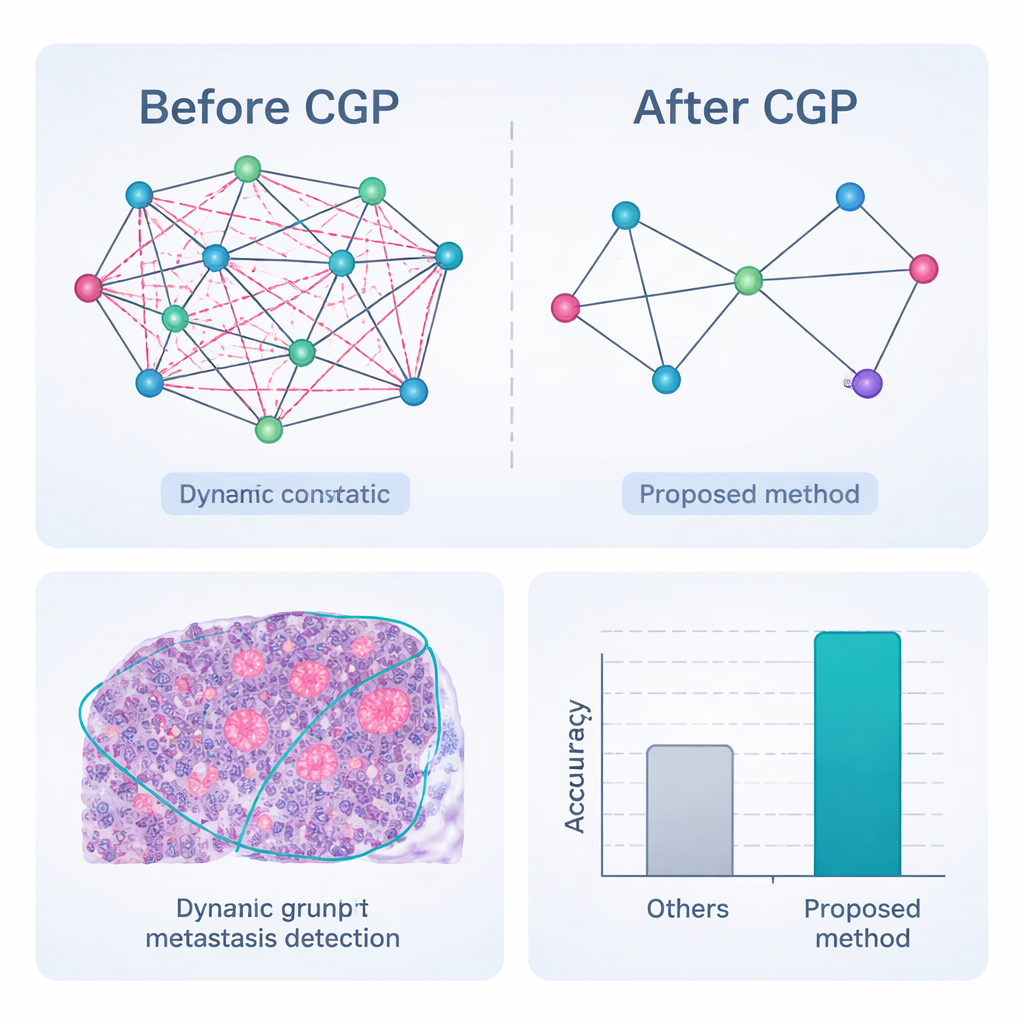
Den Rahmen auf die Probe stellen
Die vollständige Pipeline — Vorverarbeitung, dynamische Graphsegmentierung mit Pruning, Merkmals‑Embedding und graphbasierte Klassifikation — wurde an CAMELYON17 evaluiert, einer öffentlichen Sammlung von 1.000 fachmännisch annotierten Lymphknotenschnitten von Brustkrebspatientinnen und -patienten. Im Vergleich zu einer Reihe starker Deep‑Learning‑Konkurrenten, darunter verbreitete Faltungsnetze und hybride Transformermodelle, erzielte die neue Methode in fast allen Messgrößen die besten Werte. Sie klassifizierte Knoten in 98,65 % der Fälle korrekt als krebsbefallen oder nicht und zeigte eine bessere Übereinstimmung mit Expertenumrissen von Tumorregionen, besonders bei sehr kleinen oder schwachen Metastasen. Entscheidend ist, dass das aggressiv geprunte Graphmodell diese Ergebnisse mit deutlich weniger Rechenaufwand und geringerem Speicherverbrauch erreicht, weshalb es sich besser für Echtzeitanwendungen in vielbeschäftigten Pathologielabors eignet.
Was das für Patientinnen, Patienten und Kliniker bedeutet
Praktisch zeigt diese Arbeit, wie die Betrachtung von Gewebe als clever geschnittenes Netzwerk verbundener Regionen Computern ermöglicht, als äußerst gründliche Zweitleser von Lymphknotenschnitten zu fungieren. Indem Aufmerksamkeit und Rechenleistung auf die informativsten Strukturen konzentriert und Rauschen verworfen werden, erkennt das System winzige Krebsherde besser, die sonst übersehen würden — und das effizient genug, um praktisch einsetzbar zu sein. Obwohl weitere klinische Validierung nötig ist, könnten solche Werkzeuge Pathologinnen und Pathologen dabei unterstützen, schnellere und konsistentere Entscheidungen darüber zu treffen, ob sich Krebs ausgebreitet hat — eine Information, die unmittelbar Therapiepläne und letztlich Patientenergebnisse beeinflusst.
Zitation: H. N., C., N., S., S., A.R. et al. Dynamic graph convolution with comprehensive pruning and GNN classification for precise lymph node metastasis detection. Sci Rep 16, 6682 (2026). https://doi.org/10.1038/s41598-026-37193-8
Schlüsselwörter: Lymphknotenmetastase, digitale Pathologie, Graphneurale Netze, medizinische Bildsegmentierung, Brustkrebs