Clear Sky Science · de
Strukturelle Charakterisierung der Metallbindung in der humanen Tyrosylprotein-Sulfotransferase 2, TPST2
Warum winzige Metallionen für die Zellkommunikation wichtig sind
In unseren Zellen justieren zahllose molekulare Maschinen still und leise, wie Gewebe wachsen, Hormone wirken und Immunzellen miteinander kommunizieren. Eine dieser Maschinen, das Enzym TPST2, hängt bestimmten Proteinen ein kleines Sulfatetikett an, während sie durch das Versandzentrum der Zelle — dem Golgi-Apparat — gehen. Diese Studie zeigt, wie einfache Metallionen wie Natrium und Mangan TPST2 effizienter arbeiten lassen, indem sie Teile seiner Struktur dezent versteifen — eine Erkenntnis, die den Mineralhaushalt der Zelle mit Krebs- und hormonellen Erkrankungen in Verbindung bringen könnte. 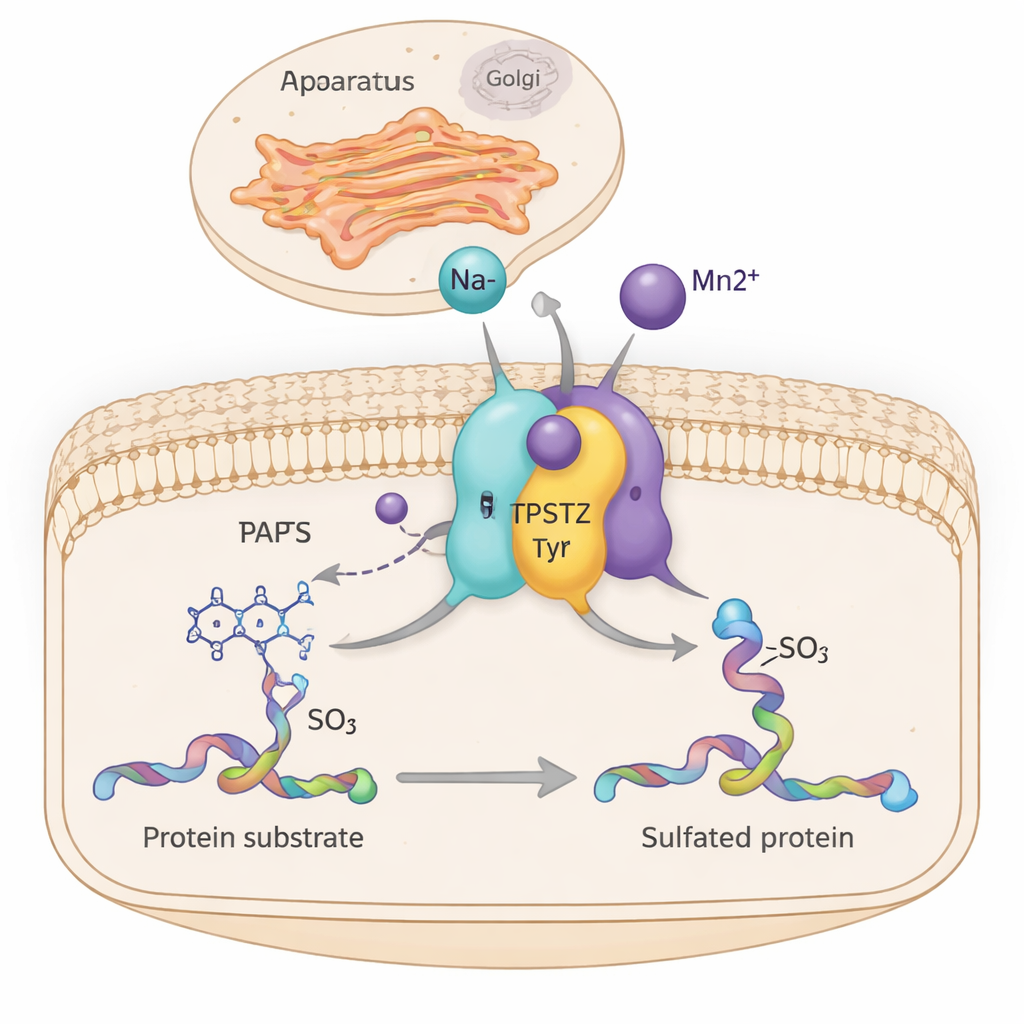
Ein Protein, das andere Proteine schmückt
TPST2 gehört zu einer Enzymfamilie, die die sogenannte „Tyrosin-Sulfatierung“ durchführt, eine chemische Modifikation, die an bestimmten Tyrosinbausteinen von Proteinen angebracht wird. Diese sulfatierten Proteine spielen wichtige Rollen außerhalb der Zellen, indem sie Blutgerinnung, Bewegung weißer Blutkörperchen, Hormon‑Rezeptor‑Bindung und sogar das Eindringen von Viren in Zellen beeinflussen. Beim Menschen gibt es zwei Hauptsulfotransferasen, TPST1 und TPST2, die in der Membran des Golgi sitzen und Proteine modifizieren, während diese für den Export vorbereitet werden. Untersuchungen an Mäusen zeigen, dass der Verlust von TPST2 die Produktion von Schilddrüsenhormonen stört, das Wachstum hemmt und männliche Unfruchtbarkeit verursacht — ein Hinweis auf seine Bedeutung für die normale Physiologie.
Verknüpfungen zu Krebs und Immunevasion
Jüngste Forschung bringt TPST2 direkt mit Krankheiten in Verbindung. Beim Melanom modifiziert TPST2 eine Komponente des Interferonrezeptors so, dass die Immunantwort abgeschwächt wird, und die Blockade von TPST2 verstärkt die Wirksamkeit von Immun-Checkpoint-Therapien gegen PD-1. Beim Pankreaskarzinom stabilisiert ein TPST2‑abhängiger Weg ein Protein (Integrin β4), das Tumorwachstum und -ausbreitung fördert. Die Hemmung von TPST2 verlangsamt in diesen Modellen die Zellteilung und Invasion von Krebszellen. Da TPST2 auf Proteine an der Zelloberfläche wirkt, verändert es effektiv, wie Zellen ihre Umgebung wahrnehmen und darauf reagieren, und ist deshalb ein attraktives Ziel für neue Therapien.
Die Metall‑„Anschalter“ finden
Biochemiker wussten schon lange, dass TPST2 deutlich aktiver wird, wenn zweiwertige Metalle wie Mangan (Mn²⁺) vorhanden sind, doch der strukturelle Grund dafür fehlte. In dieser Studie stellten die Autoren den katalytischen Kern der humanen TPST2 her und kristallisierten ihn zusammen mit einem Reaktionsnebenprodukt und entweder Natrium (Na⁺) oder Mangan. Mithilfe hochauflösender Röntgenkristallographie entdeckten sie zwei kleine Metallbindungs‑Taschen im Enzym, jeweils mit einer ordentlichen, sechsfachen (oktaedrischen) Anordnung der umliegenden Atome. Durch Abstimmung der Röntgenwellenlänge auf die charakteristischen Signaturen verschiedener Metalle bestätigten sie, dass Mn²⁺ diese Stellen selektiv besetzt, während Metalle wie Zink und Kupfer entweder schwach an anderen Orten binden oder gar nicht.
Wichtig bewegliche Teile versteifen statt das Ganze umzubauen
Überraschenderweise sahen TPST2 mit Natrium und TPST2 mit Mangan insgesamt fast identisch aus; es gab kein dramatisches Öffnen oder Schließen des Proteins. Stattdessen beeinflussten die Metalle hauptsächlich zwei flexible Regionen in der Nähe des Eingangs zur aktiven Stelle: eine Helix namens α3 und eine benachbarte Schleife, bekannt als die α12–α13‑Schleife. In metallfreien oder locker gebundenen Zuständen wackeln diese Segmente und sind teilweise ungeordnet. Wenn Na⁺ bindet, werden sie geordneter; Mn²⁺ strafft sie noch stärker, wie durch verringerte thermische Bewegungen in den Röntgendaten und durch computerbasierte Flexibilitätsanalysen gezeigt. Diese zusätzliche Steifigkeit erhöht mäßig die Schmelztemperatur des Enzyms und senkt vermutlich die „entropischen“ Kosten, die mit der Organisation der aktiven Stelle verbunden sind — wodurch es für TPST2 leichter und schneller wird, Substrate in die richtige Position für die Sulfatierung zu führen. 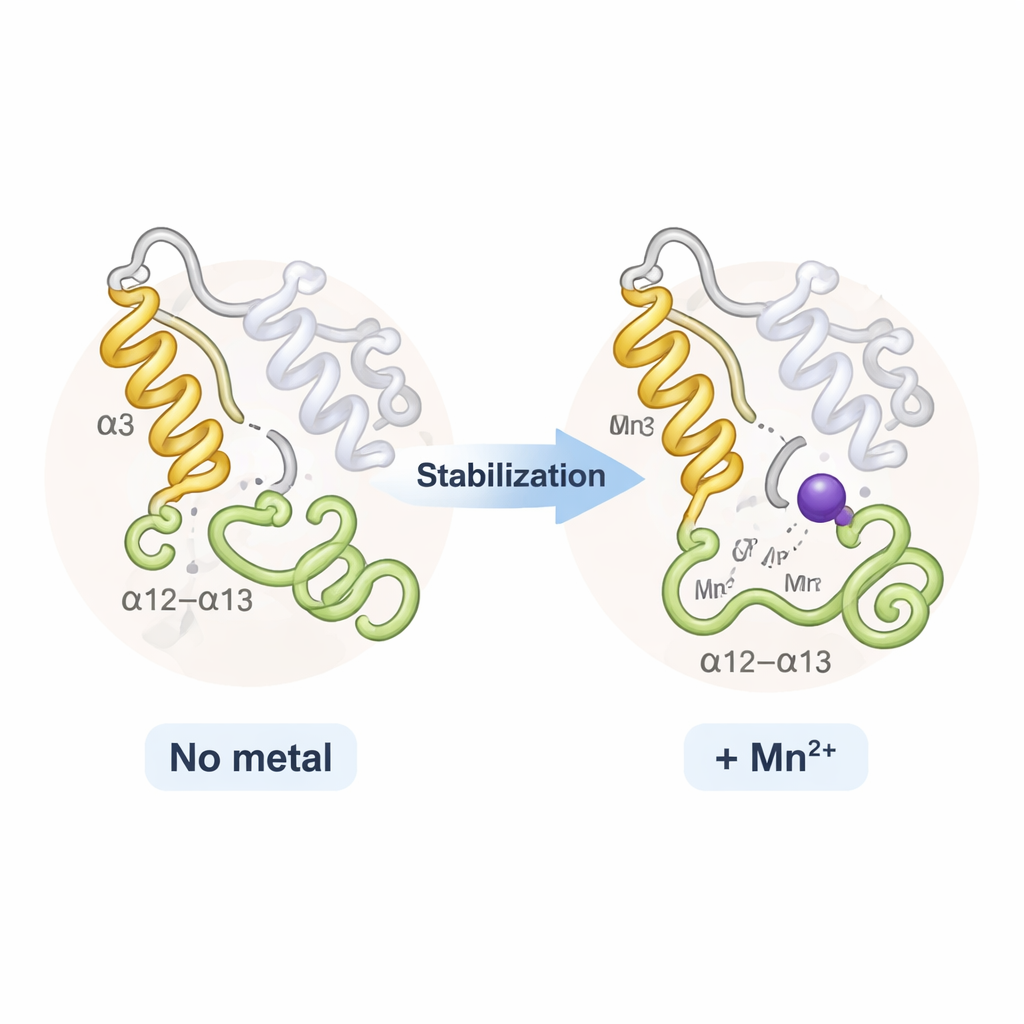
Von zellulären Mineralien zur Signalsteuerung
Die Autoren schlagen ein „Aktivierung‑durch‑Ordnen“-Modell vor. Ohne gebundenes Metall ist TPST2 um den Eingang der aktiven Stelle herum schlaff und arbeitet ineffizient. Natrium, das in Zellen reichlich vorhanden ist, kann dieselben Stellen besetzen und einen teilweise geordneten, mäßig aktiven Zustand erzeugen. Mangan, das im Golgi in sorgfältig kontrollierten Mikromolar‑Konzentrationen vorkommt, bindet stärker und verriegelt die Schlüsselregionen in einem optimal angeordneten Zustand, wodurch die katalytische Effizienz maximiert wird. Das deutet darauf hin, dass subtile Verschiebungen des Golgi‑Mangan‑Spiegels beeinflussen könnten, wie stark TPST2 seine Zielmoleküle modifiziert. Da TPST2 die Hormonproduktion und krebsrelevante Signalwege beeinflusst, hebt die Arbeit einen möglichen Zusammenhang zwischen Metallionen‑Gleichgewicht, Protein‑„Schmuck“ und Krankheit hervor — und liefert einen strukturellen Rahmen für die Entwicklung von Wirkstoffen, die TPST2‑Aktivität durch Nachahmen oder Stören der Metallbindung modulieren.
Zitation: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Schlüsselwörter: Tyrosin-Sulfatierung, TPST2, Mangan, Golgi-Apparat, Proteinmodifikation