Clear Sky Science · de
Interpretierbares hybrides Ensemble mit auf Aufmerksamkeit basierender Fusion und EAOO-GA-Optimierung zur Lungenkrebsdetektion
Warum die frühe Erkennung von Lungenkrebs uns alle angeht
Lungenkrebs gehört zu den tödlichsten Krebsarten, weil er häufig erst zu spät entdeckt wird, wenn Behandlungsmöglichkeiten begrenzt sind und die Überlebenschancen stark sinken. Ärztinnen und Ärzte verlassen sich zunehmend auf CT-Scans und Computerprogramme, um verdächtige Herdbildungen in der Lunge zu erkennen, bevor Symptome auftreten. Diese Studie stellt ein neues System der künstlichen Intelligenz (KI) vor, das nicht nur die diagnostische Genauigkeit verbessern, sondern auch die Zuverlässigkeit erhöhen und die Ergebnisse für Kliniker leichter nachvollziehbar machen soll.
Wie Computer Lungenaufnahmen lesen
Moderne KI-Systeme können CT-Bilder analysieren und Muster lernen, die harmlose Flecken von gefährlichen Tumoren unterscheiden. Diese Systeme, basierend auf tiefen neuronalen Netzen, haben bereits gezeigt, dass sie in engen Aufgaben mit menschlichen Expertinnen und Experten konkurrieren oder diese übertreffen können. In echten Kliniken stoßen sie jedoch auf drei wesentliche Probleme: Sie können auf einen Datensatz überanpassen und bei neuen Patientinnen und Patienten versagen, sie haben Schwierigkeiten mit unausgeglichenen Daten, bei denen einige Krankheitsformen selten sind, und sie arbeiten oft als undurchsichtige „Black Boxes“, denen Kliniker nur schwer vertrauen. Die Autoren richten ihren Fokus auf diese Herausforderungen bei einem weit verbreiteten Lungen-CT-Datensatz, der drei Falltypen umfasst: benigne Knoten, maligne Knoten und normale Scans.
Viele Expertinnen und Experten statt einer
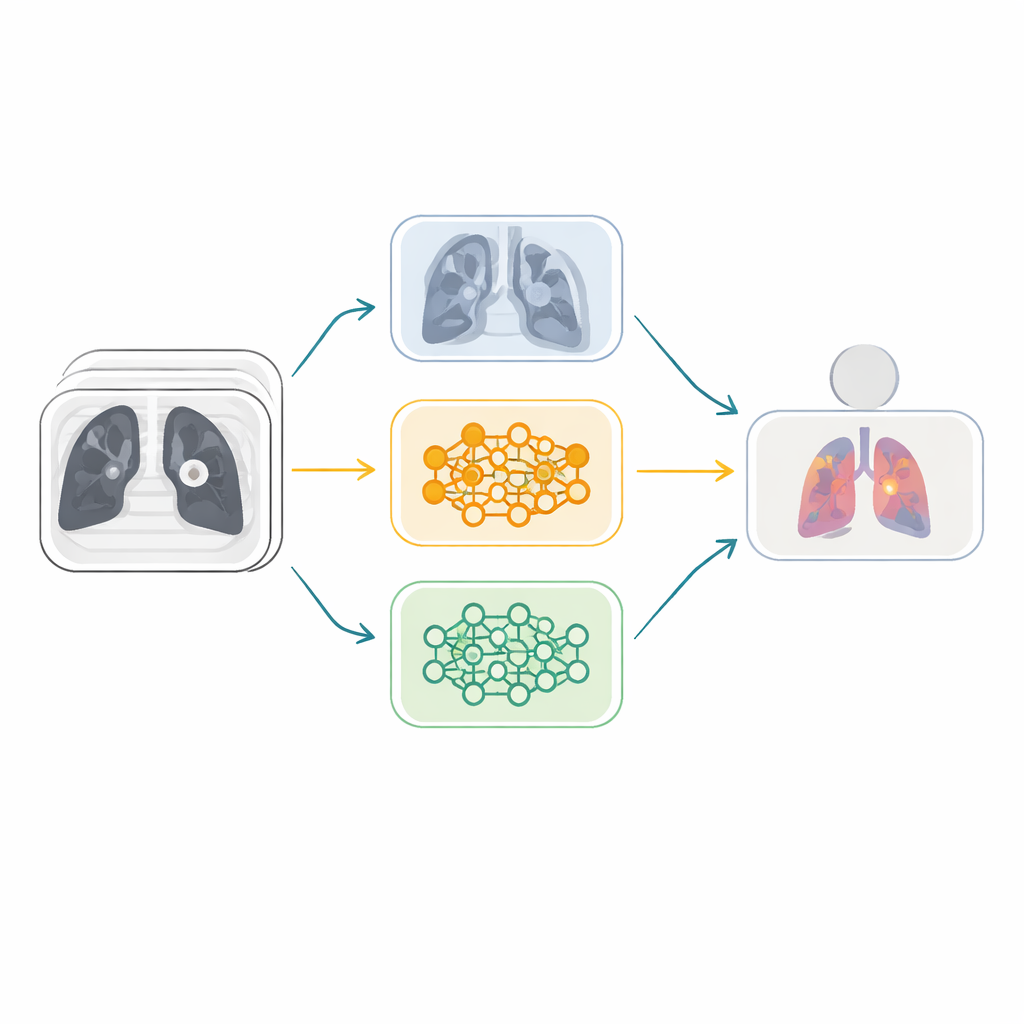
Anstatt sich auf ein einzelnes neuronales Netz zu verlassen, bauen die Forschenden ein Ensemble — ein Team verschiedener KI-Modelle, das gemeinsam abstimmt. Sie beginnen mit sechs leistungsfähigen Bild-Erkennungsarchitekturen, die ursprünglich an Millionen Alltagsfotos trainiert wurden, und passen diese an Lungen-CTs an. Diese Modelle werden dann zu drei „Fusions“-Zweigen gepaart, wobei jeweils zwei Netzwerke mit komplementären Stärken kombiniert werden. Innerhalb jedes Zweigs lernt ein spezieller Aufmerksamkeitsmechanismus, bekannt als Squeeze-and-Excitation, welche internen Merkmalskanäle die nützlichsten visuellen Hinweise tragen — etwa subtile Texturen oder Knotenformen — und verstärkt diese, während weniger informative Muster abgeschwächt werden. Das hilft dem System, sich auf medizinisch relevante Details und nicht auf Rauschen zu konzentrieren.
Naturinspiriertes Suchen zur Feinabstimmung des Teams
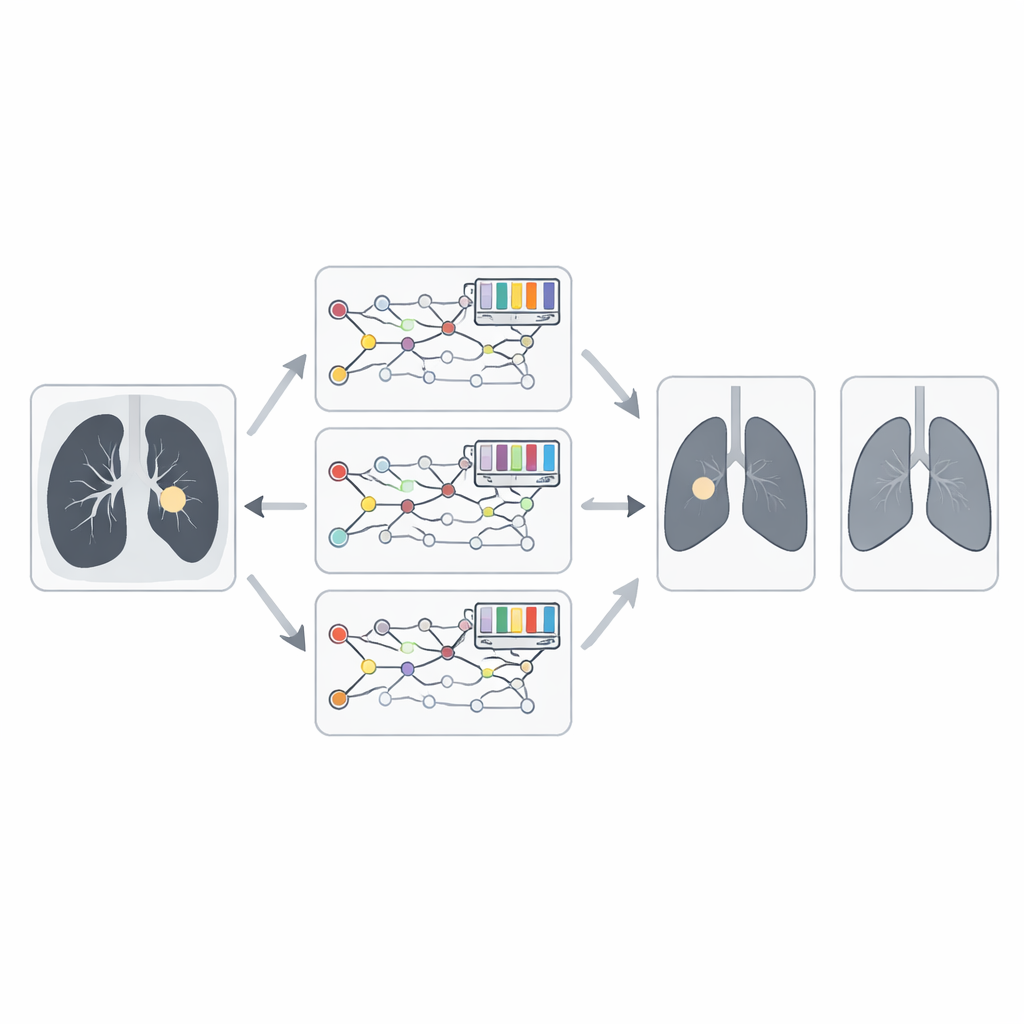
Das einfache Mittel der Durchschnittsbildung der Meinungen dreier starker Zweige lässt noch Verbesserungsmöglichkeiten offen. Die Schlüsselidee dieser Arbeit ist, einen naturinspirierten Optimierer entscheiden zu lassen, welchem Zweig wie viel Gewicht beigemessen wird. Das Team führt eine erweiterte Version des Animated Oat Optimization-Algorithmus ein, ergänzt durch genetische Operationen wie Kreuzung und Mutation. Vereinfacht behandelt dieser Algorithmus Kandidatenkombinationen von Gewichten als Population und „evolviert“ sie wiederholt, behält diejenigen bei, die zu genaueren Krebsvorhersagen führen, und mischt die übrigen neu. Über viele Iterationen findet er ein effektives Gleichgewicht, bei dem die verlässlichsten Fusionsmodelle stärker zur finalen Diagnose beitragen.
Seltene Fälle ausgleichen und die Black Box öffnen
Reale medizinische Daten enthalten oft deutlich mehr maligne als benigne oder normale Beispiele, was ein KI-System zugunsten von Überdiagnosen verzerren kann. Um dem entgegenzuwirken, nutzen die Autoren eine Technik namens SMOTE, um zusätzliche synthetische Beispiele für unterrepräsentierte Klassen zu erzeugen und so die Trainingsverteilung auszugleichen. Zudem fügen sie eine erklärende Schicht mit Grad-CAM hinzu, die Heatmaps erzeugt und die Bildregionen zeigt, die jede Entscheidung am stärksten beeinflusst haben. Bei malignen Fällen stimmen die hervorgehobenen Bereiche typischerweise mit unregelmäßigen, gestachelten Knoten überein; bei benignen oder normalen Scans verschiebt sich der Fokus auf glatteres Gewebe. Das hilft Radiologinnen und Radiologen zu überprüfen, ob das Modell die richtigen Strukturen betrachtet statt irrelevanter Artefakte.
Wie gut das System an realen Daten funktioniert
Getestet am IQ-OTH/NCCD-Lungenkrebs-Datensatz erreicht das vorgeschlagene Ensemble eine beeindruckende Genauigkeit von etwa 99,4 Prozent sowie ähnlich hohe Präzision, Recall und F1-Score. Es übertrifft konstant jedes einzelne Netzwerk, einfachere Fusionsschemata und eine Reihe anderer Optimierungsmethoden. Entscheidend validieren die Autoren das Modell außerdem an einer separaten, weit verbreiteten CT-Sammlung namens LIDC-IDRI, wo es nahezu 98 Prozent Genauigkeit beibehält. Dieser externe Test deutet darauf hin, dass das System über die ursprünglich verwendeten Bilder hinaus generalisiert — eine zentrale Voraussetzung für ein Hilfsmittel, das Kliniker in verschiedenen Krankenhäusern und mit unterschiedlichen Scannern unterstützen soll.
Was das für Patientinnen, Patienten und Behandelnde bedeutet
Für Laien ist die wichtigste Erkenntnis, dass die Kombination mehrerer KI-„Expertinnen“ und „Experten“, das sorgfältige Abstimmen ihres Zusammenspiels und eine bessere Transparenz ihrer Entscheidungsfindung die frühe Erkennung von Lungenkrebs aus CT-Scans deutlich verbessern können. Das in dieser Arbeit vorgestellte Rahmenwerk verwandelt Rohbilder in eine sehr genaue, relativ interpretierbare Zweitmeinung für Radiologinnen und Radiologen. Wenn es in klinischen Studien weiter validiert und für den Alltag in Krankenhäusern angepasst wird, könnten solche Systeme helfen, gefährliche Tumoren früher zu entdecken, unnötige Folgeuntersuchungen zu reduzieren und letztlich Überleben und Lebensqualität von Menschen mit Lungenkrebs-Risiko zu verbessern.
Zitation: Al Duhayyim, M., Aldawsari, M.A., Ismail, A. et al. Interpretable hybrid ensemble with attention-based fusion and EAOO-GA optimization for lung cancer detection. Sci Rep 16, 8159 (2026). https://doi.org/10.1038/s41598-026-37187-6
Schlüsselwörter: Lungenkrebs-Erkennung, CT-Scan-Analyse, Tiefenlern-Ensemble, medizinische Bild-KI, erklärbare Diagnostik