Clear Sky Science · de
Integrative maschinelle Lernverfahren und molekulares Docking zeigen, dass Narirutin ABCC1/ABCG2 für die Umgestaltung des immunen Mikromilieus beim kolorektalen Krebs anvisiert
Fruchtverbindung mit großen Hoffnungen gegen Krebs
Kolorektales Karzinom gehört zu den tödlichsten Krebsarten weltweit, und viele Patientinnen und Patienten sind weiterhin harten Therapien und Wirkstoffresistenzen ausgesetzt. Diese Studie untersucht Narirutin, einen natürlichen Stoff, der in Zitrusfrüchten vorkommt, und prüft, ob er helfen könnte, Darmtumoren schonender zu bekämpfen – indem er verändert, wie Krebszellen mit Medikamenten umgehen und wie Immunzellen in der Tumorumgebung agieren.
Von der Zitrusfrucht zum Krebsziel
Die Forschenden begannen mit einer einfachen Frage: Wenn Narirutin ein Medikament wäre, an welchen Stellen unserer Zellen würde es andocken? Mithilfe großer öffentlicher Krebsdatenbanken und computergestützter Vorhersagewerkzeuge durchsuchten sie Tausende von Genen aus Darmtumoren und gesundem Gewebe. Anschließend überschnitten sie diese krebsassoziierten Gene mit denen, die Narirutin voraussichtlich beeinflussen kann. Von mehr als 3.000 veränderten Genen beim Darmkrebs wurde vorhergesagt, dass Narirutin sinnvollerweise nur mit neun interagiert, wobei besonders fünf „Hub“-Gene hervorstechen, die an wichtigen Steuerpunkten innerhalb der Tumorzellen sitzen.
Wichtige Torwächter auf der Oberfläche von Krebszellen
Unter diesen Hub-Genen traten zwei besonders hervor: ABCC1 und ABCG2. Sie codieren für pumpenähnliche Proteine, die in der Zellaußenmembran sitzen und Wirkstoffe wieder aus der Zelle herausschleusen – ein Grund, warum manche Tumoren gegenüber Chemotherapien resistent werden. Die neue Analyse legt nahe, dass Narirutin an diese Pumpen binden und möglicherweise ihre Funktion beeinflussen kann. Andere Hub-Gene, darunter CA12, EPHX2 und PTGS1, sind an der Regulation von Säure-Basen-Haushalt, Lipidstoffwechsel und Entzündungs‑Signalen beteiligt. Zusammen beeinflussen diese Gene, ob ein Tumor unkontrolliert wächst, wie er auf Medikamente reagiert und wie er mit dem umliegenden Normalgewebe interagiert.
Simuliertes Andocken und reale Befunde
Um zu prüfen, ob Narirutin tatsächlich an diese Zielproteine binden könnte, nutzte das Team molekulares Docking – hochauflösende Computermodelle, die vorhersagen, wie ein kleines Molekül in ein größeres Protein passt. Diese Simulationen zeigten, dass Narirutin sich gut in Taschen der Zielproteine einfügt und stabile Kontakte bildet, was physikalisch plausibles Binden nahelegt. Beim Blick in Patientendaten stellten die Forschenden fest, dass die Hub-Gene Krebsgewebe klar von normalem Gewebe unterscheiden und mit der Überlebensdauer der Betroffenen in Verbindung stehen. So gingen höhere Spiegel von ABCC1 und PTGS1 tendenziell mit schlechteren Verläufen einher, was nahelegt, dass eine Hemmung dieser Gene – potenziell durch Verbindungen wie Narirutin – vorteilhaft sein könnte.
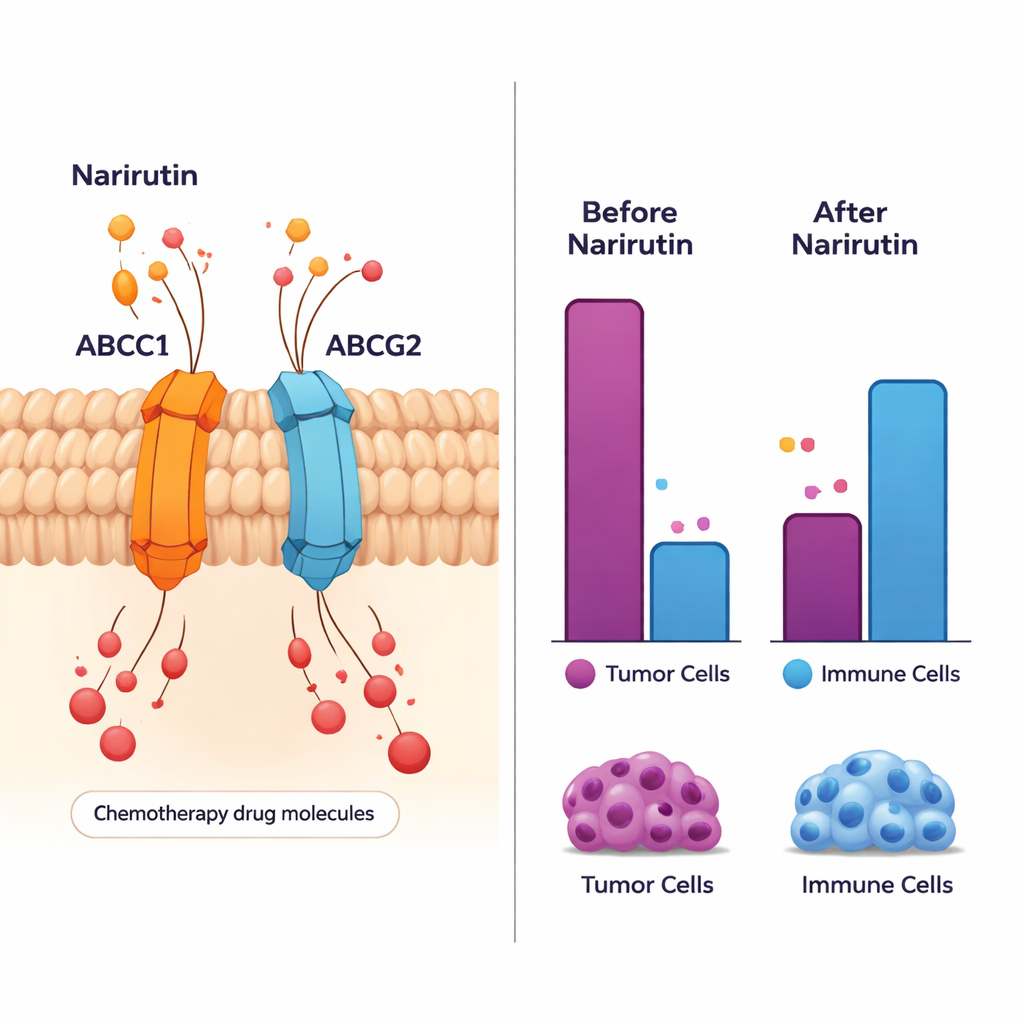
Die Immunnachbarschaft des Tumors umgestalten
Krebs wächst nicht isoliert; er lebt in einem belebten „Viertel“ aus Immunzellen, Blutgefäßen und Stützgewebe. Die Studie untersuchte 28 verschiedene Immunzelltypen in der Umgebung von Darmtumoren und fand im Vergleich zu gesundem Gewebe weitreichende Verschiebungen. Bestimmte hilfreiche Immunzellen, etwa aktivierte B-Zellen und spezifische T-Zellen, waren in Tumoren zahlreicher oder verhielten sich anders. Die Hauptziele von Narirutin, insbesondere ABCC1, ABCG2 und PTGS1, zeigten starke Zusammenhänge mit diesen immunologischen Veränderungen. Das deutet darauf hin, dass Narirutin durch Wirkung auf diese Gene nicht nur direkt Krebszellen beeinflussen, sondern auch die lokale Immunantwort modulieren könnte – möglicherweise so, dass die Umgebung für Tumorwachstum weniger günstig wird.
Verheißungsvoll, aber noch Arbeit nötig
In einfachen Worten schlägt diese Forschung vor, dass ein natürliches Flavonoid aus Zitrusfrüchten die „Pumpen“ stören könnte, mit denen Krebszellen der Chemotherapie entkommen, und dabei helfen könnte, das immunologische Umfeld um Darmtumoren neu zu justieren. Die Arbeit beruht auf leistungsfähigen Computeranalysen und umfangreichen Genetiksätzen, nicht auf Labor- oder klinischen Studien, und stellt daher einen frühen, aber wichtigen Schritt dar. Bestätigen zukünftige Experimente in Zellkulturen, Tiermodellen und klinischen Studien diese Vorhersagen, könnten Narirutin – oder davon inspirierte Wirkstoffe – eines Tages Teil kombinierter Therapien werden, die Standardbehandlungen beim kolorektalen Krebs wirksamer und weniger anfällig für Resistenzen machen.
Zitation: Bian, R., Wang, H., Zhang, H. et al. Integrative machine learning and molecular docking reveal Narirutin targets ABCC1/ABCG2 for immune microenvironment remodeling in colorectal cancer. Sci Rep 16, 7649 (2026). https://doi.org/10.1038/s41598-026-37181-y
Schlüsselwörter: kolorektales Karzinom, narirutin, Arzneimittelresistenz, Tumormikroumgebung, Immunmodulation