Clear Sky Science · de
Multimodale Bildgebung zur Bewertung der hypoxischen Knochenmark-Mikroumgebung und von Typ‑H‑Gefäßschäden bei Diabetes
Warum Knochengesundheit bei Diabetes wichtig ist
Viele verbinden Typ‑1‑Diabetes vor allem mit Blutzucker und Insulin, doch die Erkrankung verändert still und leise auch das Skelett. Viele Betroffene entwickeln schwächere Knochen und haben ein höheres Frakturrisiko, selbst wenn ihre Knochendichtemessungen nahezu normal erscheinen. Diese Studie untersucht, was tief im Knochenmark von Diabetes‑Modellkaninchen geschieht, und nutzt moderne Bildgebung, um winzige Blutgefäße und Sauerstoffverhältnisse in Aktion zu beobachten. Das Verstehen dieser verborgenen Schäden könnte zu früherer Diagnose und neuen Therapien führen, die die Knochensubstanz bei Menschen mit Diabetes schützen.
Die verborgenen Blutautobahnen des Knochens
Im Inneren langer Knochen wie der Tibia liegt ein dichtes Gefäßnetz, das den Knochen nicht nur versorgt, sondern auch sein Wachstum und seine Reparatur steuert. Unter diesen Gefäßen gibt es einen speziellen Subtyp, die sogenannten „Typ‑H“‑Gefäße, die nahe den Enden der Knochen konzentriert sind, wo Wachstumsfugen und aktive Knochenumgestaltung stattfinden. Diese Gefäße transportieren mehr Sauerstoff als andere und sind eng mit der Bildung neuen Knochens verbunden. Bei Typ‑1‑Diabetes hingegen führen lang anhaltend hohe Blutzuckerwerte zu chemischen Nebenprodukten und oxidativem Stress, die dieses fein ausbalancierte System beeinträchtigen können. Die Forschenden wollten in lebenden Tieren visualisieren, wie sich diese Veränderungen in unterschiedlichen Regionen des Knochens entfalten.
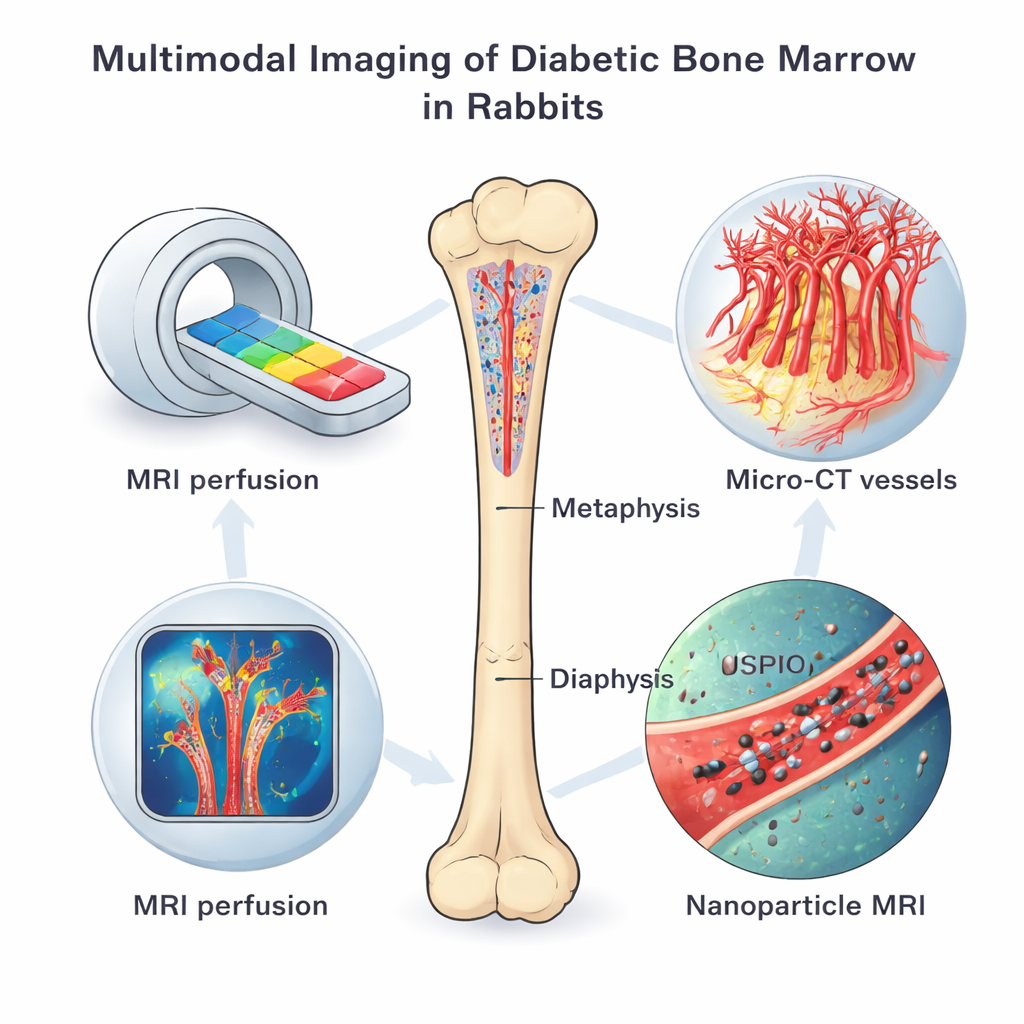
Lebenden Knochen aus mehreren Perspektiven scannen
Das Team setzte eine Reihe von Bildgebungswerkzeugen bei Kaninchen mit chemisch induziertem Typ‑1‑Diabetes und bei gesunden Kontrollen ein, jeweils vier Monate nach Etablierung des Diabetes. Dynamische kontrastverstärkte MRT verfolgte, wie schnell ein Farbstoff in das Knochenmark ein‑ und ausströmte, und zeigte damit, wie gut die feinen Gefäße das Gewebe durchströmten und wie durchlässig sie waren. Ein weiteres MRT‑Verfahren, verstärkt durch spezielle eisenbasierte Nanopartikel, zeigte, wie aktiv die Endothelzellen der Gefäße Partikel aufnahmen — ein Hinweis auf veränderten Stoffwechsel und Gefäßverhalten. Nach der Opferung der Tiere kartierten hochauflösende Mikro‑CT‑Scans das dreidimensionale Netzwerk der Mikrogefäße, während fluoreszente Färbungen, Gentests und Elektronenmikroskopie Gefäßtypen, sauerstoffsensierende Proteine und zelluläre Schäden im Detail untersuchten.
Wo Diabetes im Knochen am stärksten zuschlägt
Über alle Bildgebungsverfahren hinweg zeigten diabetische Kaninchen Knochenmarkgefäße, die durchlässiger und auffälliger waren als die gesunder Tiere. Kontrastmittel bewegte sich schneller und verweilte länger, und Eisen‑Nanopartikel wurden intensiver aufgenommen, besonders in der Metaphyse — der Endregion des Knochens, die reich an Typ‑H‑Gefäßen ist. Die Mikro‑CT zeigte, dass diabetische Knochen deutlich weniger kleine Gefäße und ein geringeres Gesamtkörpervolumen an Gefäßen hatten, so dass der sonst übliche Vorteil der Metaphyse gegenüber dem Schaftbereich verschwand. Durchflusszytometrie und fluoreszente Markierung bestätigten, dass der Anteil an Typ‑H‑Gefäßen selbst im Diabetes stark sank, während neue sprossende Gefäße entlang der Wachstumsfuge selten wurden. Kurz: Die vaskuläre Nische, die normalerweise robustes Knochenwachstum unterstützt, war selektiv ausgedünnt und geschädigt.
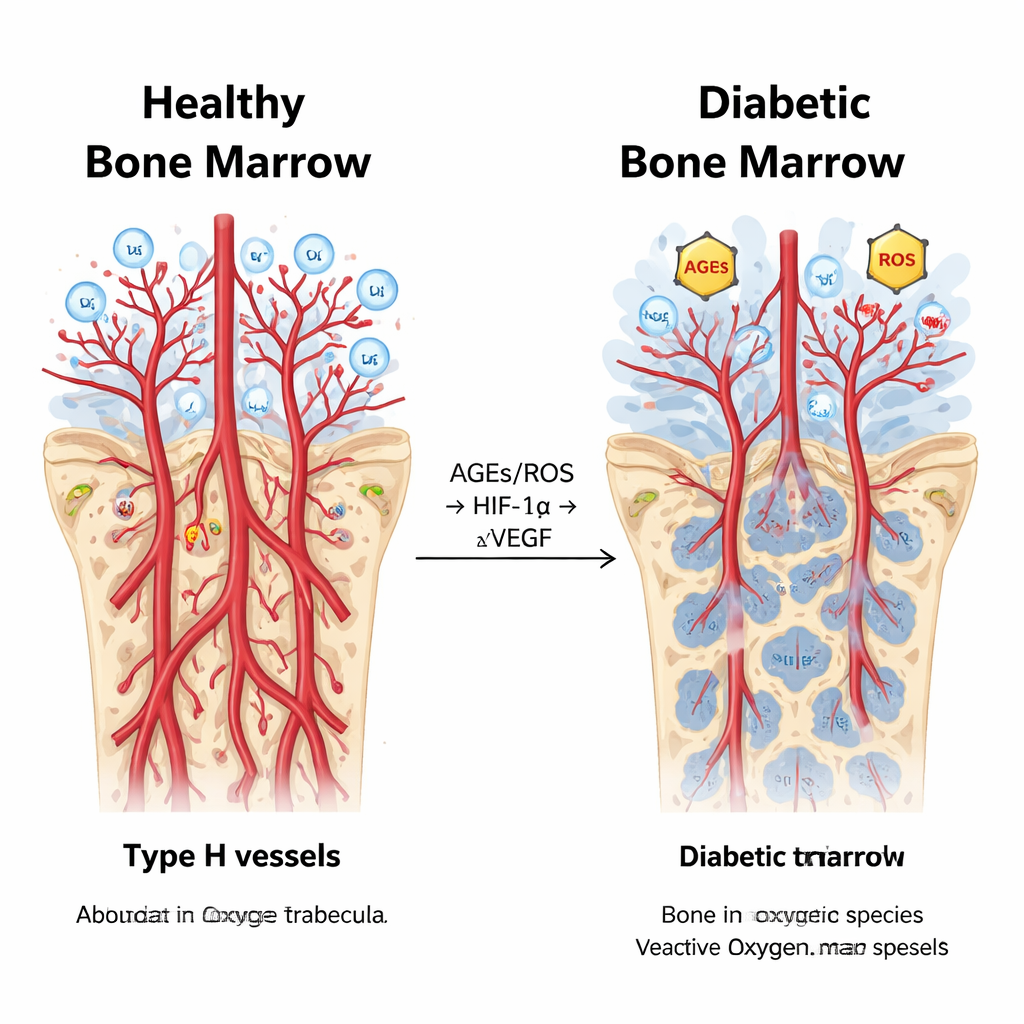
Eine verästelte chemische Kaskade im diabetischen Mark
Bei tieferer Analyse maßen die Forschenden Moleküle, die an Hypoxie — dem Sauerstoffmangel — und am oxidativen Stress durch hohen Blutzucker beteiligt sind. Diabetische Kaninchen wiesen höhere Spiegel an fortgeschrittenen Glykationsendprodukten (AGEs) und reaktiven Sauerstoffspezies (ROS) auf, zusammen mit stärkerer Aktivität des sauerstoffsensierenden Proteins HIF‑1α und seines Rezeptorpartners AGER, insbesondere in der Metaphyse. Überraschenderweise war trotz der normalerweise gefäßfördernden Rolle von HIF‑1α das zentrale Wachstumsignal VEGF im diabetischen Knochenmark tatsächlich unterdrückt, und das Gefäßsprossen nahm ab. Statistische Analysen verbanden diese Befunde: Marker für oxidativen Stress und abnorme Perfusion stiegen und fielen parallel zu HIF‑1α, während VEGF und Maße der Gefäßdichte in die entgegengesetzte Richtung gingen. Dieses Muster deutet darauf hin, dass bei chronischem Diabetes das normale „Sauerstoff‑Alarmsystem“ kapert und Entzündung und Durchlässigkeit fördert, statt gesundes Gefäß‑ und Knochenwachstum.
Was das für Menschen mit Diabetes bedeutet
Kurz gesagt zeigt die Studie, dass Diabetes Knochen nicht gleichmäßig ausdünnt, sondern fleckige „Hotspots“ von Gefäßschäden und Sauerstoffmangel schafft, besonders dort, wo der Knochen am stärksten und regenerativsten sein sollte. Durch die Kombination mehrerer Bildgebungsverfahren konnten die Forschenden sowohl die funktionelle Durchlässigkeit als auch den strukturellen Verlust von Typ‑H‑Gefäßen beobachten und diese Veränderungen mit einem spezifischen chemischen Signalweg verknüpfen, an dem AGEs, ROS, HIF‑1α und VEGF beteiligt sind. Für Patientinnen und Patienten legt diese Arbeit nahe, dass zukünftige Bildgebung möglicherweise frühe Knochenschäden vor Frakturen erkennen kann und dass Therapien, die eine gesunde Sauerstoff‑Signalgebung wiederherstellen und Typ‑H‑Gefäße schützen, eine neue Strategie zur Verhinderung diabetischer Knochenerkrankungen sein könnten.
Zitation: Lei, H., Wang, K., Li, L. et al. Multimodal imaging evaluation of hypoxic bone marrow microenvironment and type H vascular injury in diabetes. Sci Rep 16, 7206 (2026). https://doi.org/10.1038/s41598-026-37164-z
Schlüsselwörter: Typ‑1‑Diabetes, Knochenmark, Mikrogefäßschädigung, Hypoxie, Knochenfragilität